名校
解题方法
1 . 现有 与
与 的混合溶液,为了分析混合溶液中
的混合溶液,为了分析混合溶液中 与
与 的质量分数,设计如下实验方案:取四份混合溶液各
的质量分数,设计如下实验方案:取四份混合溶液各 ,分别缓慢加入到
,分别缓慢加入到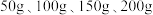 某
某 溶液中,测得四组实验数据如表:
溶液中,测得四组实验数据如表:
(1) 混合溶液与
混合溶液与 溶液完全反应生成沉淀的质量为
溶液完全反应生成沉淀的质量为______ g。
(2)试求出混合溶液中 的溶质质量分数是
的溶质质量分数是______ ?(写出计算过程)
(3)混合溶液中 的溶质质量分数为
的溶质质量分数为______ 。
(4)若在 混合溶液中不断加入上述
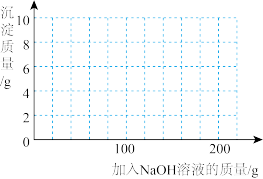
混合溶液中不断加入上述 的溶液,请画出加入
的溶液,请画出加入 溶液的质量与所产生沉淀质量的关系图
溶液的质量与所产生沉淀质量的关系图______ 。(在答题卡的坐标图中作图)
 与
与 的混合溶液,为了分析混合溶液中
的混合溶液,为了分析混合溶液中 与
与 的质量分数,设计如下实验方案:取四份混合溶液各
的质量分数,设计如下实验方案:取四份混合溶液各 ,分别缓慢加入到
,分别缓慢加入到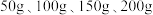 某
某 溶液中,测得四组实验数据如表:
溶液中,测得四组实验数据如表: | 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | 第Ⅳ组 | |
 溶液的质量 溶液的质量 | 50 | 100 | 150 | 200 |
生成沉淀的质量 | 0 | 2.45 | 7.35 | 9.8 |
(1)
 混合溶液与
混合溶液与 溶液完全反应生成沉淀的质量为
溶液完全反应生成沉淀的质量为(2)试求出混合溶液中
 的溶质质量分数是
的溶质质量分数是(3)混合溶液中
 的溶质质量分数为
的溶质质量分数为(4)若在
 混合溶液中不断加入上述
混合溶液中不断加入上述 的溶液,请画出加入
的溶液,请画出加入 溶液的质量与所产生沉淀质量的关系图
溶液的质量与所产生沉淀质量的关系图
您最近一年使用:0次
2 . 加强废旧金属的回收和再利用,是合理开发和利用金属资源的主要途径之一。下图是从镀铜废电路板中回收金属铜的一种工艺流程(各过程需控制适宜条件)。
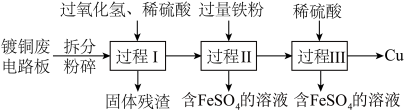
(1)上述流程中,为加快化学反应速率而采取的措施是______ 。
(2)过程Ⅰ中,Cu溶解,过氧化氢的作用是______ 。
(3)过程Ⅱ中,获得Cu的反应的离子方程式为______ 。
(4)过程Ⅲ的目的是______ 。

(1)上述流程中,为加快化学反应速率而采取的措施是
(2)过程Ⅰ中,Cu溶解,过氧化氢的作用是
(3)过程Ⅱ中,获得Cu的反应的离子方程式为
(4)过程Ⅲ的目的是
您最近一年使用:0次
2020-08-04更新
|
300次组卷
|
5卷引用:江苏省宿迁市泗阳县桃州中学2020-2021学年高二上学期第一次调研考试化学试题
名校
3 . 下列物质的转化在给定条件下能实现的是( )
A.MgCO3 MgCl2(aq) MgCl2(aq) 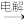 Mg Mg |
B.Cu2(OH)2CO3 CuO CuO Cu(OH)2 Cu(OH)2 |
C.BrCH2COOH HOCH2COOH HOCH2COOH H-[OCH2CO]n-OH H-[OCH2CO]n-OH |
D.NH3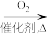 NO NO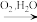 HNO3 HNO3 |
您最近一年使用:0次
名校
4 . 实验室以海绵铜(主要成分为Cu和CuO)为原料制取CuCl的主要流程如图所示。
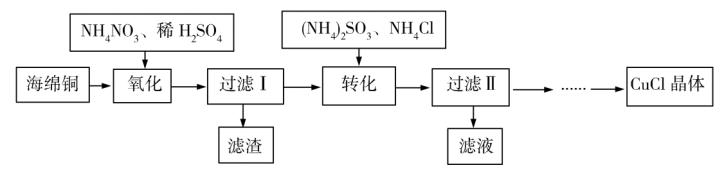
已知:①CuCl微溶于水,不溶于乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl露置于潮湿的空气中易被氧化。
回答下列问题。
(1)“氧化”时温度应控制在60℃~70℃,原因是___ 。
(2)写出“转化”过程中的离子方程式___ 。
(3)“过滤Ⅱ”所得滤液经蒸发浓缩、降温结晶、过滤等操作获得(NH4)2SO4晶体,可用作化学肥料。“过滤Ⅱ”所得滤渣主要成分为CuCl,用乙醇洗涤的优点是___ 。
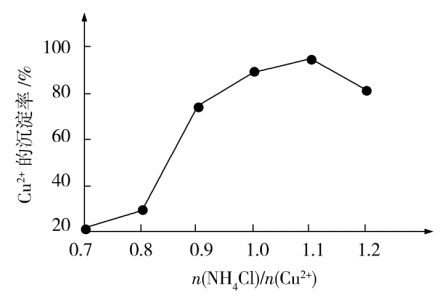
(4)氯化铵用量 与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是
与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是___ 。
(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:___ 。(实验中可选试剂:0.1mol·L-1盐酸、10mol·L-1盐酸、蒸馏水、无水乙醇)

已知:①CuCl微溶于水,不溶于乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl露置于潮湿的空气中易被氧化。
回答下列问题。
(1)“氧化”时温度应控制在60℃~70℃,原因是
(2)写出“转化”过程中的离子方程式
(3)“过滤Ⅱ”所得滤液经蒸发浓缩、降温结晶、过滤等操作获得(NH4)2SO4晶体,可用作化学肥料。“过滤Ⅱ”所得滤渣主要成分为CuCl,用乙醇洗涤的优点是
(4)氯化铵用量
 与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是
与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是
(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:
您最近一年使用:0次
名校
解题方法
5 . 下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将SO2气体通入酸性KMnO4溶液 | 溶液褪色 | SO2具有漂白性 |
| B | 在CuSO4溶液中加入KI溶液,再加入苯,振荡 | 有白色沉淀产生,苯层呈紫红色 | Cu2+有氧化性,白色沉淀可能为CuI |
| C | C2H5OH与浓硫酸共热至170℃,产生的气体通入酸性KMnO4溶液 | 溶液紫红色褪去 | C2H5OH与浓硫酸反应生成了乙烯 |
| D | 向5mL0.1mol·L-1KI溶液中加入1mL0.1mol·L-1FeCl3溶液,振荡,用苯萃取2~3次后,取下层溶液滴加5滴KSCN溶液 | 出现血红色 | 反应2Fe3++2I-=2Fe2++I2是有一定限度的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 在给定条件下,下列选项所示的物质间转化均能实现的是
A.HCl(aq) 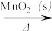 Cl2(g) Cl2(g) 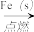 FeCl2(s) FeCl2(s) |
B.Cu(OH)2(s)  CuO(s) CuO(s) 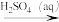 CuSO4(aq) CuSO4(aq) |
C.N2(g) 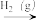 NH3(g) NH3(g) 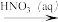 NH4NO3(s) NH4NO3(s) |
D.Al2O3(s) 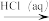 AlCl3(aq) AlCl3(aq)  AlCl3(s) AlCl3(s) |
您最近一年使用:0次
2020-06-21更新
|
237次组卷
|
2卷引用:江苏省扬州市2020届高三6月调研考试化学试题
名校
解题方法
7 . 下列有关物质性质与用途具有对应关系的是( )
| A.硅酸钠溶液呈碱性,可用作木材防火剂 |
| B.硫酸铜溶液呈蓝色,可用作游泳池中水的消毒剂 |
| C.浓硫酸具有强氧化性,可用作酯化反应的催化剂 |
| D.铅具有还原性和导电性,可用作铅蓄电池的负极材料 |
您最近一年使用:0次
2020-06-09更新
|
234次组卷
|
2卷引用:江苏省南京市2020届高三第三次模拟考试(6月) 化学试题
13-14高一上·辽宁沈阳·阶段练习
名校
解题方法
8 . 碳酸铜和碱式碳酸铜[Cu2(OH)2CO3]均可溶于HCl,转化为氯化铜。在高温下这两种化合物均能分解生成氧化铜。溶解28.4 g的上述混合物,消耗1.0 mol/L盐酸500 mL。灼烧等量的上述混合物,得到的氧化铜质量( )
| A.35 g | B.30 g | C.20 g | D.15 g |
您最近一年使用:0次
2020-06-08更新
|
402次组卷
|
17卷引用:江苏省苏州市新实中学2019-2020学年高一上学期第一次(10月)月考试题
江苏省苏州市新实中学2019-2020学年高一上学期第一次(10月)月考试题(已下线)2013-2014学年辽宁省沈阳二中高一上学期12月月考化学试卷2015届辽宁省抚顺市二中高三上学期期中考试化学试卷2014-2015上海市金山中学高一上学期期末考试化学试卷2016届安徽省合肥一六八中学高三上第四次段考化学试卷2016届湖南省长沙市雅礼中学高三上学期月考化学试卷河北省衡水中学2019届高三开学二调考试化学试题安徽省凤阳衡水高考补习学校2019届高三上学期第二次月考化学试题【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高一上学期期末考试化学试题【全国百强校】湖南省长沙市长郡中学2018-2019学年高一下学期开学考试化学试题人教版高一化学必修1第一章—第三章综合测试题(已下线)【南昌新东方】2019 南昌十九中 高一上 期中安徽省阜阳市界首中学2019-2020学年高一下学期期中考试化学试题河北省石家庄市第一中学东校区2022届高三上学期教学质量检测(一)化学试题安徽省当涂第一中学2022-2023学年高一上学期第二次月考化学试题(已下线)专题03 物质的量的基本计算-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第03讲 物质的量在化学方程式计算中的应用(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
解题方法
9 . 某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu(NO3)2的部分工艺流程如图所示:
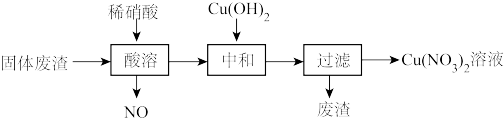
(1)Cu与稀硝酸反应的离子方程式为___ 。
(2)酸溶时,反应温度不宜超过70℃,其主要原因是___ ,若保持反应温度为70℃,欲加快反应速率可采取的措施为___ (写出一种即可)。
(3)过滤后所得废渣的主要成分的化学式为___ 。
(4)Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为___ ,由Cu(NO3)2溶液制备Cu(NO3)2晶体的操作方法是:蒸发浓缩、冷却结晶、过滤、___ 、___ 。

(1)Cu与稀硝酸反应的离子方程式为
(2)酸溶时,反应温度不宜超过70℃,其主要原因是
(3)过滤后所得废渣的主要成分的化学式为
(4)Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为
您最近一年使用:0次
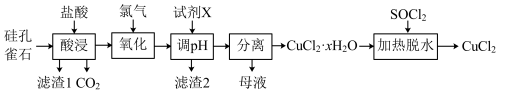
10 . 以硅孔雀石[主要成分为CuCO3·Cu(OH)2、CuSiO3·2H2O,含SiO2、FeCO3、Fe2O3等杂质]为原料制备CuCl2的工艺流程如图:
已知:SOCl2+H2O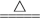 SO2↑+2HCl↑
SO2↑+2HCl↑
(1)“酸浸”时盐酸与CuCO3·Cu(OH)2反应的化学方程式为___ 。为提高“酸浸”时铜元素的浸出率,可以采取的措施有:①适当提高盐酸浓度;②适当提高反应温度;③___ 。
(2)“氧化”时发生反应的离子方程式为___ 。
(3)“滤渣2”的主要成分为___ (填化学式);“调pH”时,pH不能过高,其原因是___ 。

已知:SOCl2+H2O
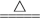 SO2↑+2HCl↑
SO2↑+2HCl↑(1)“酸浸”时盐酸与CuCO3·Cu(OH)2反应的化学方程式为
(2)“氧化”时发生反应的离子方程式为
(3)“滤渣2”的主要成分为
您最近一年使用:0次



