名校
解题方法
1 . 印刷线路板废液(主要成分有Cu2+、Fe2+、Fe3+、H+、Cl-),可用来制备碱式碳酸铜,过程如图:
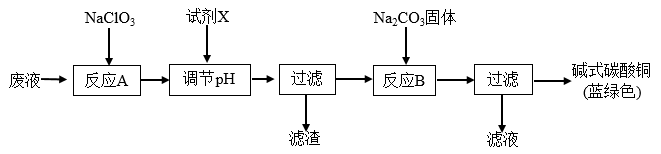
下列说法正确的是( )

下列说法正确的是( )
| A.反应A的离子方程式为:10Fe2++2ClO3-+12H+=10Fe3++Cl2↑+6H2O |
| B.铜在空气中被腐蚀得到铜锈,其主要成分是碱式碳酸铜 |
| C.NaClO3和Na2CO3中心原子杂化类型均为sp3杂化 |
| D.试剂X可为CuO,主要作用是通过调节pH值把Fe2+转化为Fe(OH)3过滤除去 |
您最近一年使用:0次
2020-05-13更新
|
302次组卷
|
4卷引用:山东省新高考质量测评联盟2020届高三5月联考化学试题
山东省新高考质量测评联盟2020届高三5月联考化学试题江苏省扬州中学2021-2022学年高二下学期6月月考化学试题江苏省连云港市灌南二中、南师大灌云附中2022-2023学年高二下学期第二次阶段性检测化学试题(已下线)押广东卷化学第15题 离子方程式正误判断-备战2022年高考化学临考题号押题(广东卷)
名校
解题方法
2 . 已知酸性条件下有如下反应:2Cu+=Cu2++Cu。由于反应温度不同,用氢气还原氧化铜时,可能产生Cu或Cu2O,两者都是红色固体。某同学对氢气还原氧化铜实验所得的红色固体产物进行验证,每一次实验操作和实验现象记录如下,由此推出氢气还原氧化铜实验的产物是( ).
| 加入试剂 | 稀硫酸 | 浓硫酸 | 稀硝酸 | 浓硝酸 |
| 实验现象 | 产生红色固体,溶液呈蓝色 | 加热,产生无色气体 | 产生无色气体,溶液呈蓝色 | 产生红棕色气体,溶液呈绿色 |
| A.只有Cu |
| B.只有Cu2O |
| C.一定有Cu,可能有Cu2O |
| D.一定有Cu2O,可能有Cu |
您最近一年使用:0次
2020-03-06更新
|
284次组卷
|
8卷引用:江苏省启东中学2020年人教版高中化学必修1期末复习第二章 化学物质及其变化(三)
江苏省启东中学2020年人教版高中化学必修1期末复习第二章 化学物质及其变化(三)2017届新疆生产建设兵团二中高三上第一次月考化学试卷2018届高三一轮复习化学:考点21-铜及其化合物性质探究福建省厦门双十中学2016-2017学年高一下学期第一次月考化学试题(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第4讲 金属材料与矿物 铜及其化合物 (题型专练)(已下线)2019年1月17日 《每日一题》高考二轮复习-铜及其化合物(已下线)第三单元 物质的性质与转化(基础过关)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)(已下线)专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练
3 . 工业上由含铜废料(含有Cu、CuS、CuSO4等)制备硝酸铜晶体的流程如图:
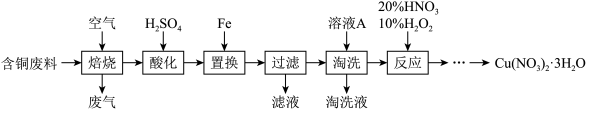
(1)“焙烧”时CuS转化为CuO和SO2,反应的化学方程式为___ 。
(2)“酸化”步骤反应的离子方程式为___ 。
(3)“过滤”所得滤液中溶质的主要成分为___ 。
(4)“淘洗”所用的溶液A应选用___ (填序号)。
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”一步的过程中无红棕色气体生成。
①理论上消耗HNO3和H2O2的物质的量之比为___ 。
②若不加10% H2O2,只用浓HNO3,随着反应的进行,容器内持续出现大量红棕色气体,写出该反应的离子方程式____ 。
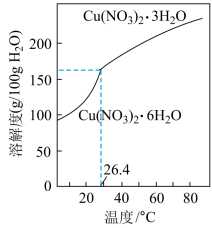
(6)由“反应”所得溶液中尽可能多地析出Cu(NO3)2·3H2O晶体的方法是___ 。(相关物质的溶解度曲线如图所示)

(1)“焙烧”时CuS转化为CuO和SO2,反应的化学方程式为
(2)“酸化”步骤反应的离子方程式为
(3)“过滤”所得滤液中溶质的主要成分为
(4)“淘洗”所用的溶液A应选用
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”一步的过程中无红棕色气体生成。
①理论上消耗HNO3和H2O2的物质的量之比为
②若不加10% H2O2,只用浓HNO3,随着反应的进行,容器内持续出现大量红棕色气体,写出该反应的离子方程式
(6)由“反应”所得溶液中尽可能多地析出Cu(NO3)2·3H2O晶体的方法是

您最近一年使用:0次
4 . 氧化亚铜(Cu2O)是一种用途广泛的光电材料,某工厂以硫化铜矿石(含 CuFeS2、Cu2S等)为原料制取Cu2O的工艺流程如下:
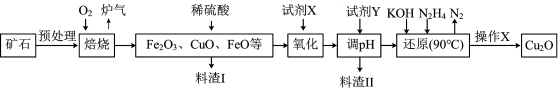
(1) “焙烧”时,提高反应速率的措施有____________ (写一条)。
(2)炉气中的有害气体成分是__________ 。
(3)若试剂X是H2O2溶液,写出相应反应的离子方程式:_________ 。

(1) “焙烧”时,提高反应速率的措施有
(2)炉气中的有害气体成分是
(3)若试剂X是H2O2溶液,写出相应反应的离子方程式:
您最近一年使用:0次
2019-12-25更新
|
116次组卷
|
2卷引用:江苏省太仓市明德高级中学2019-2020学年高二上学期合格性考试模拟化学试题
解题方法
5 . 我国很早就使用青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
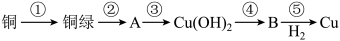
(1)从物质分类标准看,“铜绿”属于___ (填字母)。
A.酸 B.碱 C.盐 D.氧化物
(2)请写出铜绿与盐酸反应的离子方程式:___ 。
(3)上述转化过程中属于氧化还原反应的是___ (填序号)
(4)铜绿在受热时可直接分解生成物质B、CO2和水,其分解的化学方程式为___ 。

(1)从物质分类标准看,“铜绿”属于
A.酸 B.碱 C.盐 D.氧化物
(2)请写出铜绿与盐酸反应的离子方程式:
(3)上述转化过程中属于氧化还原反应的是
(4)铜绿在受热时可直接分解生成物质B、CO2和水,其分解的化学方程式为
您最近一年使用:0次
名校
6 . 将1.60gCuSO4固体在高温下加热,得到0.72g红色固体(纯净物,不含S元素),同时有气体X生成,X可能是SO2、SO3、O2中的两种或三种。下列说法正确的是
| A.所得红色固体是铜 |
| B.将X通入氢氧化钡溶液,若溶液变浑浊,则X中含有SO3 |
| C.X的物质的量最少为0.01mol |
| D.将X缓慢通过足量NaOH溶液,若溶液增重0.72g,则X中含0.005molO2 |
您最近一年使用:0次
2010·江苏泰州·一模
7 . 已知在酸性条件下能发生下列反应:Cu+→Cu+Cu2+(未配平)。NH4CuSO3与足量的10 mol∙L−1硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法一定合理的是
| A.该反应显示硫酸具有酸性 |
| B.NH4CuSO3中硫元素被氧化 |
| C.刺激性气味的气体是氨气 |
| D.反应中硫酸作氧化剂 |
您最近一年使用:0次
名校
解题方法
8 . 为探究黑色固体 X(仅含两种元素)的组成和性质,设计并完成如下实验:
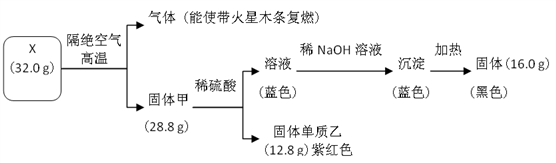
请回答:
(1)X 的化学式是______________ 。
(2)写出蓝色溶液转化为蓝色沉淀的离子方程式是______________ 。
(3)写出固体甲与稀硫酸反应的化学方程式______________ 。

请回答:
(1)X 的化学式是
(2)写出蓝色溶液转化为蓝色沉淀的离子方程式是
(3)写出固体甲与稀硫酸反应的化学方程式
您最近一年使用:0次
2018-03-14更新
|
471次组卷
|
3卷引用:浙江省舟山中学2017-2018学年高一下学期开学考试化学试题
解题方法
9 . Cu2O是一种几乎不溶于水的氧化物,在涂料、玻璃等领域应用非常广泛。一种以硫化铜矿石(含CuFeS2、Cu2S 等) 为原料制取Cu2O 的工艺流程如下:

(1)“硫酸化焙烧”时:①硫化铜矿需粉碎的目的是_________ ;②CuS 与O2反应生成CuSO4等物质的化学方程式为________ ;③加入Na2SO4的作用除减小物料间黏结外,另一主要作用是__________ 。
(2)“浸取”时为提高铜的浸取率,除需控制硫酸的浓度外,还需控制_________ (至少列举两点)。
(3)“制备”时,溶液的pH与Cu2O 的产率关系如右图所示。
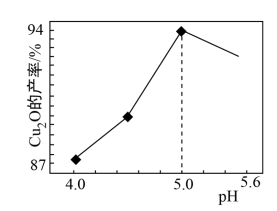
①在100℃时,发生反应的离子方程式为__________
②图中在4<pH<5 时,pH越小产率越低且产品中杂质Cu的含量越高,是因为________ 。

(1)“硫酸化焙烧”时:①硫化铜矿需粉碎的目的是
(2)“浸取”时为提高铜的浸取率,除需控制硫酸的浓度外,还需控制
(3)“制备”时,溶液的pH与Cu2O 的产率关系如右图所示。

①在100℃时,发生反应的离子方程式为
②图中在4<pH<5 时,pH越小产率越低且产品中杂质Cu的含量越高,是因为
您最近一年使用:0次
10 . A~J是中学化学中常见的化学物质,它们之间的相互转化关系如下列框图所示(部分反应的产物未列出)。

已知:A、F为无色气体单质,B为无色具有刺激性气味的碱性气体,C为黑色氧化物,E为红色金属单质。请回答下列问题:
(1)D的化学式为_____________ ;F的电子式为______________ 。
(2)B和C反应的化学方程式为_______________ 。该反应中生成1molF时,转移的电子数为_________ mol
(3)E与G的稀溶液反应的离子方程式为:____________________ 。
(4)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式___________________ 。

已知:A、F为无色气体单质,B为无色具有刺激性气味的碱性气体,C为黑色氧化物,E为红色金属单质。请回答下列问题:
(1)D的化学式为
(2)B和C反应的化学方程式为
(3)E与G的稀溶液反应的离子方程式为:
(4)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式
您最近一年使用:0次



