解题方法
1 . 下列离子方程式中,正确的是
A. 和稀盐酸反应: 和稀盐酸反应: |
B. 溶液与过量氨水反应: 溶液与过量氨水反应: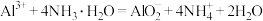 |
C. 溶液与稀硫酸反应: 溶液与稀硫酸反应: |
D. 溶液与 溶液与 溶液反应: 溶液反应: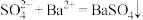 |
您最近一年使用:0次
2023-05-03更新
|
153次组卷
|
2卷引用:贵州省遵义市红花岗区2022-2023学年高一下学期4月期中联考化学试题
解题方法
2 . 回答下列问题:
(1)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即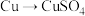 ;
;
方案乙:由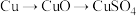 。
。
这两种方案,你认为哪一种方案更合理?_______ ,理由是_______ 。
(2)氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
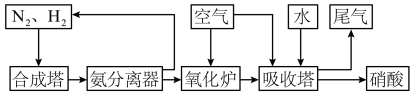
①合成塔中发生反应的化学方程式为_______ 。
②向吸收塔中通入空气的作用是_______ 。
③氧化炉中发生反应的化学方程式为_______ 。标准状况下,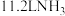 被氧化为
被氧化为 时转移电子的数目为
时转移电子的数目为_______ 。
④吸收塔中出来的尾气 可用具有碱性的
可用具有碱性的 溶液吸收,其中
溶液吸收,其中 既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:
既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:_______ 。
(1)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即
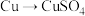 ;
;方案乙:由
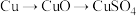 。
。这两种方案,你认为哪一种方案更合理?
(2)氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

①合成塔中发生反应的化学方程式为
②向吸收塔中通入空气的作用是
③氧化炉中发生反应的化学方程式为
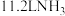 被氧化为
被氧化为 时转移电子的数目为
时转移电子的数目为④吸收塔中出来的尾气
 可用具有碱性的
可用具有碱性的 溶液吸收,其中
溶液吸收,其中 既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:
既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:
您最近一年使用:0次
名校
3 . 某校化学研究性学习小组设计实验验证NH3能还原CuO,并对还原产物进行探究。请回答下列问题:
Ⅰ.验证NH3能还原CuO
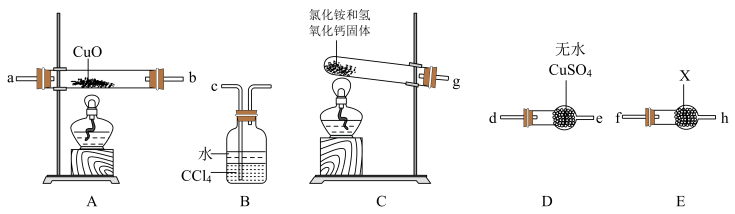
(1)装置C中发生的反应化学方程式为___________ 。
(2)试剂X为___________ 。
(3)请将提供的装置按合理顺序连接:g→___________ 。
(4)装置B的作用是___________ 。
(5)证明NH3能还原CuO的实验现象是___________ 。
Ⅱ.探究还原产物的成分
[查阅资料] Cu2O粉末呈红色,在酸性溶液中不稳定:
Cu2O+H2SO4(稀)=Cu+CuSO4+H2O。
[实验探究]
(6)
Ⅰ.验证NH3能还原CuO

(1)装置C中发生的反应化学方程式为
(2)试剂X为
(3)请将提供的装置按合理顺序连接:g→
(4)装置B的作用是
(5)证明NH3能还原CuO的实验现象是
Ⅱ.探究还原产物的成分
[查阅资料] Cu2O粉末呈红色,在酸性溶液中不稳定:
Cu2O+H2SO4(稀)=Cu+CuSO4+H2O。
[实验探究]
(6)
| 实验操作 | 实验现象 | 实验结论 |
| 取10.4g红色固体于烧杯中,加入足量稀硫酸,充分搅拌,静置 | 若无现象 | 证明红色固体为 |
| 若 | 证明红色固体肯定含有Cu2O,可能含有Cu |
您最近一年使用:0次
名校
解题方法
4 . 在无色强酸性溶液中,能大量共存的一组离子是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
解题方法
5 . 下列物质对应的化学式不正确的是
| A.重晶石:BaSO4 | B.纯碱:Na2CO3 |
| C.胆矾:CuSO4·5H2O | D.石膏:CaSO4 |
您最近一年使用:0次
6 . 孔雀石古称石绿,是铜的表生矿物[化学式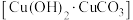 ,“水色”从植物中提取,如花青(分子式
,“水色”从植物中提取,如花青(分子式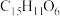 )。下列说法错误的是
)。下列说法错误的是
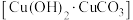 ,“水色”从植物中提取,如花青(分子式
,“水色”从植物中提取,如花青(分子式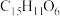 )。下列说法错误的是
)。下列说法错误的是| A.“石绿”耐酸、耐碱 | B.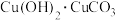 属于纯净物 属于纯净物 |
| C.保存不善的国画,“水色”容易变色 | D.从蓝草中提取花青,可用有机溶剂萃取 |
您最近一年使用:0次
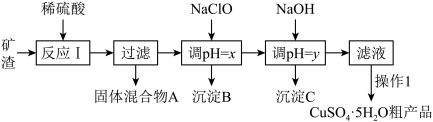
7 . 某铜矿石的主要成分为Cu2O,还含有少量Al2O3、Fe2O3、SiO2。工业上用该矿石获取铜和胆矾的操作流程如下:
已知:①Cu2O+2H+=Cu+Cu2++H2O
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)实际生产中将矿石粉碎为矿渣的目的是___________ 。
(2)固体混合物A中含有较多的铜,加入某试剂可以提纯铜。该反应的离子方程式为___________ 。
(3)反应Ⅰ完成后的滤液中铁元素的存在形式为___________ (填离子符号),检验该离子常用的试剂为___________ ,生成该离子的离子方程式为___________ 。
(4)加入NaClO调节溶液pH可生成沉淀B,利用题中所给信息,沉淀B为___________ ,该反应中氧化剂与还原剂物质的量之比为___________ 。
(5)加入NaOH调节pH,得到沉淀C,利用题中所给信息分析y的范围___________ 。
(6)操作1主要包括:蒸发浓缩、冷却结晶、过滤、 冷水洗涤得到CuSO4·5H2O。如何洗涤CuSO4·5H2O粗品___________ 。

已知:①Cu2O+2H+=Cu+Cu2++H2O
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 5.4 | 4.0 | 2.7 | 5.8 |
| 沉淀完全的pH | 6.7 | 5.2 | 3.7 | 8.8 |
(1)实际生产中将矿石粉碎为矿渣的目的是
(2)固体混合物A中含有较多的铜,加入某试剂可以提纯铜。该反应的离子方程式为
(3)反应Ⅰ完成后的滤液中铁元素的存在形式为
(4)加入NaClO调节溶液pH可生成沉淀B,利用题中所给信息,沉淀B为
(5)加入NaOH调节pH,得到沉淀C,利用题中所给信息分析y的范围
(6)操作1主要包括:蒸发浓缩、冷却结晶、过滤、 冷水洗涤得到CuSO4·5H2O。如何洗涤CuSO4·5H2O粗品
您最近一年使用:0次
2023-04-17更新
|
262次组卷
|
2卷引用:黑龙江省哈尔滨市第四中学校2022-2023学年高一下学期4月月考化学试题
名校
解题方法
8 . 下列是两种制备 的方式
的方式
甲: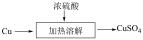
乙: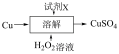
下列说法正确的是
 的方式
的方式甲:

乙:

下列说法正确的是
| A.从环境保护角度分析方案甲更好 |
| B.乙方案中试剂X为稀盐酸 |
C.若用方案甲制备 会产生 会产生 |
D.方案乙“溶解”时发生反应的离子方程式为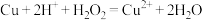 |
您最近一年使用:0次
2023-04-16更新
|
97次组卷
|
2卷引用:湖北省宜昌市协作体2022-2023学年高一下学期期中考试化学试题
名校
解题方法
9 . 氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业,是难溶于水的白色固体,能溶解于硝酸,在潮湿空气中可被迅速氧化。实验室用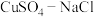 混合液与
混合液与 溶液反应制取CuCl。相关装置及数据如图:
溶液反应制取CuCl。相关装置及数据如图:

回答以下问题:
(1)图甲中仪器1的名称是___________ ;制备过程中 过量会发生副反应生成
过量会发生副反应生成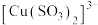 ,为提高产率,仪器2中所加试剂应为
,为提高产率,仪器2中所加试剂应为___________ 。
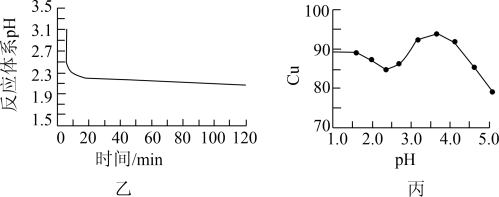
(2)如图乙所示是体系pH随时间变化关系图,写出制备CuCl的离子方程式___________ 。丙图是产率随pH变化关系图,实验过程中往往用 混合溶液代替
混合溶液代替 溶液,其中
溶液,其中 的作用是
的作用是___________ ,为保证较高产率pH应维持在___________ 左右。
(3)反应完成后经抽滤、洗涤、干燥获得产品。洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是___________ 。
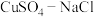 混合液与
混合液与 溶液反应制取CuCl。相关装置及数据如图:
溶液反应制取CuCl。相关装置及数据如图:
回答以下问题:
(1)图甲中仪器1的名称是
 过量会发生副反应生成
过量会发生副反应生成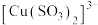 ,为提高产率,仪器2中所加试剂应为
,为提高产率,仪器2中所加试剂应为(2)如图乙所示是体系pH随时间变化关系图,写出制备CuCl的离子方程式
 混合溶液代替
混合溶液代替 溶液,其中
溶液,其中 的作用是
的作用是
(3)反应完成后经抽滤、洗涤、干燥获得产品。洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是
您最近一年使用:0次
10 . 工业上由含铜废料(含有Cu、CuS、 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
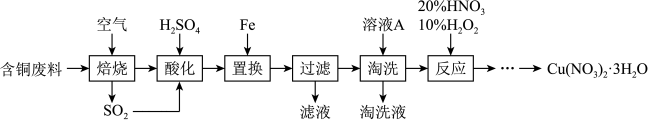
(1)写出CuS“焙烧”生成 和CuO的化学反应方程式:
和CuO的化学反应方程式:___________ 。
(2)图中 经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol
经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol  与1mol
与1mol  充分反应,所得生成物的分子数
充分反应,所得生成物的分子数___________ (填“大于2 ”、“等于2
”、“等于2 ”或“小于2
”或“小于2 ”)。
”)。 属于
属于___________ (填“酸性”或“碱性”)氧化物。
(3)“过滤”所得的滤液中溶质的主要成分为___________ 。
(4)“淘洗”所用的溶液A应选用___________ (填序号)
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”步骤中,10% 为氧化剂,20%
为氧化剂,20%  提供
提供 ,可以避免污染性气体的产生。写出该反应的离子方程式:
,可以避免污染性气体的产生。写出该反应的离子方程式:___________ 。
(6)有一份氧化铁、氧化铜和铁粉组成的混合物,将其投入到3mol/L 200mL的盐酸中,充分反应后,产生标准状况下的 896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中
896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中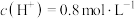 。则原混合物中铁粉的物质的量为
。则原混合物中铁粉的物质的量为___________ 。
 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
(1)写出CuS“焙烧”生成
 和CuO的化学反应方程式:
和CuO的化学反应方程式:(2)图中
 经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol
经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol  与1mol
与1mol  充分反应,所得生成物的分子数
充分反应,所得生成物的分子数 ”、“等于2
”、“等于2 ”或“小于2
”或“小于2 ”)。
”)。 属于
属于(3)“过滤”所得的滤液中溶质的主要成分为
(4)“淘洗”所用的溶液A应选用
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”步骤中,10%
 为氧化剂,20%
为氧化剂,20%  提供
提供 ,可以避免污染性气体的产生。写出该反应的离子方程式:
,可以避免污染性气体的产生。写出该反应的离子方程式:(6)有一份氧化铁、氧化铜和铁粉组成的混合物,将其投入到3mol/L 200mL的盐酸中,充分反应后,产生标准状况下的
 896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中
896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中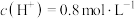 。则原混合物中铁粉的物质的量为
。则原混合物中铁粉的物质的量为
您最近一年使用:0次



