解题方法
1 . 下列反应的离子方程式书写正确的是
A.碳酸钙与稀盐酸反应: +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
| B.金属钠加入硫酸铜溶液的反应中:2Na+CuSO4=Na2SO4+Cu |
| C.铜片插入硝酸银溶液中:Cu+2Ag+=Cu2++2Ag |
| D.氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
您最近一年使用:0次
解题方法
2 . 铜器由于时间久远,表面有一层绿锈,绿锈俗称“铜绿”,是铜和空气中的水蒸气、O2、CO2作用产生的,其化学式为Cu2(OH)2CO3。下列关于“铜绿”的说法正确的是


| A.推测“铜绿”是绿色易溶于水的固体 |
| B.“铜绿”属于碱 |
| C.用稀盐酸可除去铜器表面的“铜绿”,但会损伤铜器 |
D.“铜绿”受热分解的化学方程式为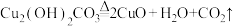 |
您最近一年使用:0次
3 . 回答下列问题
(1)下图为铁及其化合物的“价-类”二维图。
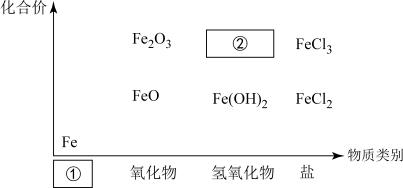
填写二维图缺失的类别 ①___________ 和化学式②___________ 。
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2 ②Fe ③NaOH ④H2SO4 ⑤AgNO3
从物质类别 上看,FeCl3属于___________ ,可能与___________ 发生反应(填序号);从化合价角度看,Fe3+具有___________ 性,可能与___________ 发生反应(填序号)。
(3)宋代《千里江山图》描绘了山清水秀的美丽景色,来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),
经千年色彩依然,其中绿色来自蓝铜矿(主要成分为Cu(OH)2·2CuCO3)。其中Cu(OH)2·2CuCO3属于___________ (填“纯净物”或“混合物”),请写出Cu(OH)2·2CuCO3与盐酸反应的化学方程式 ___________
(4)酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,H3PO2水溶液中存在H3PO2分子。
①H3PO2属于___________ 酸;NaH2PO2为___________ 盐(填序号)
a. 一元酸 b.二元酸 c.三元酸 d.强酸 e.弱酸 f.正盐 g.酸式盐
②写出H3PO2溶液与足量NaOH溶液反应的化学方程式___________ 。
(1)下图为铁及其化合物的“价-类”二维图。

填写二维图缺失的
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2 ②Fe ③NaOH ④H2SO4 ⑤AgNO3
从物质
(3)宋代《千里江山图》描绘了山清水秀的美丽景色,来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),
经千年色彩依然,其中绿色来自蓝铜矿(主要成分为Cu(OH)2·2CuCO3)。其中Cu(OH)2·2CuCO3属于
(4)酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,H3PO2水溶液中存在H3PO2分子。
①H3PO2属于
a. 一元酸 b.二元酸 c.三元酸 d.强酸 e.弱酸 f.正盐 g.酸式盐
②写出H3PO2溶液与足量NaOH溶液反应的化学方程式
您最近一年使用:0次
4 . 秦始皇兵马俑是世界文化遗产,下列对于兵马俑使用颜料的主要成分与其类别的对应关系正确的是
| 选项 | A | B | C | D |
| 颜色 | 绿色 | 棕红色 | 大红色 | 黑色 |
| 主要成分 | 石绿[Cu2(OH)2CO3] | 赭石(Fe2O3) | 朱砂(HgS) | 炭黑(C) |
| 类别 | 碱 | 酸性氧化物 | 电解质 | 有机物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 .  是一种重要的化工原料,其有关制备途径及性质如图所示。
是一种重要的化工原料,其有关制备途径及性质如图所示。

下列说法错误的是
 是一种重要的化工原料,其有关制备途径及性质如图所示。
是一种重要的化工原料,其有关制备途径及性质如图所示。
下列说法错误的是
| A.Y可以是甲酸乙酯 |
B.制取等量的 ,途径①消耗的 ,途径①消耗的 是途径②的2倍 是途径②的2倍 |
C.“混合气体”中一定含有 |
| D.在①~⑤中,Cu元素被氧化的反应有3个 |
您最近一年使用:0次
名校
解题方法
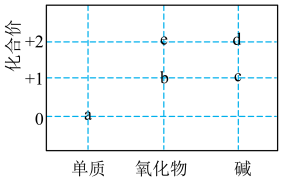
6 . 部分含 或含
或含 物质的分类与相应化合价的关系如图所示。下列推断不合理的是
物质的分类与相应化合价的关系如图所示。下列推断不合理的是
 或含
或含 物质的分类与相应化合价的关系如图所示。下列推断不合理的是
物质的分类与相应化合价的关系如图所示。下列推断不合理的是
| A.a变成e可以加入强氧化剂 | B.能与 反应生成c的物质只有b 反应生成c的物质只有b |
C.可存在 的转化 的转化 | D.b可以反应生成a和e |
您最近一年使用:0次
名校
解题方法
7 . 下列各组离子在无色酸性溶液中可以大量共存的有
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
8 . 氯化铜晶体(CuCl2·2H2O)常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗制氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:

已知:氯化亚砜( 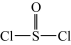 )熔点-101℃,沸点76℃,易水解。回答下列问题:
)熔点-101℃,沸点76℃,易水解。回答下列问题:
(1)为避免引入杂质,试剂x可选用___________ (填字母)
a.KMnO4溶液 b.Cl2水 c.Br2水 d.H2O2溶液
(2)溶液C中加入试剂y可以调节溶液pH,控制pH的取值范围为______~________________ ,从而除去Fe3+而不引入杂质。试剂y可选用下列物质中的___________ (填字母)
a.Cu b.CuO c.Cu2(OH)2CO3 d.NaOH
(3)SOCl2与水反应的化学方程式为___________ 。
(4)SOCl2与CuCl2·2H2O混合并加热,可得到无水CuCl2的原因是__________________ 。

| Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 7.0 | 4.7 |
| 沉淀完全的pH | 3.2 | 9.0 | 6.7 |
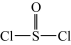 )熔点-101℃,沸点76℃,易水解。回答下列问题:
)熔点-101℃,沸点76℃,易水解。回答下列问题:(1)为避免引入杂质,试剂x可选用
a.KMnO4溶液 b.Cl2水 c.Br2水 d.H2O2溶液
(2)溶液C中加入试剂y可以调节溶液pH,控制pH的取值范围为______~_____
a.Cu b.CuO c.Cu2(OH)2CO3 d.NaOH
(3)SOCl2与水反应的化学方程式为
(4)SOCl2与CuCl2·2H2O混合并加热,可得到无水CuCl2的原因是
您最近一年使用:0次
名校
解题方法
9 . 2023年10月央视的节目《只此青绿》,提到了颜料石绿{铜绿,又名孔雀石,主要成分是碱式碳酸铜[Cu2(OH)2CO3]}。某同学利用下述反应实现了“铜→铜绿→……→Cu”的转化。回答下列问题:
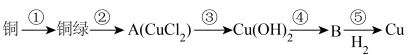
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:______
(2)A、B在无色火焰上灼烧时,其焰色______ (填“相同”或“不相同”),该原理是______ (填“物理”或“化学”)变化。
(3)完成步骤②和③可选用的试剂分别为______ 、______ 。(填标号)
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
(4)若在该转化过程中有2mol氧化铜生成,则该氧化铜的质量为多少______ ?(写出计算过程)
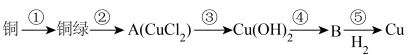
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:
(2)A、B在无色火焰上灼烧时,其焰色
(3)完成步骤②和③可选用的试剂分别为
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
(4)若在该转化过程中有2mol氧化铜生成,则该氧化铜的质量为多少
您最近一年使用:0次
名校
解题方法
10 . 碱式碳酸铜[ ,相对分子质量为222]可用作有机催化剂。工业上以辉铜矿(主要成分为
,相对分子质量为222]可用作有机催化剂。工业上以辉铜矿(主要成分为 ,含
,含 及少量
及少量 )为原料制备碱式碳酸铜,工业流程如下:
)为原料制备碱式碳酸铜,工业流程如下:
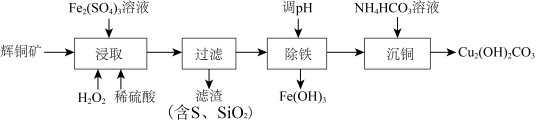
(1)“浸取”时能提高辉铜矿Cu浸取率的措施有___________ (填2条)
(2)某小组测得Cu浸取率随 浓度及温度影响的变化曲线如下:
浓度及温度影响的变化曲线如下:

①由图一可知 适宜的浓度范围为
适宜的浓度范围为___________ ;
②由图一中的a点分析,浸取时 也起到了氧化辉铜矿的作用,该反应的离子方程式为
也起到了氧化辉铜矿的作用,该反应的离子方程式为___________ 。
③图二中高于85℃时Cu浸取率下降的原因是___________ 。
(3)①“除铁”步骤调pH可加入试剂___________ (填选项字母);
a.HCl b.NaOH c.CuO d.
②常温下,“过滤”后的滤液中 ,则“除铁”步骤调pH应小于
,则“除铁”步骤调pH应小于___________ 。[常温下,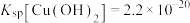 ]。
]。
(4)某实验小组为测定碱式碳酸铜的纯度,取制得的碱式碳酸铜产品5.0g,加适量硫酸,再加100mL水,加热溶解,冷却后配成250mL溶液。量取配成的25.00mL溶液于碘量瓶中,加入适量缓冲溶液控制溶液的pH在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用 的
的 溶液进行滴定,至临近滴定终点时再加入1mL淀粉溶液做指示剂,继续滴入
溶液进行滴定,至临近滴定终点时再加入1mL淀粉溶液做指示剂,继续滴入 溶液至滴定终点。平行测定3次,实验数据如下表所示。
溶液至滴定终点。平行测定3次,实验数据如下表所示。
已知: ,
,
①判断滴定到达终点的现象是___________ ;
②根据表中数据计算实验小组制得的碱式碳酸铜的纯度为___________ 。
(5)对下列几种假定情况进行讨论(填“偏高”、“偏低”或“无影响”);
①装 溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失,对测定结果的影响是
溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失,对测定结果的影响是___________ ;
②读 溶液体积时,若滴定前仰视,滴定后俯视,对测定结果的影响是
溶液体积时,若滴定前仰视,滴定后俯视,对测定结果的影响是___________ 。
 ,相对分子质量为222]可用作有机催化剂。工业上以辉铜矿(主要成分为
,相对分子质量为222]可用作有机催化剂。工业上以辉铜矿(主要成分为 ,含
,含 及少量
及少量 )为原料制备碱式碳酸铜,工业流程如下:
)为原料制备碱式碳酸铜,工业流程如下:
(1)“浸取”时能提高辉铜矿Cu浸取率的措施有
(2)某小组测得Cu浸取率随
 浓度及温度影响的变化曲线如下:
浓度及温度影响的变化曲线如下:
①由图一可知
 适宜的浓度范围为
适宜的浓度范围为②由图一中的a点分析,浸取时
 也起到了氧化辉铜矿的作用,该反应的离子方程式为
也起到了氧化辉铜矿的作用,该反应的离子方程式为③图二中高于85℃时Cu浸取率下降的原因是
(3)①“除铁”步骤调pH可加入试剂
a.HCl b.NaOH c.CuO d.

②常温下,“过滤”后的滤液中
 ,则“除铁”步骤调pH应小于
,则“除铁”步骤调pH应小于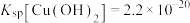 ]。
]。(4)某实验小组为测定碱式碳酸铜的纯度,取制得的碱式碳酸铜产品5.0g,加适量硫酸,再加100mL水,加热溶解,冷却后配成250mL溶液。量取配成的25.00mL溶液于碘量瓶中,加入适量缓冲溶液控制溶液的pH在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用
 的
的 溶液进行滴定,至临近滴定终点时再加入1mL淀粉溶液做指示剂,继续滴入
溶液进行滴定,至临近滴定终点时再加入1mL淀粉溶液做指示剂,继续滴入 溶液至滴定终点。平行测定3次,实验数据如下表所示。
溶液至滴定终点。平行测定3次,实验数据如下表所示。已知:
 ,
,
| 实验编号 | 滴定前 溶液的体积读数/mL 溶液的体积读数/mL | 滴定后 溶液的体积读数/mL 溶液的体积读数/mL |
| 1 | 0.10 | 20.12 |
| 2 | 1.20 | 23.21 |
| 3 | 1.50 | 21.48 |
②根据表中数据计算实验小组制得的碱式碳酸铜的纯度为
(5)对下列几种假定情况进行讨论(填“偏高”、“偏低”或“无影响”);
①装
 溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失,对测定结果的影响是
溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失,对测定结果的影响是②读
 溶液体积时,若滴定前仰视,滴定后俯视,对测定结果的影响是
溶液体积时,若滴定前仰视,滴定后俯视,对测定结果的影响是
您最近一年使用:0次



