17. 用甲烷制高纯氢气是目前研究热点之一。回答下列问题:
(1)一定条件下,CH
4(g)⇌C(s)+2H
2(g)的反应历程如图1所示,其中化学反应速率最慢的反应过程为
_______。

(2)工业上常利用甲烷与水蒸气重整制氢,涉及热化学反应方程式如下:
Ⅰ.CH
4(g)+H
2O(g)⇌CO(g)+3H
2(g) △H
1=+206kJ/mol
Ⅱ.CO(g)+H
2O(g)⇌CO
2 (g)+H
2(g) △H
1=-41kJ/mol
①总反应:CH
4(g)+2H
2O(g)⇌CO
2(g)+4H
2(g)
△H=
_______kJ/mol。
②为提高CH
4的平衡转化率,可采取的措施有
_______(写一条)。
③已知830℃时,反应Ⅱ的平衡常数K=1。在容积不变的密闭容器中,将2molCO(g)与8molH
2O(g)加热到830℃,反应达平衡时CO的转化率为
_______。
④在常压、600℃条件下,甲烷与水蒸气制备氢气的总反应中H
2平衡产率为82%。若加入适量生石灰后H
2的产率可提高到95%。应用化学平衡移动原理解释原因
_______。
(3)利用甲烷与CO
2重整制氢的热化学反应方程式如下:
Ⅲ.CH
4(g)+CO
2(g)⇌2CO(g)+2H
2(g) △H
3>0(主反应)
Ⅳ.H
2(g)+CO
2(g)⇌H
2O(g)+CO(g) △H
4>0(副反应)
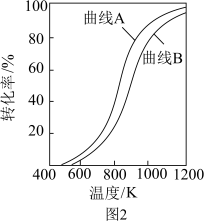
①在恒压条件下。等物质的量的CH
4(g)和CO
2(g)发生重整反应时,各物质的平衡转化率随温度变化如图2所示,则表示CO
2平衡转化率的是曲线
_______(填“A”或“B”)。
②在一刚性密闭容器中,CH
4(g)和CO
2(g)的分压分别为20kPa、25kPa,忽略副反应,达到平衡后测得体系压强是起始时的1.8倍,则该反应的Kp=
_______kPa
2(列出计算式即可)。
(4)科学家研究将CH
4(g)、H
2O(g)与CH
4(g)、CO
2(g)联合重整制备氢气,发生反应Ⅰ和Ⅲ.常压下,将CH
4(g)、H
2O(g)和CO
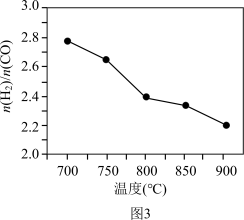
2(g)按一定比例混合置于密闭容器中,相同时间不同温度下测得体系中

变化如图3所示。
①已知700℃、NiO催化条件下,向反应体系中加入少量O
2可增加H
2产率,此条件下还原性CO
_______H
2(填“>”、“<”或“=”)。
②随着温度升高

变小的原因可能是
_______。