解题方法
1 . 某实验室模拟以粗盐(含杂质Mg2+、Ca2+、K+和 )为原料进行生产并综合利用的某过程如下图所示。已知:Ksp[Mg(OH)2]=5.6×10-12;Ksp[CaMg(CO3)2]<< Ksp[Mg(OH)2]。
)为原料进行生产并综合利用的某过程如下图所示。已知:Ksp[Mg(OH)2]=5.6×10-12;Ksp[CaMg(CO3)2]<< Ksp[Mg(OH)2]。
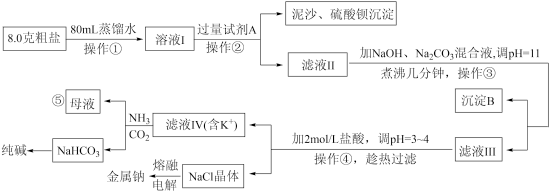
(1)过量试剂A是_________________________ 溶液。(填名称)
(2)图为KCI和NaCl的溶解度曲线,连续操作④是_____________________________ 。

(3)向滤液IV中通入NH3CO2气体后能够得到NaHCO3的原因是_______________ (用必要的化学用语和文字说明)。
(4)已知碳酸的Ka2=5.6×10-11,次氯酸的Ka=3×10-8,工业上用饱和纯碱溶液代替烧碱溶液与Cl2反应生产有效成分为次氯酸钠的消毒液,反应的化学方程式是___________________________________ 。
(5)经检测,滤液Ⅲ中c(Mg2+)<1.0×10-7mol/L,则镁元素最终沉淀物是_________________ 。
(6)⑤处母液可以生产氮肥NH4Cl,NH4Cl可用于制取具有漂白作用的三氯化氮。工业上制备NCl3的一种方法是用图所示装置电解,其原理是NH4Cl+2HCl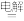 NC13十3H2↑。
NC13十3H2↑。
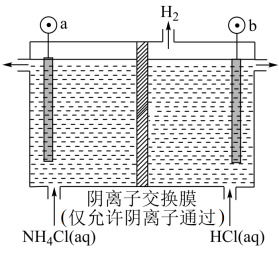
阳极反应式是___________________________________ 。
(7)电解氯化钠时需要加入一定量氯化钙,根据学习过的电解知识推测加入氯化钙的主要作用是_____________ 。
 )为原料进行生产并综合利用的某过程如下图所示。已知:Ksp[Mg(OH)2]=5.6×10-12;Ksp[CaMg(CO3)2]<< Ksp[Mg(OH)2]。
)为原料进行生产并综合利用的某过程如下图所示。已知:Ksp[Mg(OH)2]=5.6×10-12;Ksp[CaMg(CO3)2]<< Ksp[Mg(OH)2]。
(1)过量试剂A是
(2)图为KCI和NaCl的溶解度曲线,连续操作④是

(3)向滤液IV中通入NH3CO2气体后能够得到NaHCO3的原因是
(4)已知碳酸的Ka2=5.6×10-11,次氯酸的Ka=3×10-8,工业上用饱和纯碱溶液代替烧碱溶液与Cl2反应生产有效成分为次氯酸钠的消毒液,反应的化学方程式是
(5)经检测,滤液Ⅲ中c(Mg2+)<1.0×10-7mol/L,则镁元素最终沉淀物是
(6)⑤处母液可以生产氮肥NH4Cl,NH4Cl可用于制取具有漂白作用的三氯化氮。工业上制备NCl3的一种方法是用图所示装置电解,其原理是NH4Cl+2HCl
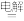 NC13十3H2↑。
NC13十3H2↑。
阳极反应式是
(7)电解氯化钠时需要加入一定量氯化钙,根据学习过的电解知识推测加入氯化钙的主要作用是
您最近一年使用:0次
2020-05-27更新
|
1009次组卷
|
2卷引用:辽宁省部分中学2019-2020高一下学期期末考试化学试题
名校
2 . 通过CH4超干重整CO2技术可得到富含CO的化工原料,其过程如下图所示。下列说法错误的是( )
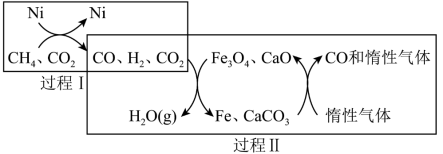
A.过程Ⅰ的化学方程式为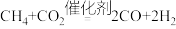 |
B.过程Ⅱ的化学方程式为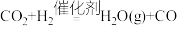 |
| C.该技术实现了含碳物质与含氢物质的分离 |
| D.Ni、Fe、CaCO3均是上述过程中用到的催化剂 |
您最近一年使用:0次
2019-10-13更新
|
2136次组卷
|
6卷引用:河南省大象联考2020届高三高考质量测评化学试题
解题方法
3 . 人类的生产生活离不开金属材料,金属及金属材料在生产、生活中应用广泛。
(1)生活中常用的铁锅炒菜,主要是利用了铁的_______ ;铁在潮湿的空气中容易锈蚀,喷漆可以延缓汽车钢铁外壳的锈蚀,起防锈原理是隔绝___________ ,喷漆前需将铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),观察到溶液变黄,有无色气泡逸出,写出其中涉及到的一个化学方程式:___________________ 。
(2)化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:
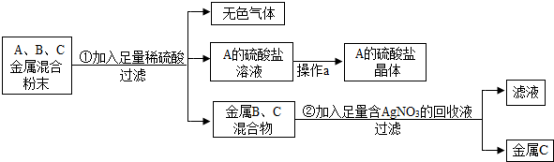
①A、B、C三种金属的活动性顺序为___________________ 。
②金属C是____________ ,已知A的硫酸盐中A元素显+2价,请写出步骤①的反应的化学方程式:________________________________________ 。
(1)生活中常用的铁锅炒菜,主要是利用了铁的
(2)化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:

①A、B、C三种金属的活动性顺序为
②金属C是
您最近一年使用:0次
4 . (I)含硫化合物的种类很多,现有SO2、Na2SO3、H2SO4、CuSO4这4种常见的含硫化合物。回答下列问题:
(1)为进一步减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2。写出该反应的化学方程式:___________________ 。
(2)亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
__ Na2SO3+__ KIO3+__ H2SO4 =__ Na2SO4+__ K2SO4+ __ I2+ __ H2O。
①配平上面的氧化还原反应方程式。
②其中氧化剂是________ ,若反应中有5 mol电子转移,则生成的碘单质是________ mol。
(3)向FeCl3和BaCl2的酸性混合溶液中通入SO2气体,有白色沉淀生成。此沉淀是______ 。
A.BaSO4 B.FeS C.BaSO3 D.S
(4)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面________________ ,则发生了钝化。
(II)A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大2,C原子的电子总数比B原子电子总数多4,1molA单质跟盐酸反应可置换出11.2L(标准状况下)氢气,这时A转变成与氖原子具有相同电子层结构的离子.试回答:
(1)A是____ 元素,C是______ 元素.
(2)分别写出A、B最高价氧化物对应水化物分别跟C的气态氢化物水溶液反应的离子方程式:______________ 、_____________ 。
(1)为进一步减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2。写出该反应的化学方程式:
(2)亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
①配平上面的氧化还原反应方程式。
②其中氧化剂是
(3)向FeCl3和BaCl2的酸性混合溶液中通入SO2气体,有白色沉淀生成。此沉淀是
A.BaSO4 B.FeS C.BaSO3 D.S
(4)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面
(II)A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大2,C原子的电子总数比B原子电子总数多4,1molA单质跟盐酸反应可置换出11.2L(标准状况下)氢气,这时A转变成与氖原子具有相同电子层结构的离子.试回答:
(1)A是
(2)分别写出A、B最高价氧化物对应水化物分别跟C的气态氢化物水溶液反应的离子方程式:
您最近一年使用:0次



