1 . I.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
①如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量的变化示意图,请问该化学反应属于___ (放热或吸热)反应,请写出该反应的热化学方程式:___ 。
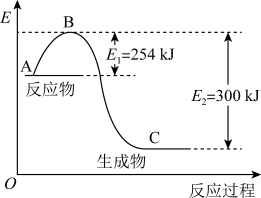
②上述反应用到的氢气是一种清洁燃料,已知氢气的燃烧热为285.8 kJ·mol-1,请写出氢气的燃烧热热化学方程式:___ 。
II.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1。回答有关中和反应的问题。
(1)如图装置中仪器A的名称__ ,碎泡沫塑料的作用是___ 。
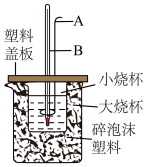
(2)若通过实验测定中和热,其数值常常小于57.3kJ·mol-1,其原因可能是___ 。
①如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量的变化示意图,请问该化学反应属于

②上述反应用到的氢气是一种清洁燃料,已知氢气的燃烧热为285.8 kJ·mol-1,请写出氢气的燃烧热热化学方程式:
II.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1。回答有关中和反应的问题。
(1)如图装置中仪器A的名称

(2)若通过实验测定中和热,其数值常常小于57.3kJ·mol-1,其原因可能是
您最近一年使用:0次
2019-10-30更新
|
165次组卷
|
2卷引用:贵州省凯里市第一中学2019-2020学年高二上学期期中考试化学(理)试题
名校
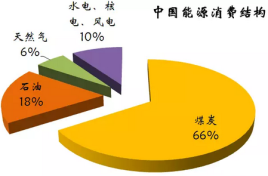
2 . 下图为我国目前的能源消费结构图:
(1)由图中数据可知,一定时期内,我国的能源结构仍以煤炭为主,但直接燃烧煤炭的弊端是____ 。
(2)将煤转化为水煤气可有效降低煤对环境的破坏性,能量变化如图所示:
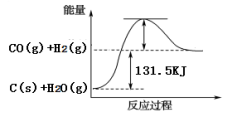
根据以上数据,写出该反应的热化学方程式_________________ ;
(3)甲醇是重要的化学工业基础原料和清洁液体燃料。将煤液化将克服直接将煤作为燃料的不足。其反应原理为CO2(g)+3H2(g) CH3OH(g) +H2O(g)。
CH3OH(g) +H2O(g)。
①在适当的催化剂作用下,该反应能自发进行。则该反应ΔH______ 0(填“>”、“<”或“=”)
②在体积一定的密闭容器中发生该反应,达到平衡后升高温度,下列说法正确的是______ 。
A.平衡正向移动 B.达到新的平衡后体系的压强增大
C.H2的转化率增大 D.体系的密度增大
③下列叙述能说明此反应达到平衡状态的是_______ 。(填字母)
a.混合气体的平均相对分子质量保持不变
b.1 mol CO2生成的同时有3 mol H—H键断裂
c.CO2的转化率和H2的转化率相等
d.混合气体的密度保持不变
④在相同起始温度(500℃)、起始体积相同(2L)的三个密闭容器中分别进行该反应,控制不同条件,反应过程中部分数据见下表:
查阅资料发现500℃时该反应的平衡常数为2.5。则反应Ⅰ在10min时v正______ v逆,则反应均达到平衡时,反应Ⅰ、Ⅱ对比H2的百分含量关系w%Ⅰ(H2)______ w%Ⅱ(H2),反应Ⅰ、Ⅲ对比:平衡时CH3OH的浓度c(I)_______ c(Ⅲ)(本小题均用“>”、“<”或“=”填空)。
(1)由图中数据可知,一定时期内,我国的能源结构仍以煤炭为主,但直接燃烧煤炭的弊端是
(2)将煤转化为水煤气可有效降低煤对环境的破坏性,能量变化如图所示:


根据以上数据,写出该反应的热化学方程式
(3)甲醇是重要的化学工业基础原料和清洁液体燃料。将煤液化将克服直接将煤作为燃料的不足。其反应原理为CO2(g)+3H2(g)
 CH3OH(g) +H2O(g)。
CH3OH(g) +H2O(g)。①在适当的催化剂作用下,该反应能自发进行。则该反应ΔH
②在体积一定的密闭容器中发生该反应,达到平衡后升高温度,下列说法正确的是
A.平衡正向移动 B.达到新的平衡后体系的压强增大
C.H2的转化率增大 D.体系的密度增大
③下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变
b.1 mol CO2生成的同时有3 mol H—H键断裂
c.CO2的转化率和H2的转化率相等
d.混合气体的密度保持不变
④在相同起始温度(500℃)、起始体积相同(2L)的三个密闭容器中分别进行该反应,控制不同条件,反应过程中部分数据见下表:
| 反应时间 | CO2/mol | H2/mol | CH3OH/mol | H2O/mol | |
| 反应Ⅰ:恒温恒容 | 0 min | 2 | 6 | 0 | 0 |
| 10 min | 4.5 | ||||
| 反应Ⅱ:恒温恒压 | 0 min | 1 | 3 | 1 | 1 |
| 反应Ⅲ:绝热恒容 | 0 min | 0 | 0 | 2 | 2 |
查阅资料发现500℃时该反应的平衡常数为2.5。则反应Ⅰ在10min时v正
您最近一年使用:0次
3 . 高炉煤气为炼铁过程中产生的副产品,主要成分为N2、CO、CO2、H2O等,其中可燃成分CO含量约占25%左右,CO2、N2的含量分别占15%、55%。回答下列问题:
(1)上述提及的气体分子中,电子数相等的两种气体是_____________ (写化学式)。
(2)CO 可以用于生产甲醇,甲醇是一种重要的化工原料,有着重要的用途和应用前景。工业生产甲醇的常用方法是:CO(g)+2H2(g)=CH3OH (g) △H=-90.8kJ/mol
已知:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ·mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ`mol-1
①H2的燃烧热为___________________ kJ/mol。
②CH3OH(g)+O2(g) CO(g) +2H2O(g) 的反应热△H=
CO(g) +2H2O(g) 的反应热△H=___________________ 。
③若在恒温恒容的容器内进行反应CO (g) +2H2 (g) CH3OH (g),则可用来判断该反应达到平衡状态的标志有
CH3OH (g),则可用来判断该反应达到平衡状态的标志有______________________ 。(填字母)
A.CO 百分含量保持不变B.容器中H2浓度与CO浓度相等
C.容器中混合气体的密度保持不变D.CO 的生成速率与CH3OH 的生成速率相等
(3)高炉煤气中N2的含量较高,利用CO前需要对CO进行富集,实现CO和N2的分离。工业上常采用醋酸亚铜氨溶液来吸收CO,该反应的热化学方程式为CH3COOCu(NH3)2(aq)+CO(g) CH3COOCu(NH3)2·CO(aq)△H<0。吸收CO后的溶液经过适当处理可恢复为醋酸亚铜氨溶液,从而实现CO与吸收液的分离,分离过程可采取的措施有
CH3COOCu(NH3)2·CO(aq)△H<0。吸收CO后的溶液经过适当处理可恢复为醋酸亚铜氨溶液,从而实现CO与吸收液的分离,分离过程可采取的措施有______________ (写出一种即可)。
(1)上述提及的气体分子中,电子数相等的两种气体是
(2)CO 可以用于生产甲醇,甲醇是一种重要的化工原料,有着重要的用途和应用前景。工业生产甲醇的常用方法是:CO(g)+2H2(g)=CH3OH (g) △H=-90.8kJ/mol
已知:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ·mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ`mol-1
①H2的燃烧热为
②CH3OH(g)+O2(g)
 CO(g) +2H2O(g) 的反应热△H=
CO(g) +2H2O(g) 的反应热△H=③若在恒温恒容的容器内进行反应CO (g) +2H2 (g)
 CH3OH (g),则可用来判断该反应达到平衡状态的标志有
CH3OH (g),则可用来判断该反应达到平衡状态的标志有A.CO 百分含量保持不变B.容器中H2浓度与CO浓度相等
C.容器中混合气体的密度保持不变D.CO 的生成速率与CH3OH 的生成速率相等
(3)高炉煤气中N2的含量较高,利用CO前需要对CO进行富集,实现CO和N2的分离。工业上常采用醋酸亚铜氨溶液来吸收CO,该反应的热化学方程式为CH3COOCu(NH3)2(aq)+CO(g)
 CH3COOCu(NH3)2·CO(aq)△H<0。吸收CO后的溶液经过适当处理可恢复为醋酸亚铜氨溶液,从而实现CO与吸收液的分离,分离过程可采取的措施有
CH3COOCu(NH3)2·CO(aq)△H<0。吸收CO后的溶液经过适当处理可恢复为醋酸亚铜氨溶液,从而实现CO与吸收液的分离,分离过程可采取的措施有
您最近一年使用:0次
2017-11-29更新
|
122次组卷
|
2卷引用:湖北省华中师范大学第一附属中学2017-2018学年高二上学期期中考试化学试题
4 . CO是合成尿素、甲酸的原料。
(1)在l00kPa和TK下,由稳定单质生成1mol化合物的焓变称为该物质在TK时的标准摩尔生成焓,用符号△H0表示。已知石墨和一氧化碳的燃烧热分别为393.5kJ/mol和283.0 kJ/mol,则CO(g)的△H0=________ 。
(2)合成尿素的反应:2NH3(g)+CO (g)=CO(NH2)2(g)+H2(g) △H = -81.0kJ/mol;T℃时,在体积为2L的恒容密闭容器中,将2 mol的NH3和1mol CO混合反应,5 min时,NH3的转化率为80%。则0—5min平均反应速率为v(CO)=_____________ 。

则:K1_________ 126.5(填“>”或“< ”);其判断理由是_________________ 。若保持恒温恒容条件,将物质的量之和为3 mol的NH3和CO以不同的氨碳比进行反应,结果如图所示:

① 若图中c表示平衡体系中尿素的体积分数,则a表示________ 的转化率。
②当 =
=____________ 时,尿素含量最大;此时,对于该反虚既能增大正反应速率又能使平衡正向移动的措施是______________ (写一种)。
(3)通过人工光合作用可将CO转化成HCOOH。已知常温下,浓度均为0.1 mol/L的HCOOH和HCOONa混合溶液pH =3.7,则HCOOH的电离常数Ka=___________ (已知lg2=0.3)。用电化学可消除H COOH对水质造成的污染,其原理是电解CoSO4、稀硫酸和HCOOH混合溶液,用电解产生的Co3+将HCOOH氧化成CO2。
COOH对水质造成的污染,其原理是电解CoSO4、稀硫酸和HCOOH混合溶液,用电解产生的Co3+将HCOOH氧化成CO2。
①Co3+氧化HCOOH的离子方程式为___________ ;
②忽略体积变化,电解前后Co2+的浓度将___________ (填“增大”、“减小”或“不变”)。
(1)在l00kPa和TK下,由稳定单质生成1mol化合物的焓变称为该物质在TK时的标准摩尔生成焓,用符号△H0表示。已知石墨和一氧化碳的燃烧热分别为393.5kJ/mol和283.0 kJ/mol,则CO(g)的△H0=
(2)合成尿素的反应:2NH3(g)+CO (g)=CO(NH2)2(g)+H2(g) △H = -81.0kJ/mol;T℃时,在体积为2L的恒容密闭容器中,将2 mol的NH3和1mol CO混合反应,5 min时,NH3的转化率为80%。则0—5min平均反应速率为v(CO)=

则:K1

① 若图中c表示平衡体系中尿素的体积分数,则a表示
②当
 =
=(3)通过人工光合作用可将CO转化成HCOOH。已知常温下,浓度均为0.1 mol/L的HCOOH和HCOONa混合溶液pH =3.7,则HCOOH的电离常数Ka=
 COOH对水质造成的污染,其原理是电解CoSO4、稀硫酸和HCOOH混合溶液,用电解产生的Co3+将HCOOH氧化成CO2。
COOH对水质造成的污染,其原理是电解CoSO4、稀硫酸和HCOOH混合溶液,用电解产生的Co3+将HCOOH氧化成CO2。①Co3+氧化HCOOH的离子方程式为
②忽略体积变化,电解前后Co2+的浓度将
您最近一年使用:0次
5 . “温室效应”是哥奉哈根世界气候变化大会研究的环境问题之一。CO2气体在大气层中具有吸热和隔热的功能,是主要的温室气体。
(1)下列措施中,有利于降低大气中CO2浓度的是 (填字母编号)。
a.采用节能技术,减少化石燃料的用量
b.鼓励乘坐公交车出行,倡导“低碳”生活
c.利崩太阳能、风能等新型能源替代化石燃料
(2)CH4是另一种主要的温室气体,l克甲烷完全燃烧生成液态水和二氧化碳,放出55.64 kJ的热量,甲烷的燃烧热是 。
(3)酸阿的形成主要是由废气中的SOx和NOx造成的。通过SO2和Br2、H2O的定量反应在电解池中产生的电流变化,可以准确测定空气中SO2的含量。该反应的化学方程式为 ,反应中氧化产物和还原产物的物质的量之比为 。
(4)某硫酸工厂以黄铁矿为原料生产硫酸。
第一阶段燃烧黄铁矿的化学方程式为 ;
第二阶段的反应原理是2SO2(g)+O2(g)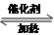 2SO3(g),其生产设备的名称为 ;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为2mol/L、2mol/L、3mol/L,当反应达到平衡时,可能存在的数据是 ___(填字母编号)。
2SO3(g),其生产设备的名称为 ;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为2mol/L、2mol/L、3mol/L,当反应达到平衡时,可能存在的数据是 ___(填字母编号)。
a. SO2为5mol/L,O2为3.5mol/L b. SO2为3mol/L
c.SO2、SO3均为2.5mol/L d.SO3为5mol/L
(1)下列措施中,有利于降低大气中CO2浓度的是 (填字母编号)。
a.采用节能技术,减少化石燃料的用量
b.鼓励乘坐公交车出行,倡导“低碳”生活
c.利崩太阳能、风能等新型能源替代化石燃料
(2)CH4是另一种主要的温室气体,l克甲烷完全燃烧生成液态水和二氧化碳,放出55.64 kJ的热量,甲烷的燃烧热是 。
(3)酸阿的形成主要是由废气中的SOx和NOx造成的。通过SO2和Br2、H2O的定量反应在电解池中产生的电流变化,可以准确测定空气中SO2的含量。该反应的化学方程式为 ,反应中氧化产物和还原产物的物质的量之比为 。
(4)某硫酸工厂以黄铁矿为原料生产硫酸。
第一阶段燃烧黄铁矿的化学方程式为 ;
第二阶段的反应原理是2SO2(g)+O2(g)
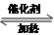 2SO3(g),其生产设备的名称为 ;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为2mol/L、2mol/L、3mol/L,当反应达到平衡时,可能存在的数据是 ___(填字母编号)。
2SO3(g),其生产设备的名称为 ;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为2mol/L、2mol/L、3mol/L,当反应达到平衡时,可能存在的数据是 ___(填字母编号)。a. SO2为5mol/L,O2为3.5mol/L b. SO2为3mol/L
c.SO2、SO3均为2.5mol/L d.SO3为5mol/L
您最近一年使用:0次
9-10高二下·河北石家庄·期中
解题方法
6 . (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,16.0gN2H4在氧气中完全燃烧生成氮气,放出热量312kJ(25℃时),写出表示N2H4燃烧热的热化学方程式 。
(2)甲烷----氧气燃料电池以20%~30%的KOH溶液为电解质溶液。
正极的电极反应式是 。
负极的电极反应式是 。
(3)右图是一个电化学过程示意图。
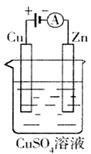
①锌片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标标准状况下的空气 L(假设空气中氧气体积含量为20%)
(2)甲烷----氧气燃料电池以20%~30%的KOH溶液为电解质溶液。
正极的电极反应式是 。
负极的电极反应式是 。
(3)右图是一个电化学过程示意图。

①锌片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标标准状况下的空气 L(假设空气中氧气体积含量为20%)
您最近一年使用:0次



