名校
解题方法
1 . Ⅰ.已知:
①
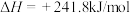
②
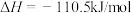
③

请填写下列空白。
(1)上述反应中属于吸热反应的是_______ (填序号)。
(2)
 完全燃烧生成水蒸气,放出的热量为
完全燃烧生成水蒸气,放出的热量为_______ 。
Ⅱ.由于亚硝酸钠和食盐性状相似,曾多次发生过将 误当食盐食用的事件。欲测定某样品中
误当食盐食用的事件。欲测定某样品中 的含量,某同学设计如下实验:①称取样品
的含量,某同学设计如下实验:①称取样品 ,加水溶解,配制成
,加水溶解,配制成 溶液。②取
溶液。②取 溶液于锥形瓶中,用
溶液于锥形瓶中,用
 标准溶液(酸性)进行滴定,滴定结束后消耗
标准溶液(酸性)进行滴定,滴定结束后消耗 溶液
溶液 。
。
(3)上述实验①所需玻璃仪器除烧杯、玻璃棒、胶头滴管之外还有_______ 。
(4)在进行滴定操作时, 溶液盛装在
溶液盛装在_______ (填“酸式”或“碱式”)滴定管中。当滴入最后半滴 溶液,
溶液,_______ 时达到滴定终点。
(5)滴定过程中发生反应的离子方程式是_______ ;测得该样品中 的质量分数为
的质量分数为_______ 。
(6)以下操作造成测定结果偏高的是_______ 。
A.滴定管未用 标准溶液润洗
标准溶液润洗
B.锥形瓶未用待测液润洗
C.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失
D.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后俯视读数
E.若滴定过程中刚出现颜色变化就停止滴定
①

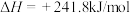
②

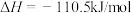
③


请填写下列空白。
(1)上述反应中属于吸热反应的是
(2)

 完全燃烧生成水蒸气,放出的热量为
完全燃烧生成水蒸气,放出的热量为Ⅱ.由于亚硝酸钠和食盐性状相似,曾多次发生过将
 误当食盐食用的事件。欲测定某样品中
误当食盐食用的事件。欲测定某样品中 的含量,某同学设计如下实验:①称取样品
的含量,某同学设计如下实验:①称取样品 ,加水溶解,配制成
,加水溶解,配制成 溶液。②取
溶液。②取 溶液于锥形瓶中,用
溶液于锥形瓶中,用
 标准溶液(酸性)进行滴定,滴定结束后消耗
标准溶液(酸性)进行滴定,滴定结束后消耗 溶液
溶液 。
。(3)上述实验①所需玻璃仪器除烧杯、玻璃棒、胶头滴管之外还有
(4)在进行滴定操作时,
 溶液盛装在
溶液盛装在 溶液,
溶液,(5)滴定过程中发生反应的离子方程式是
 的质量分数为
的质量分数为(6)以下操作造成测定结果偏高的是
A.滴定管未用
 标准溶液润洗
标准溶液润洗B.锥形瓶未用待测液润洗
C.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失
D.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后俯视读数
E.若滴定过程中刚出现颜色变化就停止滴定
您最近一年使用:0次
名校
解题方法
2 . 一些烷烃的燃烧热如下表:
下列表达正确的是
| 化合物 | 燃烧热 |
| 甲烷 | 891.0 |
| 乙烷 | 1560.8 |
| 丙烷 | 2221.5 |
| 正丁烷 | 2878.0 |
| 异丁烷 | 2869.6 |
| 2-甲基丁烷 | 3531.3 |
A.正戊烷的燃烧热大于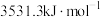 |
| B.稳定性:正丁烷>异丁烷 |
C.乙烷燃烧的热化学方程式为 |
| D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
您最近一年使用:0次
名校
3 . 完成下列问题。
(1)在 时,
时, 在足量的氧气中充分燃烧生成二氧化硫,放出
在足量的氧气中充分燃烧生成二氧化硫,放出 的热量,则表示S的燃烧热的热化学方程式为
的热量,则表示S的燃烧热的热化学方程式为___________ 。
(2)现有反应: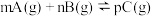 ,达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
,达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
①该反应的逆反应为___________ 热反应,且
___________ p(填“>”、“=”或“<”)。
②减压时,A的质量分数___________ 。(填“增大”、“减小”或“不变”,下同)
③若加入B(体积不变),则A的转化率___________ 。
④若升高温度,则平衡时B、C的浓度之比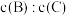 将
将___________ 。
⑤若加入催化剂,平衡时气体混合物的总物质的量___________ 。
⑥若B是有色物质,A、C均无色,则加入C(体积不变)后混合物颜色___________ ;(填“变深”、“变浅”或“不变”,下同)维持容器内压强不变,充入氖气后,混合物颜色___________ 。
(3)已知相同条件下
反应I:
反应Ⅱ:
则反应
___________ 。(用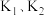 表示)。
表示)。
(1)在
 时,
时, 在足量的氧气中充分燃烧生成二氧化硫,放出
在足量的氧气中充分燃烧生成二氧化硫,放出 的热量,则表示S的燃烧热的热化学方程式为
的热量,则表示S的燃烧热的热化学方程式为(2)现有反应:
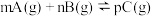 ,达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
,达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:①该反应的逆反应为

②减压时,A的质量分数
③若加入B(体积不变),则A的转化率
④若升高温度,则平衡时B、C的浓度之比
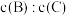 将
将⑤若加入催化剂,平衡时气体混合物的总物质的量
⑥若B是有色物质,A、C均无色,则加入C(体积不变)后混合物颜色
(3)已知相同条件下
反应I:

反应Ⅱ:

则反应

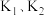 表示)。
表示)。
您最近一年使用:0次
名校
4 . 下列图示与对应叙述相符的是
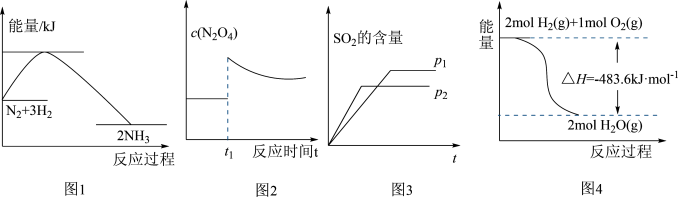

| A.图1反应达平衡后,升高温度,平衡常数K值增大 |
B.图2表示平衡 在t1时迅速将体积缩小后c(N2O4)的变化 在t1时迅速将体积缩小后c(N2O4)的变化 |
C.图3表示可逆反应“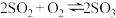 ”中SO2的含量与压强的关系,且P2>P1 ”中SO2的含量与压强的关系,且P2>P1 |
D.图4表示H2与O2发生反应过程中的能量变化,则H2的燃烧热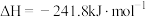 |
您最近一年使用:0次
名校
5 . 恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。[已知:2SO2(g)+O2(g) 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
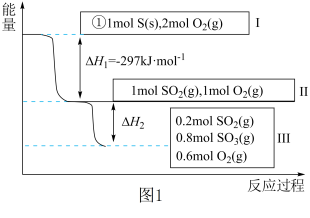
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:___________ 。
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|___________ (填“大”、“小”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是___________ ;图中表示平衡混合物中SO3的含量最高的一段时间是___________ 。

 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
| A.升高温度 | B.充入He | C.再充入1mol SO2(g)和1mol O2(g) | D.使用催化剂 |
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是

您最近一年使用:0次
6 . 2020年东京奥运会火炬传递的火炬样式将采用樱花形状。奥运会火炬常用的燃料为丙烷、丁烷等。
已知:丙烷的燃烧热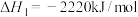 ;正丁烷的燃烧热
;正丁烷的燃烧热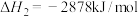 ,异丁烷的燃烧热
,异丁烷的燃烧热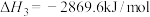 。
。
(1)写出丙烷燃烧热的热化学方程式:_______ 。
(2)下列有关说法不正确的是_______ (填标号)。
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷的多
C.正丁烷比异丁烷稳定
(3)已知A气体的燃烧热为30kJ/mol,B气体的燃烧热为500kJ/mol。现有6mol由A和B组成的混合气体,完全燃烧放出的热量是2000kJ,则该混合气体中气体A和气体B的物质的量之比是_______ 。
(4)Deacon直接氧化法可按下列催化过程进行:
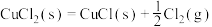
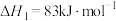
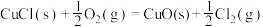


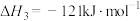
则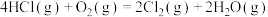 的
的
_______  。
。
(5)恒温恒容条件下,将2mol A气体和2mol B气体通入体积为2L的密闭容器中发生如下反应: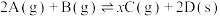 ,2min时反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为
,2min时反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为 。
。
①从开始反应至达到平衡状态,生成C的平均反应速率为_______ 。
②
_______ 。
③下列各项可作为该反应达到平衡状态的标志的是_______ (填字母)。
A.压强不再变化 B.气体密度不再变化
C.A的消耗速率与B的消耗速率之比为2∶1 D.A的百分含量保持不变
已知:丙烷的燃烧热
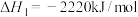 ;正丁烷的燃烧热
;正丁烷的燃烧热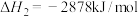 ,异丁烷的燃烧热
,异丁烷的燃烧热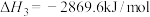 。
。(1)写出丙烷燃烧热的热化学方程式:
(2)下列有关说法不正确的是
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷的多
C.正丁烷比异丁烷稳定
(3)已知A气体的燃烧热为30kJ/mol,B气体的燃烧热为500kJ/mol。现有6mol由A和B组成的混合气体,完全燃烧放出的热量是2000kJ,则该混合气体中气体A和气体B的物质的量之比是
(4)Deacon直接氧化法可按下列催化过程进行:
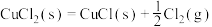
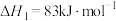
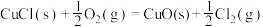


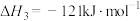
则
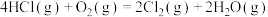 的
的
 。
。(5)恒温恒容条件下,将2mol A气体和2mol B气体通入体积为2L的密闭容器中发生如下反应:
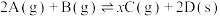 ,2min时反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为
,2min时反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为 。
。①从开始反应至达到平衡状态,生成C的平均反应速率为
②

③下列各项可作为该反应达到平衡状态的标志的是
A.压强不再变化 B.气体密度不再变化
C.A的消耗速率与B的消耗速率之比为2∶1 D.A的百分含量保持不变
您最近一年使用:0次
10-11高二下·安徽马鞍山·期中
名校
解题方法
7 . 一些烷烃的燃烧热如下表:
下列说法正确的是
| 化合物 | ΔH/(kJ·mol-1) | 化合物 | ΔH/(kJ·mol-1) |
| 甲烷 | -891.0 | 正丁烷 | -2878.0 |
| 乙烷 | -1560.8 | 异丁烷 | -2869.6 |
| 丙烷 | -2221.5 | 2-甲基丁烷 | -3531.3 |
| A.正戊烷的燃烧热大约是3540 kJ·mol-1 |
| B.热稳定性:正丁烷>异丁烷 |
| C.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g) ΔH=-1560.8 kJ·mol-1 |
| D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
您最近一年使用:0次
2021-08-27更新
|
573次组卷
|
17卷引用:2010-2011学年安徽省马鞍山市第二中学高二下学期期中素质测试化学试卷
(已下线)2010-2011学年安徽省马鞍山市第二中学高二下学期期中素质测试化学试卷(已下线)2010—2011学年安徽省马鞍山二中高二下学期期中考试化学试卷(理科)江西省上饶市玉山县第一中学2015-2016学年高二下学期重点班第一次月考化学卷(已下线)2018年10月16日 《每日一题》人教选修4-燃烧热及表示燃烧热的热化学方程式(已下线)考点08 化学反应中的热效应——备战2019年浙江新高考化学考点步步为赢 高二化学暑假作业:作业七 化学反应与能量黑龙江省牡丹江市第一高级中学2019-2020学年高二上学期开学检测化学试题浙江省杭州市西湖高级中学2019-2020学年高二10月月考化学试题(已下线)考点08 化学反应中的能量变化——《备战2020年高考精选考点专项突破题集》宁夏银川一中2020-2021学年高二上学期期末考试化学试题河南省洛阳市豫西名校2020-2021学年高二下学期第一次联考化学试题第23届(2009年)全国高中学生化学竞赛(安徽赛区)初赛试题(已下线)1.1.3 能源的充分利用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1) 福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题(已下线)必考点01 化学反应的热效应-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)河南省信阳市2021-2022学年高二上学期期中考试化学试题湖北省部分重点中学2022-2023学年高三下学期2月质量检测化学试题
名校
解题方法
8 . 为减小和消除过量 和
和 对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对
对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对 和
和 创新利用的研究。
创新利用的研究。
(1)25℃、101KPa条件下充分燃烧一定量的丁烷气体放出热量为 ,经测定,将生成的
,经测定,将生成的 通入足量澄清石灰水中产生40g白色沉淀,写出表示丁烷燃烧热的热化学方程式
通入足量澄清石灰水中产生40g白色沉淀,写出表示丁烷燃烧热的热化学方程式_______ 。
(2)用 催化还原
催化还原 还可以消除氮氧化物的污染。例如:
还可以消除氮氧化物的污染。例如:
 ;
;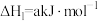
 ;
;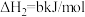
若用1mol 还原
还原 至
至 ,则该反应过程中的反应热
,则该反应过程中的反应热
___ 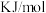 (用含a、b的式子表示)
(用含a、b的式子表示)
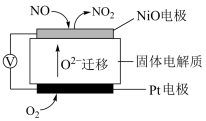
(3)通过 传感器可监测
传感器可监测 的含量,其工作原理示意图为:
的含量,其工作原理示意图为: 电极上发生的是
电极上发生的是_______ (填“氧化”或“还原”)反应。写出 电极的电极反应式
电极的电极反应式_______ 。
 和
和 对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对
对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对 和
和 创新利用的研究。
创新利用的研究。(1)25℃、101KPa条件下充分燃烧一定量的丁烷气体放出热量为
 ,经测定,将生成的
,经测定,将生成的 通入足量澄清石灰水中产生40g白色沉淀,写出表示丁烷燃烧热的热化学方程式
通入足量澄清石灰水中产生40g白色沉淀,写出表示丁烷燃烧热的热化学方程式(2)用
 催化还原
催化还原 还可以消除氮氧化物的污染。例如:
还可以消除氮氧化物的污染。例如: ;
;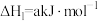
 ;
;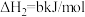
若用1mol
 还原
还原 至
至 ,则该反应过程中的反应热
,则该反应过程中的反应热
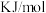 (用含a、b的式子表示)
(用含a、b的式子表示)(3)通过
 传感器可监测
传感器可监测 的含量,其工作原理示意图为:
的含量,其工作原理示意图为: 电极上发生的是
电极上发生的是 电极的电极反应式
电极的电极反应式
您最近一年使用:0次
解题方法
9 . 随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
(1)把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)=CO2(g) △H1<0 ①
途径II:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) △H2>0 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g) △H3<0 ③
2H2(g)+O2(g)=2H2O(g) △H4<0 ④
则途径I放出的热量_______ (填“大于”“等于”或“小于”)途径II放出的热量;△H1、△H2、△H3、△H4的数学关系式是_______ 。
(2)在25℃、101kPa下,1克甲醇完全燃料放热22.68kJ,写出甲醇燃烧热的热化学方程式_______ 。
(3)已知①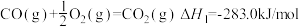
②H2(g)+ O2(g)=H2O(l) ΔH2=-285.8kJ/mol
O2(g)=H2O(l) ΔH2=-285.8kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH3=-1370kJ/mol
试计算④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的ΔH=_______ 。
(1)把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)=CO2(g) △H1<0 ①
途径II:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) △H2>0 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g) △H3<0 ③
2H2(g)+O2(g)=2H2O(g) △H4<0 ④
则途径I放出的热量
(2)在25℃、101kPa下,1克甲醇完全燃料放热22.68kJ,写出甲醇燃烧热的热化学方程式
(3)已知①
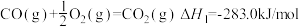
②H2(g)+
 O2(g)=H2O(l) ΔH2=-285.8kJ/mol
O2(g)=H2O(l) ΔH2=-285.8kJ/mol③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH3=-1370kJ/mol
试计算④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的ΔH=
您最近一年使用:0次
名校
解题方法
10 . 下列热化学方程式正确的是
A.理论上1 kg黄铁矿(FeS2的含量为84%)完全燃烧放出的热量5950 kJ,则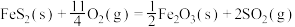 △H=-850 kJ/mol △H=-850 kJ/mol |
B.500℃、30 MPa下,将0.5 molN2(g)和1.5 molH2(g)置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为 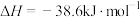 |
| C.稀盐酸和NaOH溶液反应的中和热△H=-57.3 kJ/mol,则稀H2SO4和Ba(OH)2溶液反应的中和热为2×57.3 kJ/mol |
D.甲烷的燃烧热△H=-890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为: 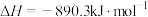 |
您最近一年使用:0次



