名校
解题方法
1 . Ⅰ.已知:
①
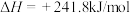
②
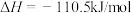
③

请填写下列空白。
(1)上述反应中属于吸热反应的是_______ (填序号)。
(2)
 完全燃烧生成水蒸气,放出的热量为
完全燃烧生成水蒸气,放出的热量为_______ 。
Ⅱ.由于亚硝酸钠和食盐性状相似,曾多次发生过将 误当食盐食用的事件。欲测定某样品中
误当食盐食用的事件。欲测定某样品中 的含量,某同学设计如下实验:①称取样品
的含量,某同学设计如下实验:①称取样品 ,加水溶解,配制成
,加水溶解,配制成 溶液。②取
溶液。②取 溶液于锥形瓶中,用
溶液于锥形瓶中,用
 标准溶液(酸性)进行滴定,滴定结束后消耗
标准溶液(酸性)进行滴定,滴定结束后消耗 溶液
溶液 。
。
(3)上述实验①所需玻璃仪器除烧杯、玻璃棒、胶头滴管之外还有_______ 。
(4)在进行滴定操作时, 溶液盛装在
溶液盛装在_______ (填“酸式”或“碱式”)滴定管中。当滴入最后半滴 溶液,
溶液,_______ 时达到滴定终点。
(5)滴定过程中发生反应的离子方程式是_______ ;测得该样品中 的质量分数为
的质量分数为_______ 。
(6)以下操作造成测定结果偏高的是_______ 。
A.滴定管未用 标准溶液润洗
标准溶液润洗
B.锥形瓶未用待测液润洗
C.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失
D.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后俯视读数
E.若滴定过程中刚出现颜色变化就停止滴定
①

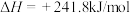
②

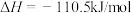
③


请填写下列空白。
(1)上述反应中属于吸热反应的是
(2)

 完全燃烧生成水蒸气,放出的热量为
完全燃烧生成水蒸气,放出的热量为Ⅱ.由于亚硝酸钠和食盐性状相似,曾多次发生过将
 误当食盐食用的事件。欲测定某样品中
误当食盐食用的事件。欲测定某样品中 的含量,某同学设计如下实验:①称取样品
的含量,某同学设计如下实验:①称取样品 ,加水溶解,配制成
,加水溶解,配制成 溶液。②取
溶液。②取 溶液于锥形瓶中,用
溶液于锥形瓶中,用
 标准溶液(酸性)进行滴定,滴定结束后消耗
标准溶液(酸性)进行滴定,滴定结束后消耗 溶液
溶液 。
。(3)上述实验①所需玻璃仪器除烧杯、玻璃棒、胶头滴管之外还有
(4)在进行滴定操作时,
 溶液盛装在
溶液盛装在 溶液,
溶液,(5)滴定过程中发生反应的离子方程式是
 的质量分数为
的质量分数为(6)以下操作造成测定结果偏高的是
A.滴定管未用
 标准溶液润洗
标准溶液润洗B.锥形瓶未用待测液润洗
C.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失
D.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后俯视读数
E.若滴定过程中刚出现颜色变化就停止滴定
您最近半年使用:0次
名校
解题方法
2 . 一些烷烃的燃烧热如下表:
下列表达正确的是
| 化合物 | 燃烧热 |
| 甲烷 | 891.0 |
| 乙烷 | 1560.8 |
| 丙烷 | 2221.5 |
| 正丁烷 | 2878.0 |
| 异丁烷 | 2869.6 |
| 2-甲基丁烷 | 3531.3 |
A.正戊烷的燃烧热大于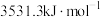 |
| B.稳定性:正丁烷>异丁烷 |
C.乙烷燃烧的热化学方程式为 |
| D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
您最近半年使用:0次
名校
3 . 完成下列问题。
(1)在 时,
时, 在足量的氧气中充分燃烧生成二氧化硫,放出
在足量的氧气中充分燃烧生成二氧化硫,放出 的热量,则表示S的燃烧热的热化学方程式为
的热量,则表示S的燃烧热的热化学方程式为___________ 。
(2)现有反应: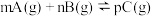 ,达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
,达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
①该反应的逆反应为___________ 热反应,且
___________ p(填“>”、“=”或“<”)。
②减压时,A的质量分数___________ 。(填“增大”、“减小”或“不变”,下同)
③若加入B(体积不变),则A的转化率___________ 。
④若升高温度,则平衡时B、C的浓度之比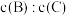 将
将___________ 。
⑤若加入催化剂,平衡时气体混合物的总物质的量___________ 。
⑥若B是有色物质,A、C均无色,则加入C(体积不变)后混合物颜色___________ ;(填“变深”、“变浅”或“不变”,下同)维持容器内压强不变,充入氖气后,混合物颜色___________ 。
(3)已知相同条件下
反应I:
反应Ⅱ:
则反应
___________ 。(用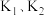 表示)。
表示)。
(1)在
 时,
时, 在足量的氧气中充分燃烧生成二氧化硫,放出
在足量的氧气中充分燃烧生成二氧化硫,放出 的热量,则表示S的燃烧热的热化学方程式为
的热量,则表示S的燃烧热的热化学方程式为(2)现有反应:
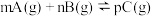 ,达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
,达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:①该反应的逆反应为

②减压时,A的质量分数
③若加入B(体积不变),则A的转化率
④若升高温度,则平衡时B、C的浓度之比
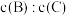 将
将⑤若加入催化剂,平衡时气体混合物的总物质的量
⑥若B是有色物质,A、C均无色,则加入C(体积不变)后混合物颜色
(3)已知相同条件下
反应I:

反应Ⅱ:

则反应

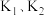 表示)。
表示)。
您最近半年使用:0次
名校
4 . 过氧乙酸(CH3CO3H)是一种广谱高效消毒剂,不稳定、易分解,高浓度易爆炸。常用于空气、器材的消毒,可由乙酸与H2O2在硫酸催化下反应制得,热化学方程式为:CH3COOH(aq)+H2O2(aq) CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
(1)利用上述反应制备760g CHCOH,放出的热量为_______ kJ。
(2)取质量相等的冰醋酸和50% H2O2溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在25℃下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应(反应均未达到平衡),测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
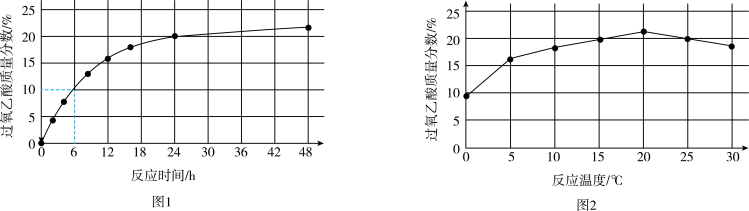 ①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=
①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=_____ g/h。(用含m的代数式表示)
②综合图1、图2分析,与20℃相比,25℃时过氧乙酸产率降低的可能原因是_______ (写出2条)。
(3)SV-1、SV-2是两种常用于实验研究的病毒,粒径分别为40nm和70nm。病毒在水中可能会聚集成团簇。不同pH下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
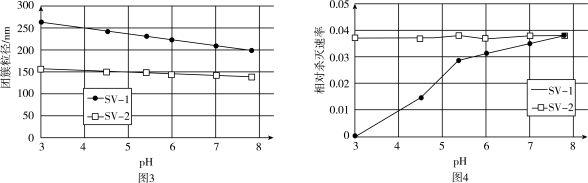
依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是___________ 。
 CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol(1)利用上述反应制备760g CHCOH,放出的热量为
(2)取质量相等的冰醋酸和50% H2O2溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在25℃下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应(反应均未达到平衡),测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
 ①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=
①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=②综合图1、图2分析,与20℃相比,25℃时过氧乙酸产率降低的可能原因是
(3)SV-1、SV-2是两种常用于实验研究的病毒,粒径分别为40nm和70nm。病毒在水中可能会聚集成团簇。不同pH下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。

依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是
您最近半年使用:0次
5 . Ⅰ.燃料电池电动汽车是利用氢气、甲醇、天然气(主要成分为甲烷)、汽油等燃料和空气中的氧在催化剂的作用下在燃料电池中经电化学反应产生的电能,并作为主要动力源驱动的汽车。
(1)汽车行驶的过程中,能量的转化形式为_______ 。
Ⅱ.利用下表数据回答下列问题:
(2)表示乙烷燃烧热的热化学方程式为_______ 。
(3)稳定性:正丁烷_______ 异丁烷(填“>”“<”或“=”);原因_______ 。
(4)相同质量的燃料,_______ (填“C”或“H”)的质量分数越大,燃烧放出的热量越多。
(5)二氧化碳是重要的温室气体,从环保角度分析,放出相同的热量时选择_______ (填“乙烷”或“甲醇”)作为燃料产生的CO2较少。
(6)现有氢气和丙烷混合气体3 mol,完全燃烧共产生2791.5 kJ的热量,则氢气和丙烷的物质的量之比为_______ 。
(1)汽车行驶的过程中,能量的转化形式为
Ⅱ.利用下表数据回答下列问题:
| 燃料 | 燃烧热/(kJ·mol-1) | 燃料 | 燃烧热/(kJ·mol-1) |
| 氢气 | 285.8 | 甲醇(CH3OH) | 726.51 |
| 甲烷(CH4) | 890.3 | 正丁烷(CH3CH2CH2CH3) | 2878.0 |
| 乙烷(C2H6) | 1559.8 | 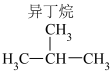 | 2869.6 |
| 丙烷(C3H8) | 2219.9 |
(3)稳定性:正丁烷
(4)相同质量的燃料,
(5)二氧化碳是重要的温室气体,从环保角度分析,放出相同的热量时选择
(6)现有氢气和丙烷混合气体3 mol,完全燃烧共产生2791.5 kJ的热量,则氢气和丙烷的物质的量之比为
您最近半年使用:0次
名校
解题方法
6 . 我国含硫天然气资源丰富,甲烷与硫化氢重整制氢和天然气脱硫具有重要的现实意义。甲烷与硫化氢重整制氢反应为 ,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为:
,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为: 在
在_____ 下可自发进行。
A.高温 B.低温
在恒压条件下,起始时按 (同时通入一定量的
(同时通入一定量的 进行稀释,
进行稀释, 不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中
不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中 、
、 、
、 、
、 的物质的量分数
的物质的量分数 的影响如图所示:
的影响如图所示: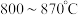 温度区间内,随温度升高,
温度区间内,随温度升高, 在平衡时反应混合物中含量迅速下降,而
在平衡时反应混合物中含量迅速下降,而 的含量几乎为0,根据图2分析其可能的原因是
的含量几乎为0,根据图2分析其可能的原因是_____ 。
(3)已知每1克 燃烧放热
燃烧放热 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_____ 。
 ,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为:
,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为: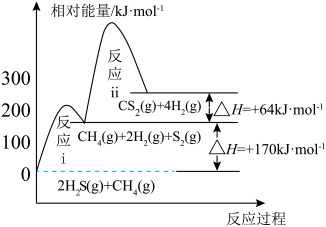
 在
在A.高温 B.低温
在恒压条件下,起始时按
 (同时通入一定量的
(同时通入一定量的 进行稀释,
进行稀释, 不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中
不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中 、
、 、
、 、
、 的物质的量分数
的物质的量分数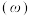 的影响如图所示:
的影响如图所示:
 温度区间内,随温度升高,
温度区间内,随温度升高, 在平衡时反应混合物中含量迅速下降,而
在平衡时反应混合物中含量迅速下降,而 的含量几乎为0,根据图2分析其可能的原因是
的含量几乎为0,根据图2分析其可能的原因是(3)已知每1克
 燃烧放热
燃烧放热 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为
您最近半年使用:0次
名校
7 . 恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。[已知:2SO2(g)+O2(g) 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
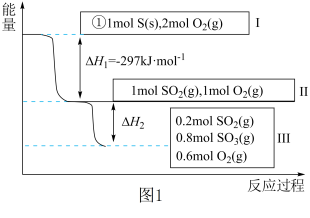
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:___________ 。
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|___________ (填“大”、“小”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是___________ ;图中表示平衡混合物中SO3的含量最高的一段时间是___________ 。

 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
| A.升高温度 | B.充入He | C.再充入1mol SO2(g)和1mol O2(g) | D.使用催化剂 |
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是

您最近半年使用:0次
名校
8 . 已知X、Y、Z、W、R、M为原子序数依次增大的元素,其中X、Y、Z、W、R为短周期主族元素,且位于三个不同周期,Y的某种核素可用于测定文物的年代,W的最外层电子数是最内层的3倍,W与R同主族,元素M是地壳中含量排名第二的金属元素。回答下列问题:
(1)写出 的电子式:
的电子式:_____ 。
(2)W的简单氢化物的熔沸点比R的高,原因是_____ 。
(3)Y、Z、R的最高价氧化物对应水化物的酸性最弱的是_____ (填化学式)。
X、Y、Z、R组成的某种酸的水溶液可用于检测溶液中的 ,该酸的化学式为
,该酸的化学式为_____ 。
(4)X、Y、W组成的某种常见物质常用于制作消毒剂,该物质的燃烧热为1366.8 ,写出该物质燃烧的热化学方程式:
,写出该物质燃烧的热化学方程式:_____ 。
(5) 与
与 的反应是可逆反应,该反应的平衡常数的表达式为
的反应是可逆反应,该反应的平衡常数的表达式为_____ ;增加 的量,
的量, 的平衡转化率如何变化?
的平衡转化率如何变化?_____ 。
(1)写出
 的电子式:
的电子式:(2)W的简单氢化物的熔沸点比R的高,原因是
(3)Y、Z、R的最高价氧化物对应水化物的酸性最弱的是
X、Y、Z、R组成的某种酸的水溶液可用于检测溶液中的
 ,该酸的化学式为
,该酸的化学式为(4)X、Y、W组成的某种常见物质常用于制作消毒剂,该物质的燃烧热为1366.8
 ,写出该物质燃烧的热化学方程式:
,写出该物质燃烧的热化学方程式:(5)
 与
与 的反应是可逆反应,该反应的平衡常数的表达式为
的反应是可逆反应,该反应的平衡常数的表达式为 的量,
的量, 的平衡转化率如何变化?
的平衡转化率如何变化?
您最近半年使用:0次
名校
解题方法
9 . 甲醇是一种可再生能源,用途广泛。请回答下列问题:
(1)一种用CO2生产甲醇燃料的反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-akJ•mol-1。
已知:CH3OH(g)=CH3OH(l) ΔH=-bkJ•mol-1;
2H2(g)+O2(g)=2H2O(g) ΔH=-ckJ•mol-1;
H2O(g)=H2O(l) ΔH=-dkJ•mol-1。
则表示CH3OH(l)摩尔燃烧焓的热化学方程式为________ 。
(2)用如图所示装置研究有关电化学问题,当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:
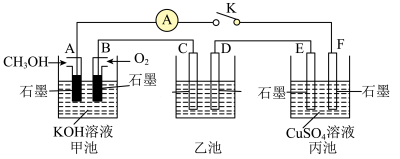
①A电极的电极反应式为________ ,C电极的电势________ (填“低于”或“高于”)D电极的电势。
②若在乙池中实现铁表面镀银,则D电极材料为________ ,乙池中的溶液为________ 。
③丙池中装有200mL1mol•L-1硫酸铜溶液,若B电极消耗3.36L(标准状况)气体,若要使电解质溶液恢复到电解前的状态,应加入________ (填字母)。
A.CuO B.Cu(OH)2 C.CuCO3 D.Cu2(OH)2CO3
(3)某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。

根据图像分析,与汽油相比,甲醇作为燃料的优点是________ 。
(1)一种用CO2生产甲醇燃料的反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-akJ•mol-1。
已知:CH3OH(g)=CH3OH(l) ΔH=-bkJ•mol-1;
2H2(g)+O2(g)=2H2O(g) ΔH=-ckJ•mol-1;
H2O(g)=H2O(l) ΔH=-dkJ•mol-1。
则表示CH3OH(l)摩尔燃烧焓的热化学方程式为
(2)用如图所示装置研究有关电化学问题,当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:

①A电极的电极反应式为
②若在乙池中实现铁表面镀银,则D电极材料为
③丙池中装有200mL1mol•L-1硫酸铜溶液,若B电极消耗3.36L(标准状况)气体,若要使电解质溶液恢复到电解前的状态,应加入
A.CuO B.Cu(OH)2 C.CuCO3 D.Cu2(OH)2CO3
(3)某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。

根据图像分析,与汽油相比,甲醇作为燃料的优点是
您最近半年使用:0次
名校
10 . 下列化学反应表示正确的是
A.BeO与NaOH溶液反应: |
B.镁的燃烧热为610kJ/mol,镁的燃烧: ; ; |
C.向Mg(HCO3)2溶液中滴加足量NaOH溶液: |
D.用酸性KMnO4测定CaC2O4的含量: |
您最近半年使用:0次



