名校
1 . 链状葡萄糖分子中的醛基可与分子内羟基发生加成反应形成两种六元环状结构。常温下,各种葡萄糖结构及其所占百分含量如下图所示。已知各种葡萄糖结构中链状结构的熵最大,两种环状结构的熵相近。下列说法正确的是

A. |
B.三种结构中,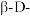 吡喃葡萄糖的焓最小 吡喃葡萄糖的焓最小 |
| C.葡萄糖由链状转化为环状结构是醛基和6号碳原子上羟基作用的结果 |
D.18g葡萄糖完全燃烧生成 和 和 放热akJ,故葡萄糖的燃烧热为10akJ/mol 放热akJ,故葡萄糖的燃烧热为10akJ/mol |
您最近一年使用:0次
名校
解题方法
2 . 我国含硫天然气资源丰富,甲烷与硫化氢重整制氢和天然气脱硫具有重要的现实意义。甲烷与硫化氢重整制氢反应为 ,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为:
,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为: 在
在_____ 下可自发进行。
A.高温 B.低温
在恒压条件下,起始时按 (同时通入一定量的
(同时通入一定量的 进行稀释,
进行稀释, 不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中
不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中 、
、 、
、 、
、 的物质的量分数
的物质的量分数 的影响如图所示:
的影响如图所示: 温度区间内,随温度升高,
温度区间内,随温度升高, 在平衡时反应混合物中含量迅速下降,而
在平衡时反应混合物中含量迅速下降,而 的含量几乎为0,根据图2分析其可能的原因是
的含量几乎为0,根据图2分析其可能的原因是_____ 。
(3)已知每1克 燃烧放热
燃烧放热 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_____ 。
 ,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为:
,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为: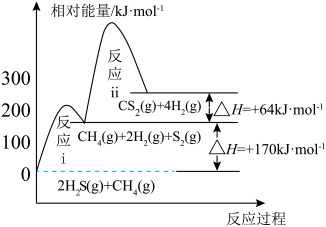
 在
在A.高温 B.低温
在恒压条件下,起始时按
 (同时通入一定量的
(同时通入一定量的 进行稀释,
进行稀释, 不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中
不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中 、
、 、
、 、
、 的物质的量分数
的物质的量分数 的影响如图所示:
的影响如图所示: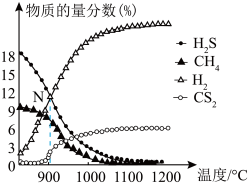
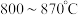 温度区间内,随温度升高,
温度区间内,随温度升高, 在平衡时反应混合物中含量迅速下降,而
在平衡时反应混合物中含量迅速下降,而 的含量几乎为0,根据图2分析其可能的原因是
的含量几乎为0,根据图2分析其可能的原因是(3)已知每1克
 燃烧放热
燃烧放热 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为
您最近一年使用:0次
名校
3 . 下列化学反应表示正确的是
A.BeO与NaOH溶液反应: |
B.镁的燃烧热为610kJ/mol,镁的燃烧: ; ; |
C.向Mg(HCO3)2溶液中滴加足量NaOH溶液: |
D.用酸性KMnO4测定CaC2O4的含量: |
您最近一年使用:0次
名校
4 . 周期表中ⅡA族元素及其化合物应用广泛。铍的化合物性质与铝相似, 的熔点为
的熔点为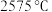 ,熔融时
,熔融时 能导电,而
能导电,而 不能导电;
不能导电; 的燃烧热为
的燃烧热为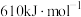 ,实验室中常用酸性
,实验室中常用酸性 测定物品中不溶性
测定物品中不溶性 的含量。铍镍合金可用于制造弹簧秤的弹簧,
的含量。铍镍合金可用于制造弹簧秤的弹簧, 可用作隔音材料,
可用作隔音材料, 可用作工业废气脱硫剂。下列化学反应表示正确的是
可用作工业废气脱硫剂。下列化学反应表示正确的是
 的熔点为
的熔点为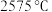 ,熔融时
,熔融时 能导电,而
能导电,而 不能导电;
不能导电; 的燃烧热为
的燃烧热为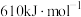 ,实验室中常用酸性
,实验室中常用酸性 测定物品中不溶性
测定物品中不溶性 的含量。铍镍合金可用于制造弹簧秤的弹簧,
的含量。铍镍合金可用于制造弹簧秤的弹簧, 可用作隔音材料,
可用作隔音材料, 可用作工业废气脱硫剂。下列化学反应表示正确的是
可用作工业废气脱硫剂。下列化学反应表示正确的是A. 与 与 溶液反应: 溶液反应: |
B.镁的燃烧:  |
C.向 溶液中滴加足量 溶液中滴加足量 溶液: 溶液: |
D.用酸性 测定 测定 的含量: 的含量: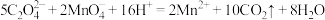 |
您最近一年使用:0次
2024-01-28更新
|
605次组卷
|
3卷引用:2024届江苏省连云港市高三第一次调研考试(一模)化学试题
2024届江苏省连云港市高三第一次调研考试(一模)化学试题河南省焦作市博爱县第一中学2023-2024学年高三下学期开学化学试题(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
10-11高二下·安徽马鞍山·期中
名校
解题方法
5 . 一些烷烃的燃烧热如下表:
下列说法正确的是
| 化合物 | ΔH/(kJ·mol-1) | 化合物 | ΔH/(kJ·mol-1) |
| 甲烷 | -891.0 | 正丁烷 | -2878.0 |
| 乙烷 | -1560.8 | 异丁烷 | -2869.6 |
| 丙烷 | -2221.5 | 2-甲基丁烷 | -3531.3 |
| A.正戊烷的燃烧热大约是3540 kJ·mol-1 |
| B.热稳定性:正丁烷>异丁烷 |
| C.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g) ΔH=-1560.8 kJ·mol-1 |
| D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
您最近一年使用:0次
2021-08-27更新
|
574次组卷
|
17卷引用:2010-2011学年安徽省马鞍山市第二中学高二下学期期中素质测试化学试卷
(已下线)2010-2011学年安徽省马鞍山市第二中学高二下学期期中素质测试化学试卷(已下线)2010—2011学年安徽省马鞍山二中高二下学期期中考试化学试卷(理科)江西省上饶市玉山县第一中学2015-2016学年高二下学期重点班第一次月考化学卷(已下线)2018年10月16日 《每日一题》人教选修4-燃烧热及表示燃烧热的热化学方程式(已下线)考点08 化学反应中的热效应——备战2019年浙江新高考化学考点步步为赢 高二化学暑假作业:作业七 化学反应与能量黑龙江省牡丹江市第一高级中学2019-2020学年高二上学期开学检测化学试题浙江省杭州市西湖高级中学2019-2020学年高二10月月考化学试题(已下线)考点08 化学反应中的能量变化——《备战2020年高考精选考点专项突破题集》宁夏银川一中2020-2021学年高二上学期期末考试化学试题河南省洛阳市豫西名校2020-2021学年高二下学期第一次联考化学试题第23届(2009年)全国高中学生化学竞赛(安徽赛区)初赛试题(已下线)1.1.3 能源的充分利用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1) 福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题(已下线)必考点01 化学反应的热效应-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)河南省信阳市2021-2022学年高二上学期期中考试化学试题湖北省部分重点中学2022-2023学年高三下学期2月质量检测化学试题
6 . 苯乙烯是一种重要的有机化工原料,可广泛用于合成橡胶,工程塑料及制药等。工业上可通过乙苯催化脱氢来制取苯乙烯,反应方程式如下:
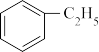 (g)
(g)
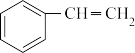 (g)+H2(g) ΔH
(g)+H2(g) ΔH
(1)已知部分物质的燃烧热数据如下表:
则
_______ 。
(2)下列关于反应的说法正确的是_______(填序号)
(3)工业装置通常采用铁基氧化物催化剂,通入过热水蒸气(615~645℃)、水油比(水与乙苯质量比)1.4~1.8、常压的条件下发生乙苯的催化脱氢反应。
①反应中通入水蒸气的作用是_______ 。
②将物质的量分数组成为m%乙苯(g)、n% 的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为
的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为 ,则苯乙烯的分压为
,则苯乙烯的分压为_______ ,平衡常数
_______ (以分压表示,分压=总压×物质的量分数)
(4)近年来,有研究者发现若将上述生产过程中通入 改为通入
改为通入 ,通入
,通入 后会发生反应
后会发生反应 。在常压下,分别按投料比为仅乙苯,乙苯
。在常压下,分别按投料比为仅乙苯,乙苯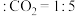 ,乙苯
,乙苯 ,测得乙苯的平衡转化率与温度的关系如下图。
,测得乙苯的平衡转化率与温度的关系如下图。
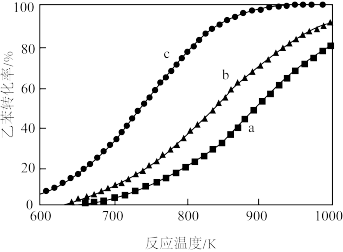
则乙苯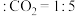 对应的曲线为
对应的曲线为_______ (填“a”,“b”或“c”),理由是_______ 。
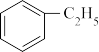 (g)
(g)
 (g)+H2(g) ΔH
(g)+H2(g) ΔH(1)已知部分物质的燃烧热数据如下表:
| 物质 | 乙苯 | 苯乙烯 | 氢气 |
燃烧热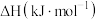 | -4610.2 | -4441.8 | -285.8 |

(2)下列关于反应的说法正确的是_______(填序号)
| A.高温有利于反应自发进行 |
| B.工业生产中应尽可能提高反应温度,并增大压强,以提高原料的利用率 |
| C.恒温恒容条件下,反应达到平衡后,向体系中再充入乙苯蒸气,乙苯的转化率将增大 |
| D.选择合适的催化剂可以缩短达到平衡的时间,但不会提高生成物中苯乙烯的含量 |
①反应中通入水蒸气的作用是
②将物质的量分数组成为m%乙苯(g)、n%
 的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为
的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为 ,则苯乙烯的分压为
,则苯乙烯的分压为
(4)近年来,有研究者发现若将上述生产过程中通入
 改为通入
改为通入 ,通入
,通入 后会发生反应
后会发生反应 。在常压下,分别按投料比为仅乙苯,乙苯
。在常压下,分别按投料比为仅乙苯,乙苯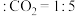 ,乙苯
,乙苯 ,测得乙苯的平衡转化率与温度的关系如下图。
,测得乙苯的平衡转化率与温度的关系如下图。
则乙苯
 对应的曲线为
对应的曲线为
您最近一年使用:0次
解题方法
7 . 化学物质在汽车的动力、安全等方面有着极为重要的作用。
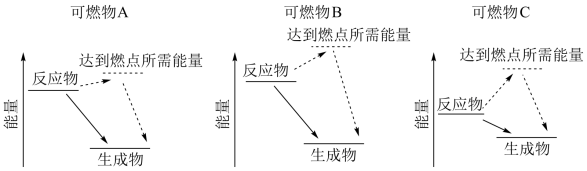
(1)某同学根据所查阅的资料,绘制了三种可燃物在空气中发生燃烧反应的能量变化示意图。根据示意图,你认为可燃物_______ (填“A”、“B”或“C”)更适合用作车用燃料。(已知:燃点是指在规定的条件下,应用外部热源使物质表面起火并持续燃烧一定时间所需的最低温度,燃点较低时存在安全隐患。)
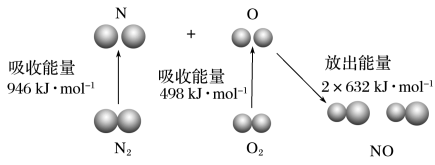
(2)汽车尾气中含有 、
、 等污染物。其中
等污染物。其中 生成过程的能量变化如图,由该图数据计算可得,该反应为
生成过程的能量变化如图,由该图数据计算可得,该反应为_______ (填“吸热”或“放热”)反应。
(3)通过 传感器可监测汽车尾气中
传感器可监测汽车尾气中 的含量,其工作原理如图所示:
的含量,其工作原理如图所示:
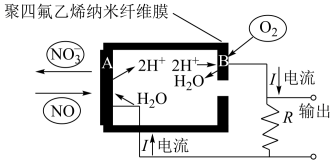
①A电极发生的是_______ 反应(填“氧化”或“还原”)。
②B电极反应为_______ 。
(4)电动汽车普遍使用锂离子电池。某锂离子电池反应为 。
。
①当有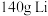 消耗时,电路中转移电子数目为
消耗时,电路中转移电子数目为_______ 。
②根据①的计算思路,分析 做电极优于
做电极优于 的原因是
的原因是_______ 。
(5)安全性是汽车发展需要解决的重要问题。汽车受到强烈撞击时,预置在安全气囊内的化学药剂发生反应产生大量气体,气囊迅速弹出。某种产气药剂主要含有 、
、 、
、 、
、 ,已知
,已知 在猛烈撞击时分解产生两种单质,并放出大量的热。
在猛烈撞击时分解产生两种单质,并放出大量的热。
①药剂中 做冷却剂原因是
做冷却剂原因是_______ 。
②根据产气药剂的组成,在设计气囊中所运用的化学反应时,需要考虑的角度有_______ (填标号)。
A.固体反应物的颜色 B.气体产物的毒性 C.反应的快慢 D.反应的能量变化
(1)某同学根据所查阅的资料,绘制了三种可燃物在空气中发生燃烧反应的能量变化示意图。根据示意图,你认为可燃物

(2)汽车尾气中含有
 、
、 等污染物。其中
等污染物。其中 生成过程的能量变化如图,由该图数据计算可得,该反应为
生成过程的能量变化如图,由该图数据计算可得,该反应为
(3)通过
 传感器可监测汽车尾气中
传感器可监测汽车尾气中 的含量,其工作原理如图所示:
的含量,其工作原理如图所示:
①A电极发生的是
②B电极反应为
(4)电动汽车普遍使用锂离子电池。某锂离子电池反应为
 。
。①当有
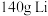 消耗时,电路中转移电子数目为
消耗时,电路中转移电子数目为②根据①的计算思路,分析
 做电极优于
做电极优于 的原因是
的原因是(5)安全性是汽车发展需要解决的重要问题。汽车受到强烈撞击时,预置在安全气囊内的化学药剂发生反应产生大量气体,气囊迅速弹出。某种产气药剂主要含有
 、
、 、
、 、
、 ,已知
,已知 在猛烈撞击时分解产生两种单质,并放出大量的热。
在猛烈撞击时分解产生两种单质,并放出大量的热。①药剂中
 做冷却剂原因是
做冷却剂原因是②根据产气药剂的组成,在设计气囊中所运用的化学反应时,需要考虑的角度有
A.固体反应物的颜色 B.气体产物的毒性 C.反应的快慢 D.反应的能量变化
您最近一年使用:0次
名校
解题方法
8 . 为了合理利用化学能确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得:5g液态甲醇(CH3OH)在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出113.5kJ的热量。试写出甲醇燃烧热的热化学方程式:___ 。
(2)合成甲醇的主要反应是2H2(g)+CO(g) CH3OH(g)ΔH=-90.8kJ·mol-1,t℃时,向2L的密闭容器中投入2molH2和mmolCO,反应10min后测得各组分的浓度如下:
CH3OH(g)ΔH=-90.8kJ·mol-1,t℃时,向2L的密闭容器中投入2molH2和mmolCO,反应10min后测得各组分的浓度如下:
则该时间段内反应速率v(H2)=___ ,m=___ mol。
(3)恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
①若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a=___ mol。
②反应达平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。则平衡时NH3的物质的量为___ ,原混合气体中a:b=___ (写出最简整数比,下同)。
③达到平衡时,N2和H2的转化率之比α(N2):α(H2)=___ 。
(1)实验测得:5g液态甲醇(CH3OH)在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出113.5kJ的热量。试写出甲醇燃烧热的热化学方程式:
(2)合成甲醇的主要反应是2H2(g)+CO(g)
 CH3OH(g)ΔH=-90.8kJ·mol-1,t℃时,向2L的密闭容器中投入2molH2和mmolCO,反应10min后测得各组分的浓度如下:
CH3OH(g)ΔH=-90.8kJ·mol-1,t℃时,向2L的密闭容器中投入2molH2和mmolCO,反应10min后测得各组分的浓度如下:| 物质 | H2 | CO | CH3OH |
| 浓度(mol·L-1) | 0.2 | 0.1 | 0.4 |
(3)恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)
 2NH3(g)
2NH3(g)①若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a=
②反应达平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。则平衡时NH3的物质的量为
③达到平衡时,N2和H2的转化率之比α(N2):α(H2)=
您最近一年使用:0次
18-19高一下·江西南昌·阶段练习
名校
9 . (1)煤燃烧的烟气(主要污染物SO2、NOx),经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g)═NO2(g)+O2(g) △H=-200.9kJ•mol-1
NO(g)+ O2(g)═NO2(g) △H= -58.2kJ•mol-1
O2(g)═NO2(g) △H= -58.2kJ•mol-1
SO2(g)+O3(g)═SO3(g)+O2(g) △H=-241.6kJ•mol-1
(1)反应3NO(g)+O3(g)═3NO2(g)的△H=_______
(2)在标准状况下的11.2L甲烷完全燃烧生成 和液态水放出444.8 kJ•mol-1热量,能表示其燃烧热的热化学方程式的是
和液态水放出444.8 kJ•mol-1热量,能表示其燃烧热的热化学方程式的是____________
(3)中和热的测定是高中重要的定量实验,取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸溶液50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:

①从如图实验装置看,其中尚缺少的一种玻璃用品是______ ,除此之外,装置中的一个明显错误是______
②若0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热△H=______ (取小数点后一位)。
NO(g)+O3(g)═NO2(g)+O2(g) △H=-200.9kJ•mol-1
NO(g)+
 O2(g)═NO2(g) △H= -58.2kJ•mol-1
O2(g)═NO2(g) △H= -58.2kJ•mol-1SO2(g)+O3(g)═SO3(g)+O2(g) △H=-241.6kJ•mol-1
(1)反应3NO(g)+O3(g)═3NO2(g)的△H=
(2)在标准状况下的11.2L甲烷完全燃烧生成
 和液态水放出444.8 kJ•mol-1热量,能表示其燃烧热的热化学方程式的是
和液态水放出444.8 kJ•mol-1热量,能表示其燃烧热的热化学方程式的是(3)中和热的测定是高中重要的定量实验,取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸溶液50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:

①从如图实验装置看,其中尚缺少的一种玻璃用品是
②若0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热△H=
| 项目 | 反应起始温度T1(℃) | 终止温度T2(℃) | T2-T1 | ||
| HCl | NaOH | 平均温度 | |||
| 第1次 | 26.2 | 26.0 | 29.4 | ||
| 第2次 | 27.0 | 27.4 | 32.2 | ||
| 第3次 | 25.9 | 25.9 | 29.1 | ||
| 第4次 | 26.4 | 26.2 | 29.7 | ||
您最近一年使用:0次
10 . 为减少交通事故,新交规明令禁止酒后驾车并对酒后驾车行为予以重罚。为检验驾驶员是否酒后驾车,可采用的检验方法有多种。回答以下问题:
(1)早期曾经采用五氧化二碘和某种高分子化合物X的混合溶液来检测酒精的存在。理是:I2O5与CH3CH2OH先发生反应(I2O5+5CH3CH2OH=I2+5Y+5H2O),生成的I2与高分子化合物X作用而变蓝。交警依据此原理来检测驾驶员是否饮酒。则:X的化学式是_____________ ;Y的化学式是_________ ;
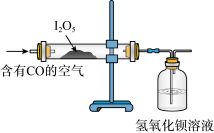
(2)已知:I2O5是白色固体,可用于检验并定量测定空气中CO;两者在常温条件下发生的反应为5CO+I2O5=5CO2+I2(空气中其余气体不与I2O5反应);某同学设计如图实验装置完成上述目的。
①指出能证明空气中有CO存在的现象:_____________ 。
②将上述反应生成的碘单质用硫代硫酸钠滴定(反应为I2+2Na2S2O3=Na2S4O6+2NaI),即可根据消耗硫代硫酸钠的量来计算空气中CO的含量。若某次实验时测得参与反应的空气体积为a mL(标准状况下),滴定过程中,共消耗vmLcmol·L﹣1Na2S2O3溶液,则该空气样品中CO的体积分数是________ 。
③有同学提出只要依据参与反应的空气体积和洗气瓶中白色沉淀的质量也可求得空气中CO。此方案是否可行?_________ 。
(3)燃料电池酒精检测仪(该电池以硫酸溶液为电解质溶液)也是检测酒精含量的一种方法。总反应是:CH3CH2OH+O2=CH3COOH+H2O。该电池负极电极反应式是________________ 。
(4)酒精是一种较为环保的燃料,298K时,1g乙醇完全燃烧放出热量qkJ,写出乙醇燃烧的热化学方程式________ 。
(1)早期曾经采用五氧化二碘和某种高分子化合物X的混合溶液来检测酒精的存在。理是:I2O5与CH3CH2OH先发生反应(I2O5+5CH3CH2OH=I2+5Y+5H2O),生成的I2与高分子化合物X作用而变蓝。交警依据此原理来检测驾驶员是否饮酒。则:X的化学式是
(2)已知:I2O5是白色固体,可用于检验并定量测定空气中CO;两者在常温条件下发生的反应为5CO+I2O5=5CO2+I2(空气中其余气体不与I2O5反应);某同学设计如图实验装置完成上述目的。

①指出能证明空气中有CO存在的现象:
②将上述反应生成的碘单质用硫代硫酸钠滴定(反应为I2+2Na2S2O3=Na2S4O6+2NaI),即可根据消耗硫代硫酸钠的量来计算空气中CO的含量。若某次实验时测得参与反应的空气体积为a mL(标准状况下),滴定过程中,共消耗vmLcmol·L﹣1Na2S2O3溶液,则该空气样品中CO的体积分数是
③有同学提出只要依据参与反应的空气体积和洗气瓶中白色沉淀的质量也可求得空气中CO。此方案是否可行?
(3)燃料电池酒精检测仪(该电池以硫酸溶液为电解质溶液)也是检测酒精含量的一种方法。总反应是:CH3CH2OH+O2=CH3COOH+H2O。该电池负极电极反应式是
(4)酒精是一种较为环保的燃料,298K时,1g乙醇完全燃烧放出热量qkJ,写出乙醇燃烧的热化学方程式
您最近一年使用:0次



