13-14高三·湖北省直辖县级单位·阶段练习
1 . Ⅰ.在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如下图所示,试回答下列问题:

(1)该合成路线对于环境保护的价值在于______ 。
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。用离子方程式表示乙醇胺水溶液呈弱碱性的原因______ 。
(3)CH3OH、H2的燃烧热分别为:△H=-725.5 kJ/mol、△H=-285.8 kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:______ 。
Ⅱ.将燃煤废气中的CO2转化为甲醚的反应原理为:2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g)。已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
CH3OCH3(g) + 3H2O(g)。已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
(4)该反应的焓变△H______ 0,熵变△S______ 0(填>、<或=)。
(5)用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式______ 。
(6)若以1.12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜______ g。

(1)该合成路线对于环境保护的价值在于
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。用离子方程式表示乙醇胺水溶液呈弱碱性的原因
(3)CH3OH、H2的燃烧热分别为:△H=-725.5 kJ/mol、△H=-285.8 kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:
Ⅱ.将燃煤废气中的CO2转化为甲醚的反应原理为:2CO2(g) + 6H2(g)
 CH3OCH3(g) + 3H2O(g)。已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
CH3OCH3(g) + 3H2O(g)。已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:| 投料比[n(H2) / n(CO2)] | 500 K | 600 K | 700 K | 800 K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
(4)该反应的焓变△H
(5)用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式
(6)若以1.12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜
您最近半年使用:0次
名校
2 . 科技的进步为二氧化碳的资源化利用提供了广阔的前景,我国科学家首次在实验室实现 CO2到淀粉的合成,其路线如下,

设NA为阿伏加德罗常数的值。下列说法错误的是

设NA为阿伏加德罗常数的值。下列说法错误的是
| A.标准状况下,11.2 L CO2含有的共用电子对的数目为NA |
| B.常温常压下,16 gCH3OH 含有的极性键数目为2.5NA |
| C.标准状况下,42 g C2H4和CO混合气体的体积为33.6 L |
| D.已知:2CO(g)+O2(g)=2CO2(g) ΔH=-565.8kJ/mol,则CO的燃烧热为282.9 kJ/mol |
您最近半年使用:0次
解题方法
3 . 科技工作者利用工业生产废气二氧化碳(含氮的氧化物和硫的氧化物杂质)与太阳能电解水产生的氢气合成甲醇 ,合成过程如下图所示:
,合成过程如下图所示:
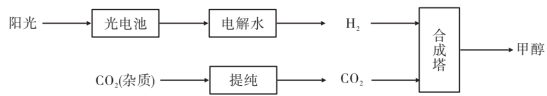
已知甲醇、氢气的燃烧热分别为:
下列说法错误的是
 ,合成过程如下图所示:
,合成过程如下图所示:
已知甲醇、氢气的燃烧热分别为:

下列说法错误的是
| A.框图中反映的是光能→电能→化学能的能量转化过程 |
| B.上述合成路线对于环境保护的价值在于能减少温室气体的排放 |
C.甲醇燃烧的热化学方程式: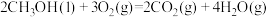 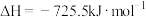 |
D.二氧化碳、氢气合成甲醇的热化学方程式: 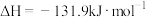 |
您最近半年使用:0次
名校
解题方法
4 . 甲烷是最简单的烃,可用来作为燃料,也是一种重要的化工原料。
(1) A.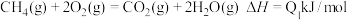
B.
C.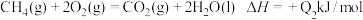
D.
上述热化学方程式中的反应热能正确表示甲烷燃烧热的是___________ 。
(2)以甲烷为原料通过以下反应可以合成甲醇: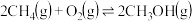
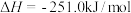
现将 和
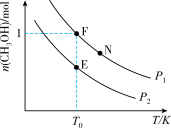
和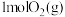 充入密闭容器中,在不同温度和压强下进行上述反应。实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示:
充入密闭容器中,在不同温度和压强下进行上述反应。实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示:
① 时升高温度,
时升高温度,
___________ (填“增大”、“减小”或“不变”);
___________  (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
②E、F、N点对应的化学反应速率由大到小的顺序为___________ (用 表示);
表示);
③下列能提高 平衡转化率的措施是
平衡转化率的措施是___________ (填序号);
a.选择高效催化剂 b.增大 投料比 c.及时分离产物
投料比 c.及时分离产物
④若 点,
点, ,总压强为
,总压强为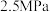 ,则
,则 时
时 点用分压强代替浓度表示的平衡常数
点用分压强代替浓度表示的平衡常数
___________ 。
(1) A.
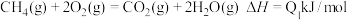
B.

C.
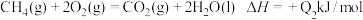
D.

上述热化学方程式中的反应热能正确表示甲烷燃烧热的是
(2)以甲烷为原料通过以下反应可以合成甲醇:
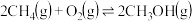
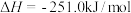
现将
 和
和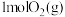 充入密闭容器中,在不同温度和压强下进行上述反应。实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示:
充入密闭容器中,在不同温度和压强下进行上述反应。实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示:
①
 时升高温度,
时升高温度,

 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);②E、F、N点对应的化学反应速率由大到小的顺序为
 表示);
表示);③下列能提高
 平衡转化率的措施是
平衡转化率的措施是a.选择高效催化剂 b.增大
 投料比 c.及时分离产物
投料比 c.及时分离产物④若
 点,
点, ,总压强为
,总压强为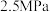 ,则
,则 时
时 点用分压强代替浓度表示的平衡常数
点用分压强代替浓度表示的平衡常数
您最近半年使用:0次
2023-12-15更新
|
220次组卷
|
3卷引用:辽宁省辽东南协作校2023-2024学年高三上学期12月月考化学(A卷)试题
5 . 短周期的元素在自然界中比较常见,尤其是非金属元素及其化合物在社会生活中有着很重要的作用。
(1)红酒中添加一定量的SO2可以防止酒液氧化,这利用了SO2的______ 性。自来水中含硫量约70mg/L,它只能以_____ (填微粒符号)形式存在。
(2)实验室可用浓氨水与氢氧化钠固体作用制取氨气,试用平衡原理分析氢氧化钠的作用:_____ 。
(3)如图是向5mL0.1mol·L-1氨水中逐滴滴加0.1mol·L-1醋酸,测量其导电性的数字化实验曲线图,请你解释曲线变化的原因_____ 。

甲硫醇(CH3SH)是一种重要的有机合成原料,用于合成染料、医药、农药等。工业上可用甲醇和硫化氢气体制取:CH3OH+H2S CH3SH+H2O。
CH3SH+H2O。
完成下列填空:
(4)写出该反应的化学平衡常数表达式_____ 。该反应的温度为280~450℃,选该反应温度可能的原因是:①加快反应速率;②_____ 。
(5)已知在2L密闭容器中,只加入反应物,进行到10分钟时达到平衡,测得水的质量为5.4g,则v(CH3SH)=_____ mol/(L•min)。
(6)常温常压下,2.4g甲硫醇完全燃烧生成二氧化硫和其他稳定产物,并同时放出52.42kJ的热量,则甲硫醇燃烧的热化学方程式为______ 。
(1)红酒中添加一定量的SO2可以防止酒液氧化,这利用了SO2的
(2)实验室可用浓氨水与氢氧化钠固体作用制取氨气,试用平衡原理分析氢氧化钠的作用:
(3)如图是向5mL0.1mol·L-1氨水中逐滴滴加0.1mol·L-1醋酸,测量其导电性的数字化实验曲线图,请你解释曲线变化的原因

甲硫醇(CH3SH)是一种重要的有机合成原料,用于合成染料、医药、农药等。工业上可用甲醇和硫化氢气体制取:CH3OH+H2S
 CH3SH+H2O。
CH3SH+H2O。| 熔点(℃) | 沸点(℃) | |
| 甲醇 | -97 | 64.7 |
| 甲硫醇 | -123 | 7.6 |
完成下列填空:
(4)写出该反应的化学平衡常数表达式
(5)已知在2L密闭容器中,只加入反应物,进行到10分钟时达到平衡,测得水的质量为5.4g,则v(CH3SH)=
(6)常温常压下,2.4g甲硫醇完全燃烧生成二氧化硫和其他稳定产物,并同时放出52.42kJ的热量,则甲硫醇燃烧的热化学方程式为
您最近半年使用:0次
名校
解题方法
6 . 乙醇(C2H5OH)是生活中常见燃料,可以通过:
方法一,植物中淀粉类或者糖类物随采用发酵方式生产;
方法二,石油化学工业使用乙烯为原料合成。回答下列问题
(1)生物质能是人类解决能源危机的重要途径之· ,下列有关生物质能的说法正确的是______
A.利用生物质能就是间接利用太阳能
B.生物质能是可再生能源
C.生物质能的缺点是严重污染环境
D.生物质能是解决农村问题的重要途径
(2)乙醇可以直接用作燃料,也可以设计乙醇一空气燃料电池,以氢氧化钾溶液做电解质,写出负极的电极反应__________ ;若以熔融的碳酸盐做电解质,写出负极的电极反应式______ ;
(3)已知乙醇的燃烧热为1366.8kJ/mol,根据下列反应的反应热:
C(s)+O2(g)═2CO2(g) △H=-393.5kJ·mol-1
H2(g)+ O2(g)=H2O(1) △H=-285.8 kJ/mol
O2(g)=H2O(1) △H=-285.8 kJ/mol
则理论上以C(s)、H2(g)、O2(g)为原料合成C2H5OH(1)的反应的热化学方程式为_________ 。
方法一,植物中淀粉类或者糖类物随采用发酵方式生产;
方法二,石油化学工业使用乙烯为原料合成。回答下列问题
(1)生物质能是人类解决能源危机的重要途径之· ,下列有关生物质能的说法正确的是
A.利用生物质能就是间接利用太阳能
B.生物质能是可再生能源
C.生物质能的缺点是严重污染环境
D.生物质能是解决农村问题的重要途径
(2)乙醇可以直接用作燃料,也可以设计乙醇一空气燃料电池,以氢氧化钾溶液做电解质,写出负极的电极反应
(3)已知乙醇的燃烧热为1366.8kJ/mol,根据下列反应的反应热:
C(s)+O2(g)═2CO2(g) △H=-393.5kJ·mol-1
H2(g)+
 O2(g)=H2O(1) △H=-285.8 kJ/mol
O2(g)=H2O(1) △H=-285.8 kJ/mol 则理论上以C(s)、H2(g)、O2(g)为原料合成C2H5OH(1)的反应的热化学方程式为
您最近半年使用:0次
名校
解题方法
7 . 研究化学反应中的能量和速率变化对生产、生活有着重要意义。
Ⅰ.煤和石油燃烧生成的 为大气主要污染物之一、硫与硫的氧化物在转化过程中的能量变化如图1所示。
为大气主要污染物之一、硫与硫的氧化物在转化过程中的能量变化如图1所示。
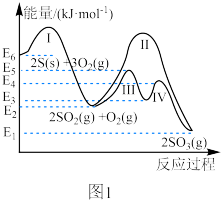
(1)写出表示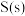 的燃烧热的热化学方程式:
的燃烧热的热化学方程式:_____ 。
Ⅱ.实验室模拟热气循环法合成尿素, 与
与 在一定条件下发生反应:
在一定条件下发生反应:
 。
。
为了验证反应温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
(2)控制变量是科学研究的重要方法,因此表中数据:a=_____ ,T1=_____ 。
(3)对比实验①③,目的是验证_____ (填“反应温度”或“催化剂的比表面积”)对化学反应速率的影响规律。
(4)一定温度下,向1L密闭容器中充入 和
和 发生反应:
发生反应: ,若起始压强为
,若起始压强为 ,反应
,反应 后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则
后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则 内,
内,
_____  ,
, 的平衡转化率为
的平衡转化率为_____  。
。
(5)下列情况中,一定能说明上述反应达到平衡的是_____(填标号)。
(6)“碳呼吸电池”是一种新型化学电源,其工作原理如图2.正极的电极反应式为_____ ;当得到 时,电路中转移的电子的物质的量为
时,电路中转移的电子的物质的量为_____  。
。

Ⅰ.煤和石油燃烧生成的
 为大气主要污染物之一、硫与硫的氧化物在转化过程中的能量变化如图1所示。
为大气主要污染物之一、硫与硫的氧化物在转化过程中的能量变化如图1所示。
(1)写出表示
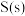 的燃烧热的热化学方程式:
的燃烧热的热化学方程式:Ⅱ.实验室模拟热气循环法合成尿素,
 与
与 在一定条件下发生反应:
在一定条件下发生反应:
 。
。为了验证反应温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
| 实验编号 | T/℃ | CO2初始浓度/ (mol·L-1) | NH3初始浓度/ (mol·L-1) | 催化剂的比表面积/ (m2·g-1) |
| ① | 280 |  | 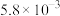 | 82 |
| ② | T1 |  | 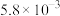 | 124 |
| ③ | 350 | a | 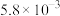 | 82 |
(3)对比实验①③,目的是验证
(4)一定温度下,向1L密闭容器中充入
 和
和 发生反应:
发生反应: ,若起始压强为
,若起始压强为 ,反应
,反应 后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则
后该反应达到化学平衡状态,平衡时的压强是起始时的0.8倍,则 内,
内,
 ,
, 的平衡转化率为
的平衡转化率为 。
。(5)下列情况中,一定能说明上述反应达到平衡的是_____(填标号)。
A. 的体积分数保持不变 的体积分数保持不变 |
| B.反应体系中气体的密度保持不变 |
C.反应消耗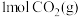 ,同时生成 ,同时生成  |
D. 的质量保持不变 的质量保持不变 |
 时,电路中转移的电子的物质的量为
时,电路中转移的电子的物质的量为 。
。
您最近半年使用:0次
2023-10-20更新
|
138次组卷
|
4卷引用:河北省部分学校2023-2024学年高三上学期9月月考化学试题
名校
8 . 氨是合成硝酸、铵盐和氮肥的基本原料,氮的氧化物是大气的污染物,请问:
(1)氨的水溶液显弱碱性,其原因为___________ (用离子方程式表示),0.1 mol•L-1的氨水中加入少量的NH4Cl固体,溶液的pH ___________ (填“增大”或“减小”);若加入少量的明矾,溶液中的 的浓度
的浓度 ___________ (填“增大”或“减小”)。
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为___________ ,平衡常数表达式为___________ ;若有1mol硝酸铵完全分解,转移的电子数为___________ mol。
(3)甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJ·mol-1,甲醚可作燃料电池的燃料。已知H2(g)和C(s)的燃烧热分别是285.8 kJ·mol-1、393.5 kJ·mol-1;计算反应4C(s)+ 6H2(g)+ O2(g)=2CH3OCH3(g)的反应热为___________ ;
(4)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+ 2CO2(g) CH3OCH3(g)+ 3H2O(g) △H<0
CH3OCH3(g)+ 3H2O(g) △H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应达到化学平衡状态的是______ (选填编号,注意大小写)
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时,有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后,达到新的平衡,CH3OCH3的产率将___________ (填“变大”、“变小”或“不变”)。
(1)氨的水溶液显弱碱性,其原因为
 的浓度
的浓度 (2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为
(3)甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJ·mol-1,甲醚可作燃料电池的燃料。已知H2(g)和C(s)的燃烧热分别是285.8 kJ·mol-1、393.5 kJ·mol-1;计算反应4C(s)+ 6H2(g)+ O2(g)=2CH3OCH3(g)的反应热为
(4)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+ 2CO2(g)
 CH3OCH3(g)+ 3H2O(g) △H<0
CH3OCH3(g)+ 3H2O(g) △H<0①一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应达到化学平衡状态的是
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时,有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后,达到新的平衡,CH3OCH3的产率将
您最近半年使用:0次
9 . 我国在第75届联合国大会上正式提出了2030年实现碳达峰、2060年实现碳中和的目标,所以研发利用二氧化碳技术,降低空气中二氧化碳含量成为重要的任务。
Ⅰ.化石燃料的燃烧产生大量的二氧化碳。已知25℃时,相关物质的燃烧热数据如表:
(1)则25℃时H2(g)和C(石墨,s)生成C2H2(l)的热化学方程式为___________ 。
Ⅱ.二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一
甲烷化主反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH =-165 kJ∙mol-1
CH4(g)+2H2O(g) ΔH =-165 kJ∙mol-1
副反应:ⅰ.CO(g)+3H2(g) CH4(g)+H2O(g) ΔH1 =___________;
CH4(g)+H2O(g) ΔH1 =___________;
ⅱ.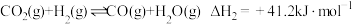 ;
;
ⅲ. =-90kJ∙mol-1;
=-90kJ∙mol-1;
ⅳ. C(s)+H2O(g) CO(g)+H2(g) ΔH4 = +131.3kJ∙mol-1。
CO(g)+H2(g) ΔH4 = +131.3kJ∙mol-1。
(2)反应ⅰ的ΔH1=___________ 。
(3)在恒温恒容的密闭容器中,关于反应ⅲ叙述正确的是___________。
(4)某容器中加入一定量的CO2和H2,保持温度和压强不变的情况下,达平衡后再向该容器中注入Ar稀释,反应ⅲ的化学平衡将___________ (填“正向移动”“逆向移动”或“不移动”),平衡时,CO2的分压P(CO2)___________ (填“增大”、“减小”或“不变”,下同)。
(5)以4molH2和1molCO2为初始原料,在催化剂(Ni/xMg)作用下保持总压为P0时,若只发生反应 ,不同温度下在相同时间测得CO2的转化率如图所示。
,不同温度下在相同时间测得CO2的转化率如图所示。
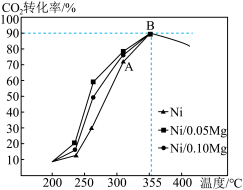
①B点的平衡常数KP___________ 。
②由图像可知,影响该催化剂活性的因素有___________ 。
Ⅰ.化石燃料的燃烧产生大量的二氧化碳。已知25℃时,相关物质的燃烧热数据如表:
| 物质 | H2(g) | C(石墨,s) | C2H2(l) |
| 燃烧热ΔH(kJ∙mol-1) | -285.8 | -393.5 | -1299.5 |
Ⅱ.二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一
甲烷化主反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH =-165 kJ∙mol-1
CH4(g)+2H2O(g) ΔH =-165 kJ∙mol-1副反应:ⅰ.CO(g)+3H2(g)
 CH4(g)+H2O(g) ΔH1 =___________;
CH4(g)+H2O(g) ΔH1 =___________;ⅱ.
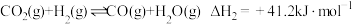 ;
;ⅲ.
 =-90kJ∙mol-1;
=-90kJ∙mol-1;ⅳ. C(s)+H2O(g)
 CO(g)+H2(g) ΔH4 = +131.3kJ∙mol-1。
CO(g)+H2(g) ΔH4 = +131.3kJ∙mol-1。(2)反应ⅰ的ΔH1=
(3)在恒温恒容的密闭容器中,关于反应ⅲ叙述正确的是___________。
| A.用CO2、H2、H2O表示的速率之比为1:2:2,可以作为判断化学平衡的依据。 |
| B.容器中气体的压强不变,不能作为平衡的判断依据。 |
| C.容器内的气体密度不变时,可以作为平衡的判断依据。 |
| D.使用催化剂不能改变平衡转化率。 |
(5)以4molH2和1molCO2为初始原料,在催化剂(Ni/xMg)作用下保持总压为P0时,若只发生反应
 ,不同温度下在相同时间测得CO2的转化率如图所示。
,不同温度下在相同时间测得CO2的转化率如图所示。
①B点的平衡常数KP
②由图像可知,影响该催化剂活性的因素有
您最近半年使用:0次
解题方法
10 . 化学反应中的能量变化通常表现为热量变化,研究热量变化具有重要的意义。化学反应的反应热可通过实验测定,也可通过计算间接获得。
(1)下列变化属于吸热反应的是___________ (填序号)。
①液态水气化 ②胆矾加热变成白色粉末 ③浓硫酸稀释 ④氢气还原氧化铜
⑤碳酸钙高温分解 ⑥氢氧化钾和稀硫酸反应 ⑦灼热的木炭与 的反应
的反应
⑧ 晶体与
晶体与 晶体的反应 ⑨甲烷在空气中燃烧的反应
晶体的反应 ⑨甲烷在空气中燃烧的反应
(2)在25℃、101kPa下,23g乙醇 完全燃烧生成
完全燃烧生成 和液态水时放热638.4kJ,则表示乙醇燃烧热的热化学方程式为
和液态水时放热638.4kJ,则表示乙醇燃烧热的热化学方程式为___________ 。
I.中和反应反应热的实验测定
设计实验测定反应 的
的
(3)实验室中盐酸和NaOH溶液已耗尽,请你为该兴趣小组推荐一种酸和一种碱___________ 。
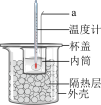
(4)选用合理的试剂,用如图装置进行实验,其中仪器a的名称为___________ 。某次实验测得中和热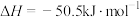 ,与理论值
,与理论值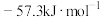 出现较大偏差,产生偏差的原因不可能是
出现较大偏差,产生偏差的原因不可能是___________ (填字母序号)
A.实验装置保温、隔热效果差
B.分多次把碱溶液倒入盛有酸的小烧杯中
C.用温度计测定碱溶液起始温度后直接测定酸溶液的温度
D.用量筒量取酸和碱溶液的体积时均仰视读数
II.通过计算间接获得反应热
(5)利用合成气(主要成分为CO、 和
和 )在催化剂作用下合成甲醇,发生的主要反应如下:
)在催化剂作用下合成甲醇,发生的主要反应如下:
①

②

③
 ,
,
已知反应①中相关的化学键键能数据如下:
(已知甲醇与CO的结构式分别如图: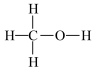
 )
)
由此计算
___________ ;已知 ,则
,则
___________ 。
(1)下列变化属于吸热反应的是
①液态水气化 ②胆矾加热变成白色粉末 ③浓硫酸稀释 ④氢气还原氧化铜
⑤碳酸钙高温分解 ⑥氢氧化钾和稀硫酸反应 ⑦灼热的木炭与
 的反应
的反应⑧
 晶体与
晶体与 晶体的反应 ⑨甲烷在空气中燃烧的反应
晶体的反应 ⑨甲烷在空气中燃烧的反应(2)在25℃、101kPa下,23g乙醇
 完全燃烧生成
完全燃烧生成 和液态水时放热638.4kJ,则表示乙醇燃烧热的热化学方程式为
和液态水时放热638.4kJ,则表示乙醇燃烧热的热化学方程式为I.中和反应反应热的实验测定
设计实验测定反应
 的
的
(3)实验室中盐酸和NaOH溶液已耗尽,请你为该兴趣小组推荐一种酸和一种碱
(4)选用合理的试剂,用如图装置进行实验,其中仪器a的名称为
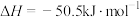 ,与理论值
,与理论值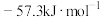 出现较大偏差,产生偏差的原因不可能是
出现较大偏差,产生偏差的原因不可能是
A.实验装置保温、隔热效果差
B.分多次把碱溶液倒入盛有酸的小烧杯中
C.用温度计测定碱溶液起始温度后直接测定酸溶液的温度
D.用量筒量取酸和碱溶液的体积时均仰视读数
II.通过计算间接获得反应热
(5)利用合成气(主要成分为CO、
 和
和 )在催化剂作用下合成甲醇,发生的主要反应如下:
)在催化剂作用下合成甲醇,发生的主要反应如下:①


②


③

 ,
,已知反应①中相关的化学键键能数据如下:
| 化学键 |  |  |  |  |  |
 | 436 | 343 | 1076 | 465 | 413 |

 )
)由此计算

 ,则
,则
您最近半年使用:0次



