名校
1 . 过氧乙酸(CH3CO3H)是一种广谱高效消毒剂,不稳定、易分解,高浓度易爆炸。常用于空气、器材的消毒,可由乙酸与H2O2在硫酸催化下反应制得,热化学方程式为:CH3COOH(aq)+H2O2(aq) CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
(1)利用上述反应制备760g CHCOH,放出的热量为_______ kJ。
(2)取质量相等的冰醋酸和50% H2O2溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在25℃下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应(反应均未达到平衡),测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
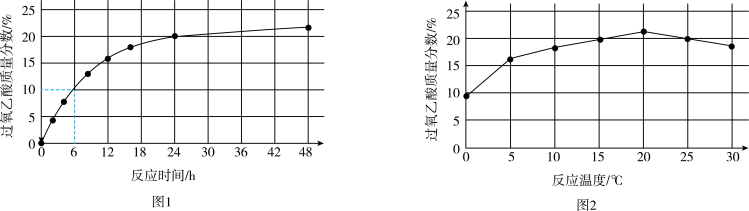 ①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=
①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=_____ g/h。(用含m的代数式表示)
②综合图1、图2分析,与20℃相比,25℃时过氧乙酸产率降低的可能原因是_______ (写出2条)。
(3)SV-1、SV-2是两种常用于实验研究的病毒,粒径分别为40nm和70nm。病毒在水中可能会聚集成团簇。不同pH下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
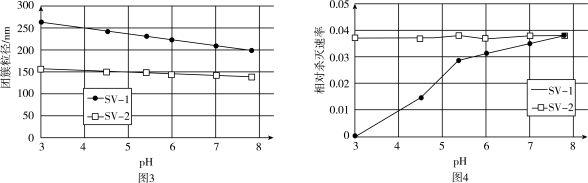
依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是___________ 。
 CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol(1)利用上述反应制备760g CHCOH,放出的热量为
(2)取质量相等的冰醋酸和50% H2O2溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在25℃下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应(反应均未达到平衡),测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
 ①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=
①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=②综合图1、图2分析,与20℃相比,25℃时过氧乙酸产率降低的可能原因是
(3)SV-1、SV-2是两种常用于实验研究的病毒,粒径分别为40nm和70nm。病毒在水中可能会聚集成团簇。不同pH下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。

依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是
您最近一年使用:0次
名校
解题方法
2 . 一些烷烃的燃烧热如下表:
下列表达正确的是
| 化合物 | 燃烧热 |
| 甲烷 | 891.0 |
| 乙烷 | 1560.8 |
| 丙烷 | 2221.5 |
| 正丁烷 | 2878.0 |
| 异丁烷 | 2869.6 |
| 2-甲基丁烷 | 3531.3 |
A.正戊烷的燃烧热大于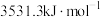 |
| B.稳定性:正丁烷>异丁烷 |
C.乙烷燃烧的热化学方程式为 |
| D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
您最近一年使用:0次
名校
3 . 恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。[已知:2SO2(g)+O2(g) 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
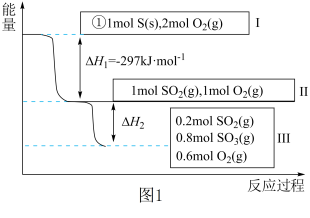
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:___________ 。
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|___________ (填“大”、“小”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是___________ ;图中表示平衡混合物中SO3的含量最高的一段时间是___________ 。

 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
| A.升高温度 | B.充入He | C.再充入1mol SO2(g)和1mol O2(g) | D.使用催化剂 |
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是

您最近一年使用:0次
名校
解题方法
4 . 下列热化学方程式正确的是
A.理论上1 kg黄铁矿(FeS2的含量为84%)完全燃烧放出的热量5950 kJ,则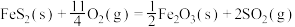 △H=-850 kJ/mol △H=-850 kJ/mol |
B.500℃、30 MPa下,将0.5 molN2(g)和1.5 molH2(g)置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为 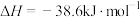 |
| C.稀盐酸和NaOH溶液反应的中和热△H=-57.3 kJ/mol,则稀H2SO4和Ba(OH)2溶液反应的中和热为2×57.3 kJ/mol |
D.甲烷的燃烧热△H=-890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为: 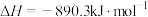 |
您最近一年使用:0次
10-11高二下·安徽马鞍山·期中
名校
解题方法
5 . 一些烷烃的燃烧热如下表:
下列说法正确的是
| 化合物 | ΔH/(kJ·mol-1) | 化合物 | ΔH/(kJ·mol-1) |
| 甲烷 | -891.0 | 正丁烷 | -2878.0 |
| 乙烷 | -1560.8 | 异丁烷 | -2869.6 |
| 丙烷 | -2221.5 | 2-甲基丁烷 | -3531.3 |
| A.正戊烷的燃烧热大约是3540 kJ·mol-1 |
| B.热稳定性:正丁烷>异丁烷 |
| C.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g) ΔH=-1560.8 kJ·mol-1 |
| D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
您最近一年使用:0次
2021-08-27更新
|
574次组卷
|
17卷引用:2010-2011学年安徽省马鞍山市第二中学高二下学期期中素质测试化学试卷
(已下线)2010-2011学年安徽省马鞍山市第二中学高二下学期期中素质测试化学试卷(已下线)2010—2011学年安徽省马鞍山二中高二下学期期中考试化学试卷(理科)(已下线)必考点01 化学反应的热效应-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)河南省信阳市2021-2022学年高二上学期期中考试化学试题江西省上饶市玉山县第一中学2015-2016学年高二下学期重点班第一次月考化学卷(已下线)2018年10月16日 《每日一题》人教选修4-燃烧热及表示燃烧热的热化学方程式(已下线)考点08 化学反应中的热效应——备战2019年浙江新高考化学考点步步为赢 高二化学暑假作业:作业七 化学反应与能量黑龙江省牡丹江市第一高级中学2019-2020学年高二上学期开学检测化学试题浙江省杭州市西湖高级中学2019-2020学年高二10月月考化学试题(已下线)考点08 化学反应中的能量变化——《备战2020年高考精选考点专项突破题集》宁夏银川一中2020-2021学年高二上学期期末考试化学试题河南省洛阳市豫西名校2020-2021学年高二下学期第一次联考化学试题第23届(2009年)全国高中学生化学竞赛(安徽赛区)初赛试题(已下线)1.1.3 能源的充分利用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1) 福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题湖北省部分重点中学2022-2023学年高三下学期2月质量检测化学试题
解题方法
6 . 汽车等交通工具为出行、物流等带来方便。然而,燃油车排放的汽车尾气中含有大量的有害物质,会对人体健康和环境产生危害。
(1)汽油在不同空燃比(空气与燃油气的体积比)时尾气的主要成分不同,空燃比较小时的有毒气体主要是_______ (填化学式)
(2)辛烷(C8H18)是汽油的主要成分之一,已知辛烷的燃烧热 ,请写出表示辛烷燃烧热的热化学方程式
,请写出表示辛烷燃烧热的热化学方程式_______ 。
(3)空气中的氮气和氧气在汽车汽缸内的高温环境下,通过电火花放电生成有毒气体NO,反应的热化学方程式:
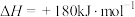 。已知:N2、O2分子中化学键的键能分别是946
。已知:N2、O2分子中化学键的键能分别是946 、497
、497 。请计算NO分子中化学键的键能为
。请计算NO分子中化学键的键能为_______  。
。
(4)为减轻污染,现在汽车上都安装三元催化转化器,可实现反应: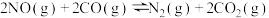
 。则该反应在
。则该反应在_______ (填“高温”、“低温”或“任何温度”)下能自发进行。
(5)将NO和CO以一定的流速通过两种不同的催化剂进行反应,经过相同时间内测量逸出气体中NO的含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图所示。
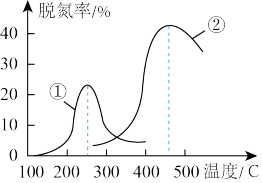
以下说法不正确的是_______。
(1)汽油在不同空燃比(空气与燃油气的体积比)时尾气的主要成分不同,空燃比较小时的有毒气体主要是
(2)辛烷(C8H18)是汽油的主要成分之一,已知辛烷的燃烧热
 ,请写出表示辛烷燃烧热的热化学方程式
,请写出表示辛烷燃烧热的热化学方程式(3)空气中的氮气和氧气在汽车汽缸内的高温环境下,通过电火花放电生成有毒气体NO,反应的热化学方程式:

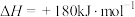 。已知:N2、O2分子中化学键的键能分别是946
。已知:N2、O2分子中化学键的键能分别是946 、497
、497 。请计算NO分子中化学键的键能为
。请计算NO分子中化学键的键能为 。
。(4)为减轻污染,现在汽车上都安装三元催化转化器,可实现反应:
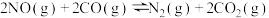
 。则该反应在
。则该反应在(5)将NO和CO以一定的流速通过两种不同的催化剂进行反应,经过相同时间内测量逸出气体中NO的含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图所示。

以下说法不正确的是_______。
| A.曲线②中催化剂脱氮率比曲线①中的高 |
| B.曲线②中的催化剂适用于450℃左右脱氢 |
| C.曲线①、②最高点表示此时平衡转化率 |
| D.若低于200℃,图中曲线①脱氮率随温度升高而变化不大的主要原因是催化剂的活性不高 |
您最近一年使用:0次
名校
7 . 下列图示与对应叙述相符的是
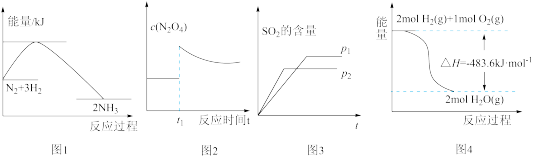

| A.图1反应达平衡后,升高温度,平衡常数K值减小 |
B.图2表示平衡2NO2(g) N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 |
C.图3表示可逆反应“2SO2+O2 2SO3”中SO2的含量与压强的关系,且P2>P1 2SO3”中SO2的含量与压强的关系,且P2>P1 |
| D.图4表示H2与O2发生反应过程中的能量变化,则H2的燃烧热ΔH=-241.8kJ•mol-1 |
您最近一年使用:0次
2022-09-27更新
|
328次组卷
|
3卷引用:湖南省邵阳市第二中学2022-2023学年高二上学期期中考试化学试题
8 . 苯乙烯是一种重要的有机化工原料,可广泛用于合成橡胶,工程塑料及制药等。工业上可通过乙苯催化脱氢来制取苯乙烯,反应方程式如下:
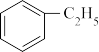 (g)
(g)
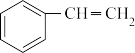 (g)+H2(g) ΔH
(g)+H2(g) ΔH
(1)已知部分物质的燃烧热数据如下表:
则
_______ 。
(2)下列关于反应的说法正确的是_______(填序号)
(3)工业装置通常采用铁基氧化物催化剂,通入过热水蒸气(615~645℃)、水油比(水与乙苯质量比)1.4~1.8、常压的条件下发生乙苯的催化脱氢反应。
①反应中通入水蒸气的作用是_______ 。
②将物质的量分数组成为m%乙苯(g)、n% 的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为
的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为 ,则苯乙烯的分压为
,则苯乙烯的分压为_______ ,平衡常数
_______ (以分压表示,分压=总压×物质的量分数)
(4)近年来,有研究者发现若将上述生产过程中通入 改为通入
改为通入 ,通入
,通入 后会发生反应
后会发生反应 。在常压下,分别按投料比为仅乙苯,乙苯
。在常压下,分别按投料比为仅乙苯,乙苯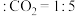 ,乙苯
,乙苯 ,测得乙苯的平衡转化率与温度的关系如下图。
,测得乙苯的平衡转化率与温度的关系如下图。
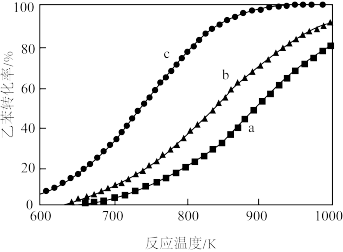
则乙苯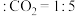 对应的曲线为
对应的曲线为_______ (填“a”,“b”或“c”),理由是_______ 。
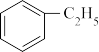 (g)
(g)
 (g)+H2(g) ΔH
(g)+H2(g) ΔH(1)已知部分物质的燃烧热数据如下表:
| 物质 | 乙苯 | 苯乙烯 | 氢气 |
燃烧热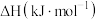 | -4610.2 | -4441.8 | -285.8 |

(2)下列关于反应的说法正确的是_______(填序号)
| A.高温有利于反应自发进行 |
| B.工业生产中应尽可能提高反应温度,并增大压强,以提高原料的利用率 |
| C.恒温恒容条件下,反应达到平衡后,向体系中再充入乙苯蒸气,乙苯的转化率将增大 |
| D.选择合适的催化剂可以缩短达到平衡的时间,但不会提高生成物中苯乙烯的含量 |
①反应中通入水蒸气的作用是
②将物质的量分数组成为m%乙苯(g)、n%
 的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为
的气体通入反应器,在温度t、压强p下进行反应。平衡时,乙苯的转化率为 ,则苯乙烯的分压为
,则苯乙烯的分压为
(4)近年来,有研究者发现若将上述生产过程中通入
 改为通入
改为通入 ,通入
,通入 后会发生反应
后会发生反应 。在常压下,分别按投料比为仅乙苯,乙苯
。在常压下,分别按投料比为仅乙苯,乙苯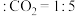 ,乙苯
,乙苯 ,测得乙苯的平衡转化率与温度的关系如下图。
,测得乙苯的平衡转化率与温度的关系如下图。
则乙苯
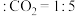 对应的曲线为
对应的曲线为
您最近一年使用:0次
9 . 下列说法正确的是
A.S(s)+ O2(g)=SO3(g) ΔH=-315 kJ·mol-1(燃烧热)(ΔH的数值正确) O2(g)=SO3(g) ΔH=-315 kJ·mol-1(燃烧热)(ΔH的数值正确) |
B.葡萄糖的燃烧热是2 800 kJ·mol-1,则 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(g) ΔH=-1 400 kJ·mol-1 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(g) ΔH=-1 400 kJ·mol-1 |
| C.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的反应热ΔH=2×(-57.3)kJ·mol-1 |
| D.开发利用各种新能源,减少对化石燃料的依赖,可以降低空气中PM2.5的含量 |
您最近一年使用:0次
2022-04-04更新
|
194次组卷
|
2卷引用:新疆乌鲁木齐市第八中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
10 . 一些烷烃的燃烧热(kJ/mol)如下:
下列推断正确的是
| 化合物 | 燃烧热 | 化合物 | 燃烧热 |
| 甲烷 | 891.0 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 2-甲基丁烷 | 3531.3 |
下列推断正确的是
| A.热稳定性:正丁烷>异丁烷 |
| B.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g)+1560.8kJ |
| C.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量就越多 |
| D.正戊烷的燃烧热大约在3540 kJ/mol左右 |
您最近一年使用:0次
2020-03-22更新
|
201次组卷
|
3卷引用:上海市奉贤区2015届高三上学期期中调研测试化学试题



