名校
解题方法
1 . 下列各组热化学方程式中,化学反应的ΔH前者大于后者的有
①H2(g)+F2(g)=2HF(g) ΔH1 H2(g)+Cl2(g)=2HCl(g) ΔH2
②C8H8(l)+ O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+
O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+ O2(g)=8CO2(g)+9H2O(l) ΔH4
O2(g)=8CO2(g)+9H2O(l) ΔH4
③2N2(g)+6H2(g) 4NH3(g) ΔH5 N2(g)+3H2(g)
4NH3(g) ΔH5 N2(g)+3H2(g) 2NH3(g) ΔH6
2NH3(g) ΔH6
④CaCO3(s)=CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)=Ca(OH)2(s) ΔH8
⑤NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH9 HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) ΔH10
①H2(g)+F2(g)=2HF(g) ΔH1 H2(g)+Cl2(g)=2HCl(g) ΔH2
②C8H8(l)+
 O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+
O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+ O2(g)=8CO2(g)+9H2O(l) ΔH4
O2(g)=8CO2(g)+9H2O(l) ΔH4③2N2(g)+6H2(g)
 4NH3(g) ΔH5 N2(g)+3H2(g)
4NH3(g) ΔH5 N2(g)+3H2(g) 2NH3(g) ΔH6
2NH3(g) ΔH6④CaCO3(s)=CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)=Ca(OH)2(s) ΔH8
⑤NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH9 HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) ΔH10
| A.2项 | B.3项 | C.4项 | D.5项 |
您最近半年使用:0次
名校
2 . 下列依据热化学方程式得出的结论正确的是
| 选项 | 热化学方程式 | 结论 |
| A | H2(g)+Cl2(g)=2HCl(g) ΔH=-akJ·mol-1 | H2燃烧热的ΔH=-akJ·mol-1 |
| B | S(s)+O2(g)=SO2(g) ΔH=-2bkJ·mol-1 | 一定条件下,在密闭容器中1molS与0.5molO2充分反应,放出热量bkJ |
| C | C(s)+ O2(g)=CO(g) ΔH=-ckJ·mol-1 O2(g)=CO(g) ΔH=-ckJ·mol-1 | C燃烧热的ΔH=-ckJ·mol-1 |
| D | P4(s,白磷)=4P(s,红磷) ΔH=-dkJ·mol-1 | 相同条件下P(s,红磷)比P4(s,白磷) 稳定 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
3 . 下列化学反应的表示正确的是
A.尿素和 溶液在碱性条件下反应: 溶液在碱性条件下反应: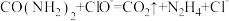 |
B.1-溴丙烷与氢氧化钠水溶液共热: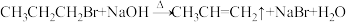 |
C.过量氨水和硫酸铜溶液反应: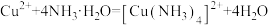 |
D.常温下 为液体,具有很高的燃烧热 为液体,具有很高的燃烧热 ,肼燃烧的热化学方程式: ,肼燃烧的热化学方程式: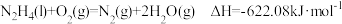 |
您最近半年使用:0次
名校
4 . 下列关于提高燃料利用率的做法不正确 的是
| A.回收利用烟道废气中的热能 | B.将煤块粉碎再燃烧 |
| C.用耐高温绝热材料砌筑炉膛 | D.减少空气鼓入量 |
您最近半年使用:0次
解题方法
5 . 依据叙述,按要求填空
(1)在25℃、101kPa下,1g甲醇(CH3OH液态)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________ 。
(2)11.2L(标准状况)H2在足量Cl2中燃烧生成HCl气体,放出91.5kJ热量,其热化学方程式:___________ 。
(3)已知1molC(石墨,s)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3kJ热量,请写出该反应的热化学方程式:___________ 。
(4)甲醛(HCHO)俗称蚁醛,是一种重要的化工原料。可通过以下方法将甲醇转化为甲醛。
脱氢法:CH3OH(g)=HCHO(g)+H2(g) △H1=+92.09kJ/mol
氧化法:CH3OH(g)+ O2(g)=HCHOg+H2O(g) △H2
O2(g)=HCHOg+H2O(g) △H2
已知:2H2(g)+O2(g)=2H2O(g) △H3=-483.64kJ/mol,则△H2=___________ 。
(1)在25℃、101kPa下,1g甲醇(CH3OH液态)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(2)11.2L(标准状况)H2在足量Cl2中燃烧生成HCl气体,放出91.5kJ热量,其热化学方程式:
(3)已知1molC(石墨,s)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3kJ热量,请写出该反应的热化学方程式:
(4)甲醛(HCHO)俗称蚁醛,是一种重要的化工原料。可通过以下方法将甲醇转化为甲醛。
脱氢法:CH3OH(g)=HCHO(g)+H2(g) △H1=+92.09kJ/mol
氧化法:CH3OH(g)+
 O2(g)=HCHOg+H2O(g) △H2
O2(g)=HCHOg+H2O(g) △H2已知:2H2(g)+O2(g)=2H2O(g) △H3=-483.64kJ/mol,则△H2=
您最近半年使用:0次
解题方法
6 . 下列说法错误的是
| A.需要加热才能发生的反应可能是吸热反应,也可能是放热反应 |
| B.已知4P(红磷,s)=P4(白磷,s) △H>0,则红磷比白磷稳定 |
| C.“冰,水为之,而寒于水”,说明相同质量的水和冰相比较,冰的能量低 |
| D.已知2H2(g)+O2(g)=2H2O(g) △H=-483.6.kJ/mol,则氢气的燃烧热为241.8kJ/mol |
您最近半年使用:0次
解题方法
7 . 工业上,常用水蒸气通过炽热的焦炭制得水煤气(主要成分为 和
和 ),其反应的化学方程式为
),其反应的化学方程式为 ,请回答下列问题:
,请回答下列问题:
(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是___________。
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是___________ 。
A.充入He使容器压强增大,能提高反应速率
B.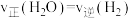 ,说明反应达到平衡状态
,说明反应达到平衡状态
C.容器中焦炭的质量不再变化,说明反应达到平衡状态
D.混合气体的密度不再发生改变时,反应达平衡状态
E.升高温度,能使正反应速率增大,逆反应速率减小
(3)298K时,1gH2燃烧生成H2O(g)放热121kJ,1molH2O(l)蒸发吸热44kJ,表示H2燃烧热的热化学方程式为___________ 。
(4)恒温下,将1molN2和3molH2置于体积为2L的密闭容器中进行反应N2+3H2⇌2NH3,若5min时测得氢气浓度为0.9mol/L,则用氨气表示5min内的化学反应速率为___________ ,N2的转化率为___________ ,欲提高合成氨的反应速率可采取的措施为___________ 。(任意答2点)
(5)工业制备硝酸过程中,通常对氨气进行催化氧化,其化学方程式为___________ 。
 和
和 ),其反应的化学方程式为
),其反应的化学方程式为 ,请回答下列问题:
,请回答下列问题:(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是___________。

| A.铝粉与氧化铁的反应 |
B.氯化铵与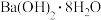 的反应 的反应 |
C.锌片与稀硫酸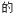 反应 反应 |
| D.钠与冷水的反应 |
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是
A.充入He使容器压强增大,能提高反应速率
B.
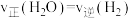 ,说明反应达到平衡状态
,说明反应达到平衡状态C.容器中焦炭的质量不再变化,说明反应达到平衡状态
D.混合气体的密度不再发生改变时,反应达平衡状态
E.升高温度,能使正反应速率增大,逆反应速率减小
(3)298K时,1gH2燃烧生成H2O(g)放热121kJ,1molH2O(l)蒸发吸热44kJ,表示H2燃烧热的热化学方程式为
(4)恒温下,将1molN2和3molH2置于体积为2L的密闭容器中进行反应N2+3H2⇌2NH3,若5min时测得氢气浓度为0.9mol/L,则用氨气表示5min内的化学反应速率为
(5)工业制备硝酸过程中,通常对氨气进行催化氧化,其化学方程式为
您最近半年使用:0次
名校
解题方法
8 . 25 ℃、101 kPa下,1g甲醇燃烧生成CO2和液态水时放热22.69 kJ,下列热化学方程式正确的是
| A.CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=726kJ·mol-1 |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1 452 kJ·mol-1 |
| C.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-726 kJ·mol-1 |
| D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=1 452 kJ·mol-1 |
您最近半年使用:0次
名校
9 . 已知下列反应:i.

ii.
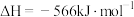
iii.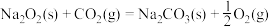

(1)CO的燃烧热
___________ 。
(2)根据上述信息,写出一氧化碳与过氧化钠在催化剂的作用下生成固体碳酸钠的热化学方程式___________ 。


ii.

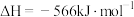
iii.
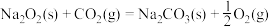

(1)CO的燃烧热

(2)根据上述信息,写出一氧化碳与过氧化钠在催化剂的作用下生成固体碳酸钠的热化学方程式
您最近半年使用:0次
名校
10 . 下列方程式书写正确的是
A.NaHSO4在水溶液中的电离方程式: |
B.甲烷燃烧热的热化学方程式: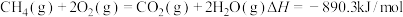 |
C.Na2CO3水解的离子方程式: |
D.CH3COONH4在水溶液中的电离方程式: |
您最近半年使用:0次



