解题方法
1 . 根据如下能量关系示意图,下列说法正确的是


A.1mol 与1mol 与1mol 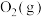 的能量之和为393.5kJ 的能量之和为393.5kJ |
B.反应 中,生成物的总能量大于反应物的总能量 中,生成物的总能量大于反应物的总能量 |
C.C的燃烧热的热化学方程式为: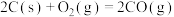  |
D.CO气体燃烧的热化学方程式为:  |
您最近一年使用:0次
解题方法
2 . 按要求填空:
(1)电解液态水制备1molO2(g),电解反应的ΔH =+572kJ·mol-1。请写出表示氢气燃烧热的热化学方程式___________ ;
(2)有机物M经过太阳光光照可转化成N,转化过程为: ΔH = +88.6kJ·mol-1。则M、N相比,较稳定的是
ΔH = +88.6kJ·mol-1。则M、N相比,较稳定的是___________ (填“M”或“N”),此反应逆反应活化能E逆=a kJ·mol-1,则正反应活化能为___________ (填含a的代数式)kJ·mol-1;
(3)K2Cr2O7溶液可通过调节pH改变颜色,原因___________ (用离子方程式表示);
(4)已知H3PO2是一种一元酸,写出它的正盐水解的离子方程式___________ 。
(1)电解液态水制备1molO2(g),电解反应的ΔH =+572kJ·mol-1。请写出表示氢气燃烧热的热化学方程式
(2)有机物M经过太阳光光照可转化成N,转化过程为:
 ΔH = +88.6kJ·mol-1。则M、N相比,较稳定的是
ΔH = +88.6kJ·mol-1。则M、N相比,较稳定的是(3)K2Cr2O7溶液可通过调节pH改变颜色,原因
(4)已知H3PO2是一种一元酸,写出它的正盐水解的离子方程式
您最近一年使用:0次
解题方法
3 . 下列说法与相关方程式书写均正确的是
A.NaHCO3溶于水会水解:HCO + H2O + H2O H3O+ + CO H3O+ + CO |
B.一定条件下的密闭容器中0.5molN2与过量H2充分反应,测得放出热量akJ:N2(g) + 3H2(g) 2NH3(g) ΔH= –2akJ·mol-1(a>0) 2NH3(g) ΔH= –2akJ·mol-1(a>0) |
C.HClO溶液显酸性:HClO + H2O ClO– + H3O+ ClO– + H3O+ |
D.硫的燃烧热ΔH=-315kJ·mol-1,硫燃烧的热化学方程式:S(g)+ O2(g) = SO3(g) ΔH= – 315kJ·mol-1 O2(g) = SO3(g) ΔH= – 315kJ·mol-1 |
您最近一年使用:0次
名校
解题方法
4 . 根据所学知识,完成下列问题。
(1)下列反应中,属于吸热反应的是___________ (填序号)。
a.灼热的炭与CO2反应 b.煅烧石灰石 c.铝与盐酸反应 d.盐酸与氢氧化钠反应
(2)已知CH4、CH3OH(l)的燃烧热分别为890.3kJ/mol,726.5kJ/mol,
①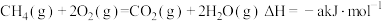 ,则a
,则a___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②写出表示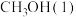 燃烧热的热化学方程式
燃烧热的热化学方程式___________ ;
(3)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,盐碱地呈碱性的原因:___________ (用离子方程式说明);
(4)水溶液是中学化学的重点研究对象、水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中水电离产生的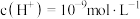 ,则该电解质可能是
,则该电解质可能是___________ (填序号)。
A. B.HCl C.
B.HCl C. D.
D. E.
E.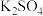
(5)联氨(N2H4)是一种应用广泛的化工原料,可用作火箭燃料。N2H4性质与NH3类似,在水中,N2H4是一种二元弱碱,请写出等物质的量N2H4与硫酸反应生成的盐的化学式为___________ 。
(1)下列反应中,属于吸热反应的是
a.灼热的炭与CO2反应 b.煅烧石灰石 c.铝与盐酸反应 d.盐酸与氢氧化钠反应
(2)已知CH4、CH3OH(l)的燃烧热分别为890.3kJ/mol,726.5kJ/mol,
①
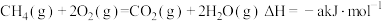 ,则a
,则a (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②写出表示
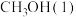 燃烧热的热化学方程式
燃烧热的热化学方程式(3)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,盐碱地呈碱性的原因:
(4)水溶液是中学化学的重点研究对象、水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中水电离产生的
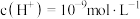 ,则该电解质可能是
,则该电解质可能是A.
 B.HCl C.
B.HCl C. D.
D. E.
E.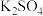
(5)联氨(N2H4)是一种应用广泛的化工原料,可用作火箭燃料。N2H4性质与NH3类似,在水中,N2H4是一种二元弱碱,请写出等物质的量N2H4与硫酸反应生成的盐的化学式为
您最近一年使用:0次
名校
5 . 下列有关热化学方程式书写与对应表述均正确的是
A.稀醋酸与稀NaOH溶液反应:  |
B.已知 , , ,则 ,则 |
C. 的燃烧热为 的燃烧热为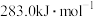 ,则 ,则 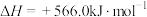 |
D.500℃、30MPa下,将0.5mol 和1.5mol 和1.5mol 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放出热量19.3kJ,其热化学方程式为 ,放出热量19.3kJ,其热化学方程式为 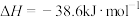 |
您最近一年使用:0次
6 . 下列说法或表达不正确 的是
A. 晶体和 晶体和 晶体反应是吸热反应 晶体反应是吸热反应 |
| B.101kPa时,1mol氢气完全燃烧生成液态水时所放出的热量称为氢气的燃烧热 |
C. 的水溶液能导电, 的水溶液能导电, 是电解质 是电解质 |
| D.我们可以利用溶液颜色变化与浓度变化之间的比例关系来测量反应速率 |
您最近一年使用:0次
解题方法
7 . 下列说法正确的是
A.甲烷的燃烧热为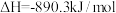 ,则甲烷燃烧的热化学方程式可表示为: ,则甲烷燃烧的热化学方程式可表示为: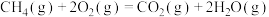 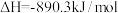 |
| B.进行中和热的测定实验时,用温度计测定HCl溶液的起始温度后,不需洗涤就可直接测定NaOH溶液的起始温度 |
C.500℃、30MPa下,将 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学方程式为: ,放热19.3kJ,其热化学方程式为: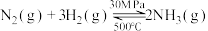 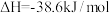 |
D.已知25℃、101KPa条件下: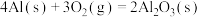 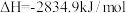 , , 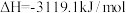 ,则 ,则 比 比 稳定 稳定 |
您最近一年使用:0次
名校
8 . 下列说法正确的是
A.甲烷的燃烧热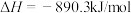 。则 。则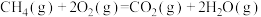 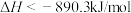 |
B.25℃ 时, 时,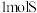 和 和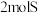 的燃烧热相等 的燃烧热相等 |
C.一定条件下,将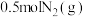 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,热化学方程式为: ,放热19.3kJ,热化学方程式为: 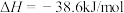 |
D.在稀溶液中: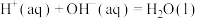 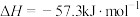 ,若将含 ,若将含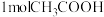 的醋酸稀溶液与含 的醋酸稀溶液与含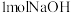 的稀溶液混合,放出的热量大于57.3kJ 的稀溶液混合,放出的热量大于57.3kJ |
您最近一年使用:0次
2023-12-04更新
|
136次组卷
|
4卷引用:浙江省绍兴市第一中学2023-2024学年高二上学期11月期中考试(平行班)化学试题
解题方法
9 . 回答下列问题:
(1)杭州亚运会火炬以丙烷( )为燃料,丙烷的燃烧热为2220kJ/mol,请写出丙烷燃烧热的热化学方程式:
)为燃料,丙烷的燃烧热为2220kJ/mol,请写出丙烷燃烧热的热化学方程式:_______ 。
(2)电化学方法是化工生产及生活中常用的一种方法。如图为用石墨作电极,在一定条件下电解饱和食盐水制取二氧化氯( )的装置图。
)的装置图。

①电极b应接电源的_______ (填“正”或“负”)极,图中应使用_______ (填“阴”或“阳”)离子交换膜。
②写出产生 一极的电极反应式:
一极的电极反应式:_______ 。
(3)如表所示25℃时某些弱酸的电离平衡常数。
①写出碳酸钠溶液中滴加少量草酸的离子方程式:_______ 。
②常温下,稀 溶液加水稀释过程中,下列数据变大的是
溶液加水稀释过程中,下列数据变大的是_______ 。
A. B.
B. C.
C. D.
D.
③25℃时,有 的一组醋酸、醋酸钠混合溶液,当溶液pH=3时,
的一组醋酸、醋酸钠混合溶液,当溶液pH=3时,
_______  。
。
(1)杭州亚运会火炬以丙烷(
 )为燃料,丙烷的燃烧热为2220kJ/mol,请写出丙烷燃烧热的热化学方程式:
)为燃料,丙烷的燃烧热为2220kJ/mol,请写出丙烷燃烧热的热化学方程式:(2)电化学方法是化工生产及生活中常用的一种方法。如图为用石墨作电极,在一定条件下电解饱和食盐水制取二氧化氯(
 )的装置图。
)的装置图。
①电极b应接电源的
②写出产生
 一极的电极反应式:
一极的电极反应式:(3)如表所示25℃时某些弱酸的电离平衡常数。
| 化学式 |  |  |  |
 |   | 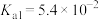  |  |
②常温下,稀
 溶液加水稀释过程中,下列数据变大的是
溶液加水稀释过程中,下列数据变大的是A.
 B.
B. C.
C. D.
D.
③25℃时,有
 的一组醋酸、醋酸钠混合溶液,当溶液pH=3时,
的一组醋酸、醋酸钠混合溶液,当溶液pH=3时,
 。
。
您最近一年使用:0次
解题方法
10 . 完成下列问题。
(1)除去 固体中混有
固体中混有 的方法(用化学方程式表示)
的方法(用化学方程式表示)___________ 。
(2)已知:常温下,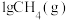 在足量的氧气中完全燃烧时放出55.6kJ热量,请写出表示
在足量的氧气中完全燃烧时放出55.6kJ热量,请写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:___________ 。
(3)25℃,某 溶液中
溶液中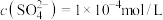 ,则该溶液中
,则该溶液中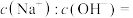
___________ 。
(4)判断 反应的自发性,并说明理由
反应的自发性,并说明理由___________ 。
(1)除去
 固体中混有
固体中混有 的方法(用化学方程式表示)
的方法(用化学方程式表示)(2)已知:常温下,
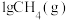 在足量的氧气中完全燃烧时放出55.6kJ热量,请写出表示
在足量的氧气中完全燃烧时放出55.6kJ热量,请写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:(3)25℃,某
 溶液中
溶液中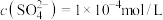 ,则该溶液中
,则该溶液中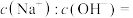
(4)判断
 反应的自发性,并说明理由
反应的自发性,并说明理由
您最近一年使用:0次



