1 . 生产、生活中的化学反应都伴随着能量的变化。回答下列问题:
(1) 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下:
 ,则常温下,
,则常温下, (单斜)与
(单斜)与 (斜方)中较稳定的是
(斜方)中较稳定的是______ [填“ (单斜)”或“
(单斜)”或“ (斜方)”]
(斜方)”]
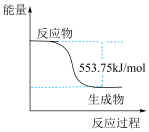
(2)丙烷( )常用作运动会火炬燃料。如图是一定量丙烷完全燃烧生成
)常用作运动会火炬燃料。如图是一定量丙烷完全燃烧生成 和
和 过程中的能量变化图。写出丙烷燃烧的热化学方程式:
过程中的能量变化图。写出丙烷燃烧的热化学方程式:______ ,丙烷的燃烧热( )为
)为_____ 。
(3)水煤气是由 和
和 组成的混合气体,在工业上常用作燃料。已知:
组成的混合气体,在工业上常用作燃料。已知: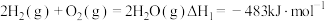 ;
; 。现取
。现取 (标准状况)水煤气,使其完全燃烧生成
(标准状况)水煤气,使其完全燃烧生成 和
和 ,测得反应共放热
,测得反应共放热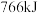 ,则水煤气中
,则水煤气中 与
与 的物质的量之比是
的物质的量之比是___ 。
(4)盖斯定律:不管化学过程是一步完成或分多步完成,整个过程的总热效应相同。
①反应 分两步进行:
分两步进行:
(ⅰ)
(ⅱ)
下列示意图中,能正确表示总反应过程中能量变化的是___ (填字母)。
A.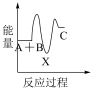 B.
B. 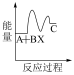 C.
C. 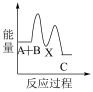 D.
D.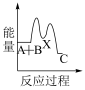
②已知:
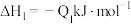

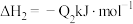


若将 液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为
液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为___  (用含
(用含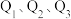 的代数式表示)。
的代数式表示)。
(5)下表中的数据表示断裂 化学键需消耗的能量(即键能,单位为
化学键需消耗的能量(即键能,单位为 ):
):
热化学方程式: ,则
,则 键的键能为
键的键能为______  。
。
(1)
 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下:
 ,则常温下,
,则常温下, (单斜)与
(单斜)与 (斜方)中较稳定的是
(斜方)中较稳定的是 (单斜)”或“
(单斜)”或“ (斜方)”]
(斜方)”](2)丙烷(
 )常用作运动会火炬燃料。如图是一定量丙烷完全燃烧生成
)常用作运动会火炬燃料。如图是一定量丙烷完全燃烧生成 和
和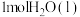 过程中的能量变化图。写出丙烷燃烧的热化学方程式:
过程中的能量变化图。写出丙烷燃烧的热化学方程式: )为
)为
(3)水煤气是由
 和
和 组成的混合气体,在工业上常用作燃料。已知:
组成的混合气体,在工业上常用作燃料。已知: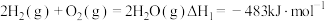 ;
; 。现取
。现取 (标准状况)水煤气,使其完全燃烧生成
(标准状况)水煤气,使其完全燃烧生成 和
和 ,测得反应共放热
,测得反应共放热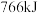 ,则水煤气中
,则水煤气中 与
与 的物质的量之比是
的物质的量之比是(4)盖斯定律:不管化学过程是一步完成或分多步完成,整个过程的总热效应相同。
①反应
 分两步进行:
分两步进行:(ⅰ)

(ⅱ)

下列示意图中,能正确表示总反应过程中能量变化的是
A.
 B.
B.  C.
C.  D.
D.
②已知:

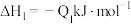

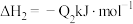


若将
 液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为
液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为 (用含
(用含 的代数式表示)。
的代数式表示)。(5)下表中的数据表示断裂
 化学键需消耗的能量(即键能,单位为
化学键需消耗的能量(即键能,单位为 ):
):| 化学键 |  |  |
| 键能 | 436 | 431 |
 ,则
,则 键的键能为
键的键能为 。
。
您最近一年使用:0次
2 . 已知:氢气的燃烧热为 ,碳的燃烧热为
,碳的燃烧热为 。下列说法正确的是
。下列说法正确的是
 ,碳的燃烧热为
,碳的燃烧热为 。下列说法正确的是
。下列说法正确的是A.氢气燃烧热的热化学方程式为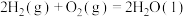 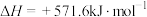 |
| B.标准状况下,22.4L氢气完全燃烧生成液态水放出热量285.8kJ |
C.反应 的 的 |
D.2.4g碳完全燃烧放出的热量为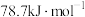 |
您最近一年使用:0次
名校
3 . 近年来,许多城市都全面禁止燃放烟花爆竹,爆竹中用到的炸药——黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为

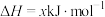
已知:碳的摩尔燃烧焓


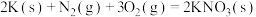

则x为

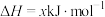
已知:碳的摩尔燃烧焓



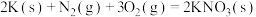

则x为
A.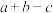 | B. | C.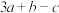 | D. |
您最近一年使用:0次
2024-03-03更新
|
195次组卷
|
3卷引用:安徽省蚌埠市五河致远实验学校 固镇汉兴学校2023-2024学年高二上学期11月期中联合考试化学试题
名校
解题方法
4 . 2023年7月全国首枚液氧甲烷火箭——朱雀二号在酒泉卫星发射基地发射成功。下列说法错误的是
| A.液态氧转化为气态氧是熵增的过程 |
| B.甲烷燃烧过程中反应物能量之和大于生成物能量之和 |
C.液氧甲烷燃料比 —偏二甲肼( —偏二甲肼( )燃料更环保 )燃料更环保 |
D.表示甲烷燃烧热的热化学方程式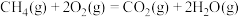 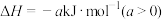 |
您最近一年使用:0次
名校
解题方法
5 . 下列推论正确的是
A.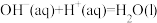 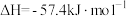 ,则含49g硫酸的稀硫酸与稀氨水完全反应,放出的热量小于57.4k ,则含49g硫酸的稀硫酸与稀氨水完全反应,放出的热量小于57.4k |
B.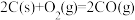 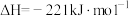 ,则碳的燃烧热 ,则碳的燃烧热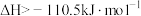 |
C.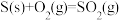  , ,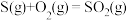  ,则 ,则 < < |
D.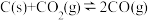 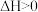 ,△S>0,则该反应在任何温度下都能自发进行 ,△S>0,则该反应在任何温度下都能自发进行 |
您最近一年使用:0次
名校
6 . 氢能是清洁能源之一,工业制取氢气涉及的重要反应之一是:

已知:①
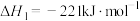
②
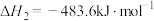
③
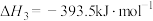
下列说法正确的是


已知:①

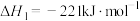
②

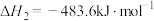
③

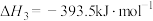
下列说法正确的是
A. 的燃烧热 的燃烧热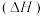 为 为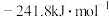 |
B. 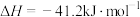 |
C.相比完全燃烧,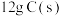 不完全燃烧生成 不完全燃烧生成 时损失的热量为 时损失的热量为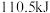 |
D. 的平衡常数表达式为 的平衡常数表达式为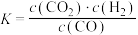 |
您最近一年使用:0次
名校
7 . Ⅰ.氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
(1)已知氨气的燃烧热为316.25kJ/mol,请写出氨气燃烧热的热化学方程式___________ 。
(2)根据下图数据计算反应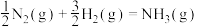 的
的
___________ 。

Ⅱ.用如图所示的装置测定中和反应反应热。

实验药品:50mL0.50mol/L盐酸、50mL0.50mol/L醋酸、100mL。0.55mol/LNaOH溶液。
(3)从实验装置上看;还缺少的重要仪器是___________ 。
(4)浓度0.55mol/L的碱溶液和浓度为 的酸溶液各50mL混合(溶液密度均为
的酸溶液各50mL混合(溶液密度均为 ),生成的溶液的比热容
),生成的溶液的比热容 ,测得温度如下:
,测得温度如下:
①

___________  ;
;
②某同学利用上述装置重新做甲组实验,测得反应热 偏大,则可能的原因是
偏大,则可能的原因是___________ (填序号)。
A.测完盐酸的温度计直接测NaOH溶液温度
B.用量筒量取酸和碱溶液的体积时均俯视读数
C.杯盖未盖严
D.NaOH溶液一次性迅速倒入
(1)已知氨气的燃烧热为316.25kJ/mol,请写出氨气燃烧热的热化学方程式
(2)根据下图数据计算反应
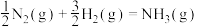 的
的

Ⅱ.用如图所示的装置测定中和反应反应热。

实验药品:50mL0.50mol/L盐酸、50mL0.50mol/L醋酸、100mL。0.55mol/LNaOH溶液。
(3)从实验装置上看;还缺少的重要仪器是
(4)浓度0.55mol/L的碱溶液和浓度为
 的酸溶液各50mL混合(溶液密度均为
的酸溶液各50mL混合(溶液密度均为 ),生成的溶液的比热容
),生成的溶液的比热容 ,测得温度如下:
,测得温度如下:| 反应物 | 起始温度 | 最高温度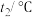 |
甲组( ) ) | 15.0 | 18.0 |
乙组( ) ) | 15.0 | 17.5 |


 ;
;②某同学利用上述装置重新做甲组实验,测得反应热
 偏大,则可能的原因是
偏大,则可能的原因是A.测完盐酸的温度计直接测NaOH溶液温度
B.用量筒量取酸和碱溶液的体积时均俯视读数
C.杯盖未盖严
D.NaOH溶液一次性迅速倒入
您最近一年使用:0次
名校
8 . 已知:各相关物质的燃烧热数据,如下表。
下列热化学方程式正确的是
| 物质 | C(s) |  |  |
燃烧热 /(kJ·mol-1) /(kJ·mol-1) | -393.5 | -1366.8 | -285.8 |
A.  kJ⋅mol-1 kJ⋅mol-1 |
B.  kJ⋅mol-1 kJ⋅mol-1 |
C.  kJ⋅mol-1 kJ⋅mol-1 |
D.  kJ⋅mol-1 kJ⋅mol-1 |
您最近一年使用:0次
2023-12-26更新
|
139次组卷
|
2卷引用:安徽省滁州中学2023-2024学年高二上学期期中考试化学试题
名校
9 . 已知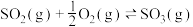 反应过程的能量变化如图所示:
反应过程的能量变化如图所示:
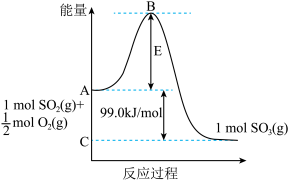
(1)由图可知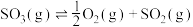 为
为___________ (填“吸热”或“放热”)反应。
(2)图中C点表示___________ 。E所代表的能量是___________ ;E的大小对该反应的反应热___________ (填“有”或“无”)影响。
(3)请求出反应
___________  。
。
(4)又知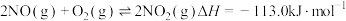 ,请根据题给条件求出反应
,请根据题给条件求出反应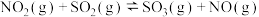 的焓变
的焓变
___________  。
。
(5)25℃、101 kP时,11g丙烷( )完全燃烧生成
)完全燃烧生成 和液态水时放出的热量是555.0 kJ,则表示丙烷燃烧热的热化学方程式是
和液态水时放出的热量是555.0 kJ,则表示丙烷燃烧热的热化学方程式是___________ 。
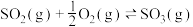 反应过程的能量变化如图所示:
反应过程的能量变化如图所示:
(1)由图可知
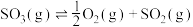 为
为(2)图中C点表示
(3)请求出反应

 。
。(4)又知
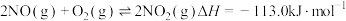 ,请根据题给条件求出反应
,请根据题给条件求出反应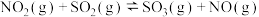 的焓变
的焓变
 。
。(5)25℃、101 kP时,11g丙烷(
 )完全燃烧生成
)完全燃烧生成 和液态水时放出的热量是555.0 kJ,则表示丙烷燃烧热的热化学方程式是
和液态水时放出的热量是555.0 kJ,则表示丙烷燃烧热的热化学方程式是
您最近一年使用:0次
2023-10-11更新
|
543次组卷
|
6卷引用:安徽省合肥卓越中学2023-2024学年高二上学期期中考试化学试题
解题方法
10 . 下列说法正确的是
A.已知 ,该反应为熵减小的反应 ,该反应为熵减小的反应 |
| B.氢氧化钠固体溶于水体系温度升高,是因为发生了放热反应 |
| C.甲烷燃烧放热,是因为破坏反应物化学键所需的能量特别大 |
D.已知乙醚的摩尔燃烧焓为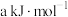 ,则表示乙醚摩尔燃烧焓的热化学方程式为: ,则表示乙醚摩尔燃烧焓的热化学方程式为: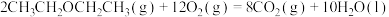 , , |
您最近一年使用:0次



