按要求填空:
(1)电解液态水制备1molO2(g),电解反应的ΔH =+572kJ·mol-1。请写出表示氢气燃烧热的热化学方程式___________ ;
(2)有机物M经过太阳光光照可转化成N,转化过程为: ΔH = +88.6kJ·mol-1。则M、N相比,较稳定的是
ΔH = +88.6kJ·mol-1。则M、N相比,较稳定的是___________ (填“M”或“N”),此反应逆反应活化能E逆=a kJ·mol-1,则正反应活化能为___________ (填含a的代数式)kJ·mol-1;
(3)K2Cr2O7溶液可通过调节pH改变颜色,原因___________ (用离子方程式表示);
(4)已知H3PO2是一种一元酸,写出它的正盐水解的离子方程式___________ 。
(1)电解液态水制备1molO2(g),电解反应的ΔH =+572kJ·mol-1。请写出表示氢气燃烧热的热化学方程式
(2)有机物M经过太阳光光照可转化成N,转化过程为:
 ΔH = +88.6kJ·mol-1。则M、N相比,较稳定的是
ΔH = +88.6kJ·mol-1。则M、N相比,较稳定的是(3)K2Cr2O7溶液可通过调节pH改变颜色,原因
(4)已知H3PO2是一种一元酸,写出它的正盐水解的离子方程式
更新时间:2024-01-29 14:25:36
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知一些烷烃的燃烧热如下表:
(1)热稳定性:正丁烷________ (填“>”或“<”)异丁烷。
(2)写出表示乙烷燃烧热的热化学方程式_____________________________________ 。
(3)相同物质的量的烷烃,碳原子数越多,燃烧放出的热量越_______ (填“多”或“少”)。
(4)有同学估计“正戊烷的燃烧热大约在3 540 kJ·mol−1左右”,你认为正确吗?______ 。理由是_______________________________________ 。
| 化合物 | 燃烧热/kJ·mol−1 | 化合物 | 燃烧热/kJ·mol−1 |
| 甲烷 | 891.0 | 正丁烷 | 2 878.0 |
| 乙烷 | 1 560.8 | 异丁烷 | 2 869.6 |
| 丙烷 | 2 221.5 | 异戊烷 | 3 531.3 |
(1)热稳定性:正丁烷
(2)写出表示乙烷燃烧热的热化学方程式
(3)相同物质的量的烷烃,碳原子数越多,燃烧放出的热量越
(4)有同学估计“正戊烷的燃烧热大约在3 540 kJ·mol−1左右”,你认为正确吗?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)已知C(s,石墨)═C(s,金刚石), ;则稳定性:金刚石
;则稳定性:金刚石___________ (填“>”或“<”)石墨。
(2)已知: ;
; ,则
,则
___________ (填“>”或“<”) 。
。
(3) 、
、 时,
时,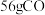 在足量的
在足量的 中充分燃烧,放出
中充分燃烧,放出 热量。则
热量。则 的燃烧热为
的燃烧热为
___________ 。
(4) 溶液与
溶液与 溶液完全反应,放出
溶液完全反应,放出 热量,该反应的中和热
热量,该反应的中和热
___________ 。
(5)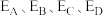 分别表示
分别表示 所具有的能量,则对于反应:
所具有的能量,则对于反应: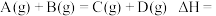
___________ (用含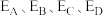 的代数式表示)。
的代数式表示)。
(6)合成氨反应的能量变化如下图所示,则反应
___________ 。

(1)已知C(s,石墨)═C(s,金刚石),
 ;则稳定性:金刚石
;则稳定性:金刚石(2)已知:
 ;
; ,则
,则
 。
。(3)
 、
、 时,
时,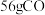 在足量的
在足量的 中充分燃烧,放出
中充分燃烧,放出 热量。则
热量。则 的燃烧热为
的燃烧热为
(4)
 溶液与
溶液与 溶液完全反应,放出
溶液完全反应,放出 热量,该反应的中和热
热量,该反应的中和热
(5)
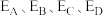 分别表示
分别表示 所具有的能量,则对于反应:
所具有的能量,则对于反应: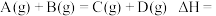
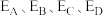 的代数式表示)。
的代数式表示)。(6)合成氨反应的能量变化如下图所示,则反应


您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活中的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:

ΔH=+88.6 kJ/mol则M、N相比,较稳定的是_____________ 。
(2)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(l)+1/2O2(g)=CO2(g)+2H2O(g) ΔH=-a kJ/mol,则a________ 238.6(填“>”“<”或“=”)。
(3)将Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:__________________________________ 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1 176 kJ/mol,则反应过程中,每转移1 mol电子放出的热量为________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:

ΔH=+88.6 kJ/mol则M、N相比,较稳定的是
(2)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(l)+1/2O2(g)=CO2(g)+2H2O(g) ΔH=-a kJ/mol,则a
(3)将Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1 176 kJ/mol,则反应过程中,每转移1 mol电子放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)298K时,1gH2燃烧生成H2O(g)放热121kJ,1molH2O(l)蒸发吸热44kJ,表示H2燃烧热的热化学方程式为___________ 。
(2)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
①直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g),∆H1=172kJ·mol-1,Kp1=1.0×10-2Pa
②碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g),∆H2=-51kJ·mol-1,Kp2=1.2×1012Pa
反应2C(s)+O2(g)=2CO(g)的∆H为___________ kJ·mol-1,Kp=___________ Pa。
(3)已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g),ΔH1=-1036kJ·mol-1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g),ΔH2=94kJ·mol-1
③2H2(g)+O2(g)=2H2O(g),ΔH3=-484kJ·mol-1
计算H2S热分解反应④2H2S(g)+O2(g)=S2(g)+2H2O(g)的ΔH4=___________ kJ·mol-1
(1)298K时,1gH2燃烧生成H2O(g)放热121kJ,1molH2O(l)蒸发吸热44kJ,表示H2燃烧热的热化学方程式为
(2)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
①直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g),∆H1=172kJ·mol-1,Kp1=1.0×10-2Pa
②碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g),∆H2=-51kJ·mol-1,Kp2=1.2×1012Pa
反应2C(s)+O2(g)=2CO(g)的∆H为
(3)已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g),ΔH1=-1036kJ·mol-1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g),ΔH2=94kJ·mol-1
③2H2(g)+O2(g)=2H2O(g),ΔH3=-484kJ·mol-1
计算H2S热分解反应④2H2S(g)+O2(g)=S2(g)+2H2O(g)的ΔH4=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.已知C、H2、CO的燃烧热的数据如表所示:
(1)写出C完全燃烧的热化学方程式:_____ 。
(2)能表示H2燃烧热的热化学方程式为____ 。
(3)现以H2或CO为燃料来提供热能,从热能的角度考虑,你认为最好选择__ (填写序号)。
A.H2 B.CO C.均可以
理由是___ 。
Ⅱ.已知下列热化学方程式:
①H2O(l)=H2(g)+ O2(g) ΔH=+285.8 kJ/mol
O2(g) ΔH=+285.8 kJ/mol
②H2(g)+ O2(g)=H2O(g) ΔH=-241.8 kJ/mol
O2(g)=H2O(g) ΔH=-241.8 kJ/mol
③NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ/mol
回答下列问题:
(4)上述反应中属于吸热反应的是___ (填序号)。
(5)燃烧10gH2生成液态水,放出的热量为___ 。
| 物质 | C | H2 | CO |
| ΔH/kJ·mol-1 | -393.5 | -285.8 | -283.0 |
(1)写出C完全燃烧的热化学方程式:
(2)能表示H2燃烧热的热化学方程式为
(3)现以H2或CO为燃料来提供热能,从热能的角度考虑,你认为最好选择
A.H2 B.CO C.均可以
理由是
Ⅱ.已知下列热化学方程式:
①H2O(l)=H2(g)+
 O2(g) ΔH=+285.8 kJ/mol
O2(g) ΔH=+285.8 kJ/mol②H2(g)+
 O2(g)=H2O(g) ΔH=-241.8 kJ/mol
O2(g)=H2O(g) ΔH=-241.8 kJ/mol③NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ/mol
回答下列问题:
(4)上述反应中属于吸热反应的是
(5)燃烧10gH2生成液态水,放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知下列热化学方程式:
①2H2(g) +O2(g) = 2H2O(l) △H = -571.6 kJ / mol
②C(s) + O2(g) = CO2(g) △H = -393.5 kJ / mol
③C(s) + H2O(g) = CO(g) + H2(g) △H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是__________ (填序号,下同),属于吸热反应的是__________ 。
(2)2g H2完全燃烧生成液态水,放出的热量为_____________ 。
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量,该反应的热化学方程式为_________________________________ 。
②已知HCN稀溶液与NaOH稀溶液反应生成1mol H2O时,放出12.1kJ热量,用离子方程式表示该反应的热化学方程为_______________________________________________ 。
③在25℃、101kpa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为________________________________________________ 。
①2H2(g) +O2(g) = 2H2O(l) △H = -571.6 kJ / mol
②C(s) + O2(g) = CO2(g) △H = -393.5 kJ / mol
③C(s) + H2O(g) = CO(g) + H2(g) △H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)2g H2完全燃烧生成液态水,放出的热量为
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量,该反应的热化学方程式为
②已知HCN稀溶液与NaOH稀溶液反应生成1mol H2O时,放出12.1kJ热量,用离子方程式表示该反应的热化学方程为
③在25℃、101kpa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐1】2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH= —99kJ·mol—1。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH= —99kJ·mol—1。请回答下列问题:
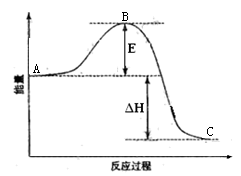
(1)图中A点表示_________ 。E的大小对该反应的反应热有无影响?________ 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________ ,理由是______________________________________ ;
(2)图中△H=_____________ kJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式
________________________________ ,_______________________________________ 。
 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH= —99kJ·mol—1。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH= —99kJ·mol—1。请回答下列问题:
(1)图中A点表示
(2)图中△H=
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据有关要求回答问题:
(1)如图是1mol NO2(g)和1mol CO(g)反应生成CO2和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是___ ,△H的变化是___ (填“增大”、“减小”、“不变”)。请写出NO2和CO反应的热化学方程式:___ 。

(2)以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。反应Ⅱ包含两步反应:

第一步:H2SO4(l)=SO3(g)+H2O(g) △H1=+177kJ/mol
第二步:2SO3(g)=2SO2(g)+O2(g) △H2=+196kJ/mol
①写出第一步反应自发进行的条件是:___ 。
②写出反应Ⅱ的热化学方程式:___ 。
(1)如图是1mol NO2(g)和1mol CO(g)反应生成CO2和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是

(2)以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。反应Ⅱ包含两步反应:

第一步:H2SO4(l)=SO3(g)+H2O(g) △H1=+177kJ/mol
第二步:2SO3(g)=2SO2(g)+O2(g) △H2=+196kJ/mol
①写出第一步反应自发进行的条件是:
②写出反应Ⅱ的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】
(1)在25℃、101kPa下, 1g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式:_______ 。
(2)2Zn(s)+O2(g)=2ZnO(s) ΔH1 =-702kJ/mol
2Hg(l)+O2(g)=2HgO(s) ΔH2 =-182kJ/mol
由此可知ZnO(s)+Hg(l)= Zn(s)+HgO(s) ΔH3=_______ 。
(3)已知 2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3的 ΔH=-99kJ·mol-1,请回答下列问题:
2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3的 ΔH=-99kJ·mol-1,请回答下列问题:
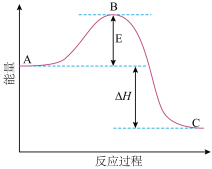
①图中A、C分别表示_______ 、_______ 。
②E的大小对该反应的反应热有无影响?_______ ,该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?_______ ,理由是_______ 。
③图中ΔH=_______ kJ/mol。
(1)在25℃、101kPa下, 1g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式:
(2)2Zn(s)+O2(g)=2ZnO(s) ΔH1 =-702kJ/mol
2Hg(l)+O2(g)=2HgO(s) ΔH2 =-182kJ/mol
由此可知ZnO(s)+Hg(l)= Zn(s)+HgO(s) ΔH3=
(3)已知 2SO2(g)+O2(g)
 2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3的 ΔH=-99kJ·mol-1,请回答下列问题:
2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3的 ΔH=-99kJ·mol-1,请回答下列问题:
①图中A、C分别表示
②E的大小对该反应的反应热有无影响?
③图中ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】NaHCO3溶液呈碱性的原因是 __________ (写出有关的离子方程式,下同),Al2(SO4)3溶液呈酸性的原因是 __________ 。将NaHCO3溶液跟Al2(SO4)3溶液混合,现象是 __________ ,相关反应的离子方程式是: __________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ、下列物质中:A.KI(s) B.C2H5OH(l) C.Cl2(g) D.CH3COOH(l) E.BaSO4(s) F.NaHSO4(s) G.石墨(s) H.蔗糖(s) I.NaOH(l)
(1)属于非电解质的是____________ (填序号,下同),属于强电解质的是____________ ,属于弱电解质的是____________ 。
(2)能直接导电的是________________ ,能溶于水,且水溶液能导电的是________________ 。
Ⅱ、 根据下列事实,完成相关的离子方程式或电离方程式
(1)Na2S溶液使酚酞显红色_________________________________ 。
(2)硫酸铝钾[明矾KAl(SO4)2·12H2O]可以作净水剂_______________________________ 。
(1)属于非电解质的是
(2)能直接导电的是
Ⅱ、 根据下列事实,完成相关的离子方程式或电离方程式
(1)Na2S溶液使酚酞显红色
(2)硫酸铝钾[明矾KAl(SO4)2·12H2O]可以作净水剂
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】常温下,某水溶液M中存在的粒子有Na+、A2-、HA-、H+、OH-、H2O和H2A.根据题意回答下列问题:
(1)H2A为_______ 酸(填“强”或“弱”),往H2A溶液中加水会使 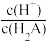 的值
的值_______ (填“增大”、“减小”或“不变”)。
(2)若M是由一种溶质组成的溶液,则M的溶质可以是Na2A或_______ 。
①Na2A的水溶液pH_______ (填“<”、“>”或“=”)7,原因是:_______ (用离子方程式表示)
②往Na2A溶液中加入_______ 可抑制其水解(选填字母序号)。
a.氯化铵固体 b.KOH固体 c. 水 d.升高温度
(1)H2A为
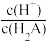 的值
的值(2)若M是由一种溶质组成的溶液,则M的溶质可以是Na2A或
①Na2A的水溶液pH
②往Na2A溶液中加入
a.氯化铵固体 b.KOH固体 c. 水 d.升高温度
您最近一年使用:0次



