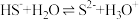下列说法与相关方程式书写均正确的是
A.NaHCO3溶于水会水解:HCO + H2O + H2O H3O+ + CO H3O+ + CO |
B.一定条件下的密闭容器中0.5molN2与过量H2充分反应,测得放出热量akJ:N2(g) + 3H2(g) 2NH3(g) ΔH= –2akJ·mol-1(a>0) 2NH3(g) ΔH= –2akJ·mol-1(a>0) |
C.HClO溶液显酸性:HClO + H2O ClO– + H3O+ ClO– + H3O+ |
D.硫的燃烧热ΔH=-315kJ·mol-1,硫燃烧的热化学方程式:S(g)+ O2(g) = SO3(g) ΔH= – 315kJ·mol-1 O2(g) = SO3(g) ΔH= – 315kJ·mol-1 |
更新时间:2024-01-29 14:25:31
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列离子方程式书写正确的是
A.碳酸钙与硝酸反应:CO32-+2H+ CO2↑+H2O CO2↑+H2O |
| B.铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑ |
| C.向NaHCO3溶液中加入过量的澄清石灰水:2HCO3﹣+Ca2++2OH﹣═CaCO3↓+2H2O+CO32﹣ |
| D.向明矾溶液中加入氢氧化钡溶液至SO42﹣恰好沉淀:Al3++2SO42﹣+2Ba2++4OH﹣═2BaSO4↓+AlO2﹣+2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列反应的离子方程式中,书写正确的是
| A.氢氧化铜与稀硫酸反应:OH-+H+===H2O |
| B.铁粉加入稀硫酸中:2Fe+6H+===2Fe3++3H2↑ |
| C.碳酸钙与醋酸反应:CaCO3+2H+===Ca2++CO2↑+H2O |
D.氯化铝溶液中加入过量氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关反应热的说法正确的是
| A.稀盐酸和稀氢氧化钠溶液反应的中和热△H= - 57.3kJ/mol,澄清石灰水与盐酸反应的中和热也为△H= - 57.3kJ/mol |
| B.H2(g)的燃烧热为285.8kJ/mol,则反应2H2O(g)=2H2(g)+O2(g)的△H=+571.6kJ/mol |
C.已知在一定条件下,N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol,则将3mol H2和足量的N2在此条件下充分反应,放出热量为92.4kJ 2NH3(g) △H=-92.4kJ/mol,则将3mol H2和足量的N2在此条件下充分反应,放出热量为92.4kJ |
| D.已知S(s) +O2(g) =SO2(g) △H1,S(g) +O2(g) =SO2(g) △H2则△H1<△H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
| A.甲烷燃烧热的数值为890.3kJ•mol﹣1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890.3kJ•mol﹣1 |
| B.500℃、30MPa 下,将 0.5mol N2 和 1.5mol H2 置于密闭的容器中充分反应生成NH3,放热 19.3kJ,其热化学方程式为: N2(g) +3 H2(g)500℃,30MPs 2NH3 (g) ∆H=- 38.6kJ/mol |
| C.已知 25℃、101KPa 条件下:4 Al(s)+3O2(g) =2 Al2O3(s) ∆H=- 284.9kJ/mol,4 Al(s)+2O3(g) =2 Al2O3(s) ∆H=- 319.1kJ/mo l, 则O3比O2稳定 |
| D.已知1mol金刚石转化为石墨,要放出1.895KJ的热能,1g石墨完全燃烧放出的热量比1g金刚石完全燃烧放出的热量少 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】人体血液里最主要的缓冲体系是碳酸氢盐缓冲体系 即为:
即为: 。下列判断正确的是( )
。下列判断正确的是( )
 即为:
即为: 。下列判断正确的是( )
。下列判断正确的是( )A.正常人血液内 |
B.人体血液里碳酸氢盐缓冲体系主要是维持血液中 和 和 的平衡 的平衡 |
C.血液中 的电离方程式为: 的电离方程式为: |
D.正常人血液中存在: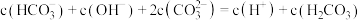 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是( )
| A.用惰性电极电解一定浓度的硫酸铜溶液,一段时间后,加入0.1molCu(OH)2后恰好恢复到电解前的浓度和pH,则电解过程中转移电子数为0.4mol |
| B.磷酸的电离方程式为:H3PO4=H++H2PO4- |
| C.电镀时保持电流恒定,升温可知加快反应速率 |
| D.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H>0 |
您最近一年使用:0次
【推荐1】天然海水中主要含有Na+、K+、Mg2+、Cl-、SO 、Br-、CO
、Br-、CO 、HCO
、HCO 等离子。火力发电时燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示:下列说法错误的是
等离子。火力发电时燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示:下列说法错误的是

 、Br-、CO
、Br-、CO 、HCO
、HCO 等离子。火力发电时燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示:下列说法错误的是
等离子。火力发电时燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示:下列说法错误的是
A.天然海水pH≈8的原因是由于海水中的CO 、HCO 、HCO 水解 水解 |
B.“氧化”是利用氧气将H2SO3、HSO 、SO 、SO 等氧化生成SO 等氧化生成SO |
| C.“反应、稀释”时加天然海水的目的是中和、稀释经氧化后海水中生成的酸 |
D.“排放”出来的海水中SO 的物质的量浓度与进入吸收塔的天然海水相同 的物质的量浓度与进入吸收塔的天然海水相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】 时,向
时,向 溶液中滴加
溶液中滴加 的
的 溶液,滴定曲线如图1,各种含磷微粒占含磷微粒总量的物质的量分数(
溶液,滴定曲线如图1,各种含磷微粒占含磷微粒总量的物质的量分数( )随
)随 变化关系如图2(已知a点的纵坐标为0.5)。下列说法正确的是
变化关系如图2(已知a点的纵坐标为0.5)。下列说法正确的是

 时,向
时,向 溶液中滴加
溶液中滴加 的
的 溶液,滴定曲线如图1,各种含磷微粒占含磷微粒总量的物质的量分数(
溶液,滴定曲线如图1,各种含磷微粒占含磷微粒总量的物质的量分数( )随
)随 变化关系如图2(已知a点的纵坐标为0.5)。下列说法正确的是
变化关系如图2(已知a点的纵坐标为0.5)。下列说法正确的是
| A.a点溶液显中性 |
B.B点溶液中存在关系: |
C.D点所加 溶液为 溶液为 ,则该点溶液中微粒浓度大小关系: ,则该点溶液中微粒浓度大小关系: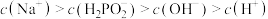 |
D.E点溶液中的水解离子方程式为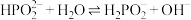 |
您最近一年使用:0次

 =PbSO4
=PbSO4 2Na+Cl2↑
2Na+Cl2↑ 7N2+12H2O
7N2+12H2O +2H2O
+2H2O +2I-+4H+
+2I-+4H+ 的
的 溶液与
溶液与 溶液的离子方程式:
溶液的离子方程式:
 水解的离子方程式:
水解的离子方程式: