1 . 完成下列填空:
(1) 水解的离子方程式为
水解的离子方程式为_______ ,在配制硫化钠溶液时可以加入少量的_______ (填化学式)以抑制其水解。
(2)硫酸铁水溶液呈_______ 性,原因是_______ 用离子方程式表示)。把 溶液蒸干灼烧,最后得到的主要固体产物是
溶液蒸干灼烧,最后得到的主要固体产物是_______ 。
(3)氢能是一种理想的绿色能源,有科学家预言,氢能有可能成为人类未来的主要能源。高纯氢的制备是目前的研究热点,包括氢的制备、储存和应用三个环节。
①适量 在
在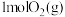 中完全燃烧,生成
中完全燃烧,生成 ,放出
,放出 的热量,请写出表示燃烧热的热化学方程式
的热量,请写出表示燃烧热的热化学方程式_______ 。
②与汽油相比,氢气作为燃料的有点是_______ 。
③下列反应均可获取 。
。
反应I:
反应II: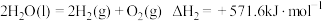
反应III: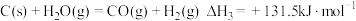
反应IV:
计算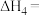
_______ 。
(1)
 水解的离子方程式为
水解的离子方程式为(2)硫酸铁水溶液呈
 溶液蒸干灼烧,最后得到的主要固体产物是
溶液蒸干灼烧,最后得到的主要固体产物是(3)氢能是一种理想的绿色能源,有科学家预言,氢能有可能成为人类未来的主要能源。高纯氢的制备是目前的研究热点,包括氢的制备、储存和应用三个环节。
①适量
 在
在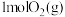 中完全燃烧,生成
中完全燃烧,生成 ,放出
,放出 的热量,请写出表示燃烧热的热化学方程式
的热量,请写出表示燃烧热的热化学方程式②与汽油相比,氢气作为燃料的有点是
③下列反应均可获取
 。
。反应I:

反应II:
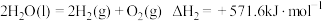
反应III:
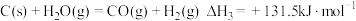
反应IV:

计算
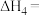
您最近一年使用:0次
2 . 生产、生活中的化学反应都伴随着能量的变化。回答下列问题:
(1) 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下:
 ,则常温下,
,则常温下, (单斜)与
(单斜)与 (斜方)中较稳定的是
(斜方)中较稳定的是______ [填“ (单斜)”或“
(单斜)”或“ (斜方)”]
(斜方)”]
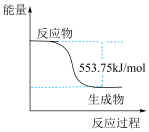
(2)丙烷( )常用作运动会火炬燃料。如图是一定量丙烷完全燃烧生成
)常用作运动会火炬燃料。如图是一定量丙烷完全燃烧生成 和
和 过程中的能量变化图。写出丙烷燃烧的热化学方程式:
过程中的能量变化图。写出丙烷燃烧的热化学方程式:______ ,丙烷的燃烧热( )为
)为_____ 。
(3)水煤气是由 和
和 组成的混合气体,在工业上常用作燃料。已知:
组成的混合气体,在工业上常用作燃料。已知: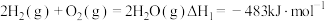 ;
; 。现取
。现取 (标准状况)水煤气,使其完全燃烧生成
(标准状况)水煤气,使其完全燃烧生成 和
和 ,测得反应共放热
,测得反应共放热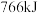 ,则水煤气中
,则水煤气中 与
与 的物质的量之比是
的物质的量之比是___ 。
(4)盖斯定律:不管化学过程是一步完成或分多步完成,整个过程的总热效应相同。
①反应 分两步进行:
分两步进行:
(ⅰ)
(ⅱ)
下列示意图中,能正确表示总反应过程中能量变化的是___ (填字母)。
A.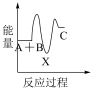 B.
B. 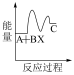 C.
C. 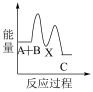 D.
D.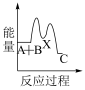
②已知:
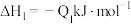

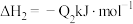


若将 液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为
液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为___  (用含
(用含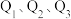 的代数式表示)。
的代数式表示)。
(5)下表中的数据表示断裂 化学键需消耗的能量(即键能,单位为
化学键需消耗的能量(即键能,单位为 ):
):
热化学方程式: ,则
,则 键的键能为
键的键能为______  。
。
(1)
 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下:
 ,则常温下,
,则常温下, (单斜)与
(单斜)与 (斜方)中较稳定的是
(斜方)中较稳定的是 (单斜)”或“
(单斜)”或“ (斜方)”]
(斜方)”](2)丙烷(
 )常用作运动会火炬燃料。如图是一定量丙烷完全燃烧生成
)常用作运动会火炬燃料。如图是一定量丙烷完全燃烧生成 和
和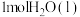 过程中的能量变化图。写出丙烷燃烧的热化学方程式:
过程中的能量变化图。写出丙烷燃烧的热化学方程式: )为
)为
(3)水煤气是由
 和
和 组成的混合气体,在工业上常用作燃料。已知:
组成的混合气体,在工业上常用作燃料。已知: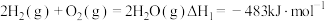 ;
; 。现取
。现取 (标准状况)水煤气,使其完全燃烧生成
(标准状况)水煤气,使其完全燃烧生成 和
和 ,测得反应共放热
,测得反应共放热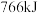 ,则水煤气中
,则水煤气中 与
与 的物质的量之比是
的物质的量之比是(4)盖斯定律:不管化学过程是一步完成或分多步完成,整个过程的总热效应相同。
①反应
 分两步进行:
分两步进行:(ⅰ)

(ⅱ)

下列示意图中,能正确表示总反应过程中能量变化的是
A.
 B.
B.  C.
C.  D.
D.
②已知:

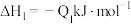

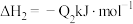


若将
 液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为
液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为 (用含
(用含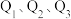 的代数式表示)。
的代数式表示)。(5)下表中的数据表示断裂
 化学键需消耗的能量(即键能,单位为
化学键需消耗的能量(即键能,单位为 ):
):| 化学键 |  |  |
| 键能 | 436 | 431 |
 ,则
,则 键的键能为
键的键能为 。
。
您最近一年使用:0次
解题方法
3 . 按题意要求填空:
(1)已知10g己烷完全燃烧生成液态水放出484kJ的热量,写出表示己烷燃烧热的热化学方程______________ 。
(2)已知在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:

则 全部被氧化成
全部被氧化成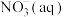 的热化学方程式为:
的热化学方程式为:_____________ 。
(3)化学键的键能是原子间形成(或断裂) 化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S:
化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S: ;S-S:
;S-S: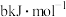 ;S=O:
;S=O: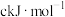 ;H-O:
;H-O: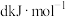 。
。
已知反应:
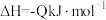 ,其反应产物中的固体
,其反应产物中的固体 实为
实为 ,实际分子是一个8元环状分子(即
,实际分子是一个8元环状分子(即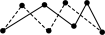 ),试根据这些数据计算已知反应的反应热:则Q=
),试根据这些数据计算已知反应的反应热:则Q=__________ (用a、b、c、d表示)。若已知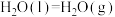
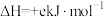 ,试写出
,试写出 和
和 反应生成
反应生成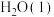 的热化学方程式为:
的热化学方程式为:_______ 。
(4)已知 (金刚石,s)
(金刚石,s)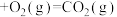
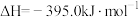
 (石墨,s)
(石墨,s)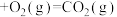
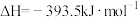
①石墨和金刚石相比,石墨的稳定性_______ 金刚石的稳定性。(填“大于”“小于”或“等于”,下同)
②石墨中 键键能
键键能_______ 金刚石中 键键能
键键能
(1)已知10g己烷完全燃烧生成液态水放出484kJ的热量,写出表示己烷燃烧热的热化学方程
(2)已知在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
则
 全部被氧化成
全部被氧化成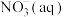 的热化学方程式为:
的热化学方程式为:(3)化学键的键能是原子间形成(或断裂)
 化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S:
化学键时释放(或吸收)的能量。以下是部分共价键键能数据:H-S: ;S-S:
;S-S: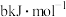 ;S=O:
;S=O: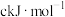 ;H-O:
;H-O: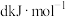 。
。已知反应:

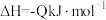 ,其反应产物中的固体
,其反应产物中的固体 实为
实为 ,实际分子是一个8元环状分子(即
,实际分子是一个8元环状分子(即 ),试根据这些数据计算已知反应的反应热:则Q=
),试根据这些数据计算已知反应的反应热:则Q=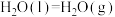
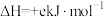 ,试写出
,试写出 和
和 反应生成
反应生成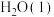 的热化学方程式为:
的热化学方程式为:(4)已知
 (金刚石,s)
(金刚石,s)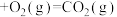
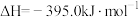
 (石墨,s)
(石墨,s)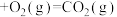
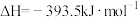
①石墨和金刚石相比,石墨的稳定性
②石墨中
 键键能
键键能 键键能
键键能
您最近一年使用:0次
4 . 已知:氢气的燃烧热为 ,碳的燃烧热为
,碳的燃烧热为 。下列说法正确的是
。下列说法正确的是
 ,碳的燃烧热为
,碳的燃烧热为 。下列说法正确的是
。下列说法正确的是A.氢气燃烧热的热化学方程式为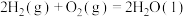 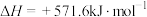 |
| B.标准状况下,22.4L氢气完全燃烧生成液态水放出热量285.8kJ |
C.反应 的 的 |
D.2.4g碳完全燃烧放出的热量为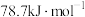 |
您最近一年使用:0次
5 . 下列说法正确的是
| A.1molH2SO4与1molBa(OH)2完全中和所放出的热量为中和热 |
| B.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,故反应一定是吸热反应 |
| C.强酸和强碱的稀溶液发生中和反应一定是放热反应,弱酸和弱碱反应一定也是放热反应 |
| D.酸和碱发生中和反应生成1mol水,这时的反应热叫中和热 |
您最近一年使用:0次
解题方法
6 . 以下几个热化学方程式,能表示燃烧热的热化学方程式是
| A.C(s)+1/2O2(g)=CO(g) ΔH = -110.5 kJ∙mol-1 |
| B.C(s)+O2(g)=CO2(g) ΔH = -393.5 kJ∙mol-1 |
| C.2H2(g)+O2(g)=2H2O(g) ΔH = -571.6 kJ∙mol-1 |
| D.H2(g)+1/2O2(g)=2H2O(g) ΔH = -241.8 kJ∙mol-1 |
您最近一年使用:0次
解题方法
7 . 大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据如下表:
则25℃时,6C(石墨,s)+3H2(g)=C6H6(l) △H=
| 物质 | H2(g) | C(石墨,s) | C6H6(l) |
| 燃烧热△H(kJ•mol-1) | -285.8 | -393.5 | -3267.5 |
| A.-30.9kJ/mol | B.+49.1kJ/mol | C.+104.7kJ/mol | D.-2588.2kJ/mol |
您最近一年使用:0次
解题方法
8 . 下列热化学方程式及有关应用的叙述中,正确的是
A. 的燃烧热为 的燃烧热为 ,则 ,则 燃烧的热化学方程式可表示为 燃烧的热化学方程式可表示为 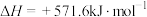 |
B.取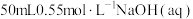 和 和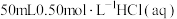 进行中和反应反应热的测定,用温度计测定 进行中和反应反应热的测定,用温度计测定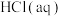 起始温度后,直接测定 起始温度后,直接测定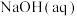 的温度,会使中和反应反应热 的温度,会使中和反应反应热 偏小 偏小 |
C.500℃、30MPa下,将 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学方程式为 ,放热19.3kJ,其热化学方程式为 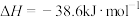 |
D.已知25℃、101KPa条件下: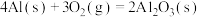  , ,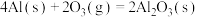 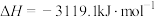 ,则 ,则 比 比 稳定 稳定 |
您最近一年使用:0次
9 . 一种物质的热值指的是“1g物质完全燃烧生成指定产物所放出的热量”,已知乙烷(结构简式为CH3CH3)的热值为52kJ/g。下列能够表示乙烷燃烧热的热化学方程式的是
A.CH3CH3(g)+ O2(g) =2CO2(g)+3H2O(l) ΔH= -52 kJ·mol-1 O2(g) =2CO2(g)+3H2O(l) ΔH= -52 kJ·mol-1 |
B.CH3CH3(g)+ O2(g) = 2CO2(g)+3H2O(g) ΔH= -1560 kJ·mol-1 O2(g) = 2CO2(g)+3H2O(g) ΔH= -1560 kJ·mol-1 |
C.CH3CH3(g)+ O2(g) = 2CO2(g)+3H2O(l) ΔH= -1560 kJ·mol-1 O2(g) = 2CO2(g)+3H2O(l) ΔH= -1560 kJ·mol-1 |
| D.2CH3CH3(g)+7O2(g) = 4CO2(g)+6H2O(l) ΔH= -3120 kJ·mol-1 |
您最近一年使用:0次
名校
10 . 下列热化学方程式书写正确的是
A. 甲烷完全燃烧生成 甲烷完全燃烧生成 和 和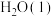 时放出 时放出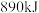 热量,它的热化学方程式为: 热量,它的热化学方程式为: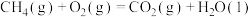 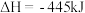 |
B.在200℃、 时, 时, 与碘蒸气作用生成 与碘蒸气作用生成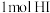 放出热量 放出热量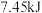 ,其热化学方程式为 ,其热化学方程式为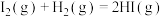  |
C. 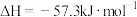 ,则 ,则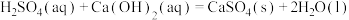 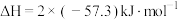 |
D.在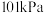 时, 时, 完全燃烧生成液态水,放出 完全燃烧生成液态水,放出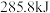 热量,则水分解的热化学方程式表示为: 热量,则水分解的热化学方程式表示为: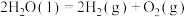  |
您最近一年使用:0次
2024-03-12更新
|
263次组卷
|
2卷引用:内蒙古自治区第二地质中学2023-2024学年高二上学期12月期中考试化学试题



