名校
解题方法
1 . 下列热化学方程式书写正确的是
A.甲烷的标准燃烧热为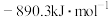 ,则甲烷燃烧的热化学方程式可表示为 ,则甲烷燃烧的热化学方程式可表示为 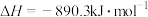 |
B.500℃、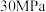 下,将 下,将 和 和 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 放热 放热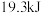 ,其热化学方程式为 ,其热化学方程式为 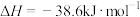 |
C.在 时, 时,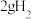 完全燃烧生成液态水,放出 完全燃烧生成液态水,放出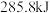 热量,氢气燃烧的热化学方程式表示为 热量,氢气燃烧的热化学方程式表示为 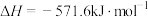 |
D.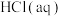 和 和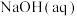 反应的中和热 反应的中和热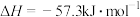 ,则稀 ,则稀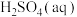 和 和 反应生成 反应生成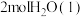 的反应热 的反应热 |
您最近一年使用:0次
2 . 依据图示关系,下列说法不正确的是
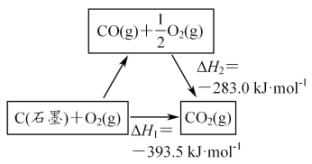

| A.C(石墨)的燃烧热为△H=—393.5kJ/mol |
| B.C(石墨)+CO2(g)= 2CO(g) △H=△H1—△H2 |
| C.1molC(石墨)和1 mol CO分别在足量O2中燃烧,全部转化为CO2,前者放热多 |
| D.化学反应的△H,只与反应体系的始态和终态有关,与反应途径无关 |
您最近一年使用:0次
名校
3 . 过氧乙酸(CH3CO3H)是一种广谱高效消毒剂,不稳定、易分解,高浓度易爆炸。常用于空气、器材的消毒,可由乙酸与H2O2在硫酸催化下反应制得,热化学方程式为:CH3COOH(aq)+H2O2(aq) CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
(1)利用上述反应制备760g CHCOH,放出的热量为_______ kJ。
(2)取质量相等的冰醋酸和50% H2O2溶液混合均匀,在一定量硫酸催化下进行如下实验。
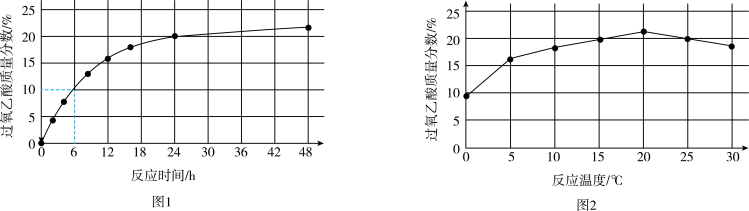
实验1:在25℃下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应(反应均未达到平衡),测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
 ①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=
①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=_____ g/h。(用含m的代数式表示)
②综合图1、图2分析,与20℃相比,25℃时过氧乙酸产率降低的可能原因是_______ (写出2条)。
(3)SV-1、SV-2是两种常用于实验研究的病毒,粒径分别为40nm和70nm。病毒在水中可能会聚集成团簇。不同pH下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
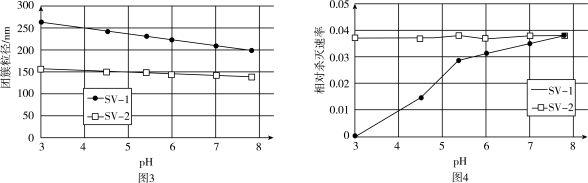
依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是___________ 。
 CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol
CH3CO3H(aq) + H2O(1) △H=-13.7kJ/mol(1)利用上述反应制备760g CHCOH,放出的热量为
(2)取质量相等的冰醋酸和50% H2O2溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在25℃下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应(反应均未达到平衡),测定24小时所得溶液中过氧乙酸的质量分数。数据如图2所示。
 ①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=
①实验1中,若反应混合液的总质量为m g,依据图1数据计算,在0~6h间,v(CH3CO3H)=②综合图1、图2分析,与20℃相比,25℃时过氧乙酸产率降低的可能原因是
(3)SV-1、SV-2是两种常用于实验研究的病毒,粒径分别为40nm和70nm。病毒在水中可能会聚集成团簇。不同pH下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。

依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是
您最近一年使用:0次
4 . 下列依据热化学方程式得出的结论正确的是
| A.已知C(s)+O2(g)=CO(g) ∆H=-akJmol-1,则1molC(s)完全燃烧放出的热大于akJ·mol-1 |
| B.已知SO2(g)+2H2S(g)=3S(s)+2H2O(l)常温下自发进行,则可推知一定∆H>0 |
| C.已知2H2(g)+O2(g)=2H2O(g) ∆H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ·mol-1 |
| D.已知C(石墨,s)=C(金刚石,s) ∆H>0,则金刚石比石墨稳定 |
您最近一年使用:0次
名校
5 . 氢能是清洁能源之一,工业制取氢气涉及的重要反应之一是:

已知:①
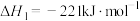
②
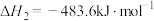
③
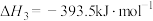
下列说法正确的是


已知:①

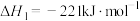
②

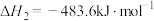
③

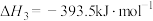
下列说法正确的是
A. 的燃烧热 的燃烧热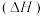 为 为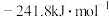 |
B. 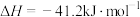 |
C.相比完全燃烧,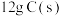 不完全燃烧生成 不完全燃烧生成 时损失的热量为 时损失的热量为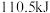 |
D. 的平衡常数表达式为 的平衡常数表达式为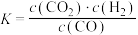 |
您最近一年使用:0次
名校
6 . Ⅰ.氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
(1)已知氨气的燃烧热为316.25kJ/mol,请写出氨气燃烧热的热化学方程式___________ 。
(2)根据下图数据计算反应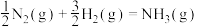 的
的
___________ 。

Ⅱ.用如图所示的装置测定中和反应反应热。

实验药品:50mL0.50mol/L盐酸、50mL0.50mol/L醋酸、100mL。0.55mol/LNaOH溶液。
(3)从实验装置上看;还缺少的重要仪器是___________ 。
(4)浓度0.55mol/L的碱溶液和浓度为 的酸溶液各50mL混合(溶液密度均为
的酸溶液各50mL混合(溶液密度均为 ),生成的溶液的比热容
),生成的溶液的比热容 ,测得温度如下:
,测得温度如下:
①

___________  ;
;
②某同学利用上述装置重新做甲组实验,测得反应热 偏大,则可能的原因是
偏大,则可能的原因是___________ (填序号)。
A.测完盐酸的温度计直接测NaOH溶液温度
B.用量筒量取酸和碱溶液的体积时均俯视读数
C.杯盖未盖严
D.NaOH溶液一次性迅速倒入
(1)已知氨气的燃烧热为316.25kJ/mol,请写出氨气燃烧热的热化学方程式
(2)根据下图数据计算反应
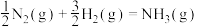 的
的

Ⅱ.用如图所示的装置测定中和反应反应热。

实验药品:50mL0.50mol/L盐酸、50mL0.50mol/L醋酸、100mL。0.55mol/LNaOH溶液。
(3)从实验装置上看;还缺少的重要仪器是
(4)浓度0.55mol/L的碱溶液和浓度为
 的酸溶液各50mL混合(溶液密度均为
的酸溶液各50mL混合(溶液密度均为 ),生成的溶液的比热容
),生成的溶液的比热容 ,测得温度如下:
,测得温度如下:| 反应物 | 起始温度 | 最高温度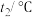 |
甲组( ) ) | 15.0 | 18.0 |
乙组( ) ) | 15.0 | 17.5 |


 ;
;②某同学利用上述装置重新做甲组实验,测得反应热
 偏大,则可能的原因是
偏大,则可能的原因是A.测完盐酸的温度计直接测NaOH溶液温度
B.用量筒量取酸和碱溶液的体积时均俯视读数
C.杯盖未盖严
D.NaOH溶液一次性迅速倒入
您最近一年使用:0次
7 . 下列说法正确的是
| A.需要加热才能发生的反应一定是吸热反应 |
| B.一定条件下石墨转化为金刚石的反应吸热,说明石墨比金刚石稳定 |
C.已知在 时, 时, 完全燃烧生成液态水,放出 完全燃烧生成液态水,放出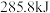 热量.则有关氢气燃烧热的热化学方程式为: 热量.则有关氢气燃烧热的热化学方程式为: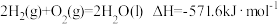 |
D.相同条件下,等质量的红磷蒸气和红磷固体分别完全燃烧,反应的热效应 |
您最近一年使用:0次
2024-01-02更新
|
285次组卷
|
3卷引用:湖北省部分高中联考协作体2023-2024学年高二上学期期中考试化学试题
名校
解题方法
8 . 已知充分燃烧一定质量的乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是
A. ; ;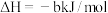 |
B. ; ; |
C. ; ;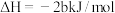 |
D. ; ; |
您最近一年使用:0次
2024-01-01更新
|
61次组卷
|
2卷引用:北京市西城外国语学校2023-2024学年高二上学期期中考试化学试题
名校
解题方法
9 . 载人飞船中通过如下过程实现 再生:
再生:
反应①: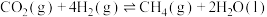
 kJ⋅mol
kJ⋅mol
反应②: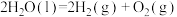
 kJ⋅mol
kJ⋅mol
下列说法正确的是
 再生:
再生:反应①:
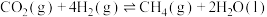
 kJ⋅mol
kJ⋅mol
反应②:
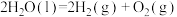
 kJ⋅mol
kJ⋅mol
下列说法正确的是
A. 的燃烧热 的燃烧热 kJ⋅mol kJ⋅mol |
B.反应 的 的 kJ⋅mol kJ⋅mol |
| C.反应①中反应物总能量低于生成物总能量 |
D.反应②的熵变 |
您最近一年使用:0次
名校
解题方法
10 . 下列热化学方程式书写正确的是
A.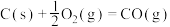  kJ⋅mol kJ⋅mol (燃烧热) (燃烧热) |
B.  kJ⋅mol kJ⋅mol (反应热) (反应热) |
C.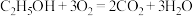  kJ⋅mol kJ⋅mol (反应热) (反应热) |
D. 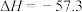 kJ⋅mol kJ⋅mol (反应热) (反应热) |
您最近一年使用:0次
2024-01-01更新
|
94次组卷
|
2卷引用:四川省甘孜藏族自治州泸定中学2023-2024学年高二上学期11月期中考试化学试题



