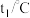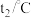名校
解题方法
1 . 肼( )是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。
)是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。 ,放出
,放出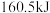 的热量,则该反应的热化学方程式为
的热量,则该反应的热化学方程式为_______ ,消耗 液态肼放出的热量为
液态肼放出的热量为_______ 。
(2)已知: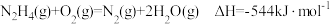 ,键能数据如下表:
,键能数据如下表:
则氮氮三键的键能为_______ ;若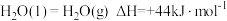 ,则
,则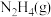 的燃烧热为
的燃烧热为_______ 。
(3)已知: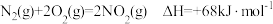 ,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为
,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为_______ 。
 )是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。
)是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。
 ,放出
,放出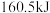 的热量,则该反应的热化学方程式为
的热量,则该反应的热化学方程式为 液态肼放出的热量为
液态肼放出的热量为(2)已知:
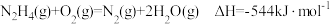 ,键能数据如下表:
,键能数据如下表:化学键 |
|
|
|
|
键能/( | 193 | 391 | 497 | 463 |
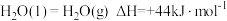 ,则
,则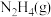 的燃烧热为
的燃烧热为(3)已知:
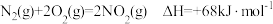 ,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为
,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为
您最近一年使用:0次
名校
2 . 下列化学反应表示正确的是
| A.NO2与水反应:NO2+H2O=2HNO3 |
B.铅蓄电池放电时的正极反应:Pb-2e-+ =PbSO4 =PbSO4 |
| C.甲烷的燃烧:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=890.3kJ·mol-1 |
D.SO2通入少量NaClO溶液中:SO2+ClO-+H2O= +Cl-+2H+ +Cl-+2H+ |
您最近一年使用:0次
名校
3 . 下列有关热化学方程式的说法正确的是
A.甲烷的燃烧热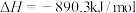 ,则甲烷燃烧的热化学方程式可表示为 ,则甲烷燃烧的热化学方程式可表示为 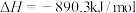 |
B.500℃、30MPa下,将 和 和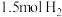 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学反应方程式为: ,放热19.3kJ,其热化学反应方程式为:  |
C.HCl和NaOH反应的中和热 ,则: ,则: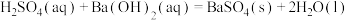 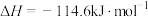 |
D.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 相同 相同 |
您最近一年使用:0次
名校
解题方法
4 . 化学反应中的能量变化,通常表现为热量的变化。从物质结构的角度看,化学反应的实质就是旧化学键的断裂和新化学键的形成,而旧化学键断裂所吸收的能量与新化学键形成所释放的能量不同导致发生了能量变化。下列说法错误的是
A.已知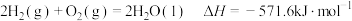 ,则H2的燃烧热 ,则H2的燃烧热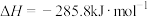 |
B.已知 ,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢时放出的热量大于270 kJ ,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢时放出的热量大于270 kJ |
C.已知 , , , ,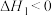 , , |
D.已知中和反应的反应热可表示为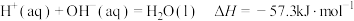 ,则1 mol H2SO4与1 mol Ba(OH)2完全反应放出的热量为114.6 kJ ,则1 mol H2SO4与1 mol Ba(OH)2完全反应放出的热量为114.6 kJ |
您最近一年使用:0次
名校
5 . 回答下列问题:
(1)科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知 和
和 的燃烧热
的燃烧热 分别为
分别为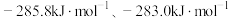 和-
和-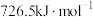 。请回答:
。请回答:
①用太阳能分解 水消耗的能量是
水消耗的能量是_______________ 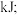
②甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_______________ 。
(2)热力学标准态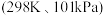 下,由稳定单质发生反应生成
下,由稳定单质发生反应生成 化合物的反应热叫该化合物的生成热
化合物的反应热叫该化合物的生成热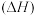 。如图为第VIA族元素(包括
。如图为第VIA族元素(包括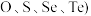 氢化物a、b、c、d的生成热数据示意图。试完成下列问题。
氢化物a、b、c、d的生成热数据示意图。试完成下列问题。 对应的氢化物是
对应的氢化物是_______________ (填化学式),结合元素周期律归纳非金属元素氢化物的稳定性与氢化物的生成热 的关系是:
的关系是:_______________ 。
②硒化氢在上述条件下发生分解反应的热化学方程式为_______________ 。
(沸点:硒化氢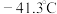 ;硒:
;硒: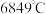 )
)
(3)某小组用 溶液和
溶液和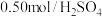 溶液进行中和热的测定。
溶液进行中和热的测定。
①取 溶液和
溶液和 溶液进行实验,实验数据如表所示。
溶液进行实验,实验数据如表所示。
近似认为 溶液和
溶液和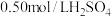 溶液的密度都是
溶液的密度都是 ,中和后混合溶液的比热容
,中和后混合溶液的比热容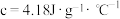 ,则
,则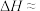
_________ (结果保留小数点后一位)。
②已知强酸强碱的稀溶液反应生成 液态
液态 时反应放出的热量为
时反应放出的热量为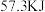 ,
,
上述实验产生偏差的原因可能是____________ (填字母)。
A.实验装置保温、隔热效果差
B.量取 溶液的体积时仰视读数
溶液的体积时仰视读数
C.把 溶液快速的一次性倒入盛有硫酸的量热计中
溶液快速的一次性倒入盛有硫酸的量热计中
D.用温度计测定 溶液起始温度后直接测定
溶液起始温度后直接测定 溶液的温度
溶液的温度
(1)科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知
 和
和 的燃烧热
的燃烧热 分别为
分别为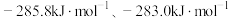 和-
和-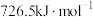 。请回答:
。请回答:①用太阳能分解
 水消耗的能量是
水消耗的能量是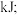
②甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(2)热力学标准态
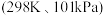 下,由稳定单质发生反应生成
下,由稳定单质发生反应生成 化合物的反应热叫该化合物的生成热
化合物的反应热叫该化合物的生成热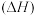 。如图为第VIA族元素(包括
。如图为第VIA族元素(包括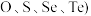 氢化物a、b、c、d的生成热数据示意图。试完成下列问题。
氢化物a、b、c、d的生成热数据示意图。试完成下列问题。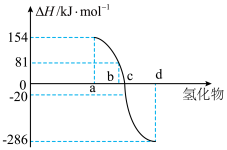
 对应的氢化物是
对应的氢化物是 的关系是:
的关系是:②硒化氢在上述条件下发生分解反应的热化学方程式为
(沸点:硒化氢
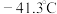 ;硒:
;硒: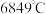 )
)(3)某小组用
 溶液和
溶液和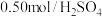 溶液进行中和热的测定。
溶液进行中和热的测定。①取
 溶液和
溶液和 溶液进行实验,实验数据如表所示。
溶液进行实验,实验数据如表所示。实验次数 | 起始温度 | 终止温度 | ||
|
| 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 29.9 |
2 | 27.0 | 27.4 | 27.2 | 33.3 |
3 | 26.3 | 26.1 | 26.2 | 30.2 |
 溶液和
溶液和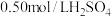 溶液的密度都是
溶液的密度都是 ,中和后混合溶液的比热容
,中和后混合溶液的比热容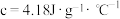 ,则
,则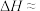
②已知强酸强碱的稀溶液反应生成
 液态
液态 时反应放出的热量为
时反应放出的热量为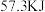 ,
,上述实验产生偏差的原因可能是
A.实验装置保温、隔热效果差
B.量取
 溶液的体积时仰视读数
溶液的体积时仰视读数C.把
 溶液快速的一次性倒入盛有硫酸的量热计中
溶液快速的一次性倒入盛有硫酸的量热计中D.用温度计测定
 溶液起始温度后直接测定
溶液起始温度后直接测定 溶液的温度
溶液的温度
您最近一年使用:0次
名校
6 . 已知C(s,石墨)、 、
、 的燃烧热依次为393.5 kJ⋅mol
的燃烧热依次为393.5 kJ⋅mol ,285.8 kJ⋅mol
,285.8 kJ⋅mol 、1299.5 kJ⋅mol
、1299.5 kJ⋅mol ,下列热化学方程式书写错误的是
,下列热化学方程式书写错误的是
 、
、 的燃烧热依次为393.5 kJ⋅mol
的燃烧热依次为393.5 kJ⋅mol ,285.8 kJ⋅mol
,285.8 kJ⋅mol 、1299.5 kJ⋅mol
、1299.5 kJ⋅mol ,下列热化学方程式书写错误的是
,下列热化学方程式书写错误的是A.C(s,石墨)  kJ⋅mol kJ⋅mol |
B.  kJ⋅mol kJ⋅mol |
C.  kJ⋅mol kJ⋅mol |
D.2C(s,石墨)  kJ⋅mol kJ⋅mol |
您最近一年使用:0次
7 . 下列有关说法正确的是
A.已知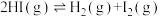 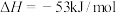 ,由此可知 ,由此可知 与 与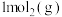 在密闭容器中充分反应后可以吸收26.5kJ的热量 在密闭容器中充分反应后可以吸收26.5kJ的热量 |
B.已知  ,则氢气的摩尔燃烧焓为: ,则氢气的摩尔燃烧焓为: |
C.已知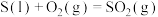  , ,  ,则 ,则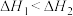 |
D. ,光照条件下的焓变 ,光照条件下的焓变 ,点燃条件下的焓变 ,点燃条件下的焓变 ,则 ,则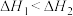 |
您最近一年使用:0次
名校
8 . 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答:
(1)在一定体积的恒容密闭容器中,进行如下化学反应: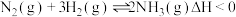 .
.
①反应过程中, 的值
的值________ (填“增大”、“减小”或“不能确定”);
②某温度下,在一个 的固定容器中充入
的固定容器中充入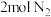 和
和 进行如下反应
进行如下反应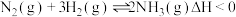 .一段时间达平衡后,
.一段时间达平衡后, 的转化率为
的转化率为 ,求平衡时
,求平衡时 的体积分数为
的体积分数为________ ;
(2)肼( )高效清洁的火箭燃料.
)高效清洁的火箭燃料. 气态肼在氧气中完全燃烧生成氮气和气态水,放出
气态肼在氧气中完全燃烧生成氮气和气态水,放出 热量,则肼燃烧的热化学方程式为
热量,则肼燃烧的热化学方程式为________________ ;
(3)金刚石、 具有优良的耐磨、耐腐蚀特性,应用广泛;
具有优良的耐磨、耐腐蚀特性,应用广泛;
①一定条件下,Na与 可制备金刚石,反应结束冷却至室温后,回收其中的
可制备金刚石,反应结束冷却至室温后,回收其中的 的实验操作名称为
的实验操作名称为________________ ;推测该反应的类型为________ (填标号);
A.分解反应 B.置换反应 C.氧化还原反应 D.离子反应
②已知: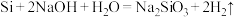 在高温电炉中碳和
在高温电炉中碳和 反应可制得
反应可制得 ,同时生成CO,其粗产品中杂质为Si和
,同时生成CO,其粗产品中杂质为Si和 ;
;
I.请写出电炉中所发生主反应的化学方程式________________ .每有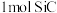 生成时,转移电子的数目为
生成时,转移电子的数目为________ ;
Ⅱ.现将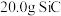 粗产品加入到过量的
粗产品加入到过量的 溶液中充分反应,收集到
溶液中充分反应,收集到 氢气,过滤得
氢气,过滤得 固体
固体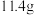 ,滤液稀释到
,滤液稀释到 ,则硅酸盐的物质的量浓度为
,则硅酸盐的物质的量浓度为________________ ;
③下列关于金刚石、 和单质Si的说法不正确的是
和单质Si的说法不正确的是________ (填标号);
A.金刚石、 和单质Si都属于无机非金属材料
和单质Si都属于无机非金属材料
B.金刚石和石墨、晶体硅和无定形硅分别互为同素异形体
C.金刚石和单质硅都是良好的半导体材料
(1)在一定体积的恒容密闭容器中,进行如下化学反应:
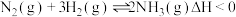 .
.①反应过程中,
 的值
的值②某温度下,在一个
 的固定容器中充入
的固定容器中充入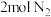 和
和 进行如下反应
进行如下反应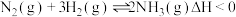 .一段时间达平衡后,
.一段时间达平衡后, 的转化率为
的转化率为 ,求平衡时
,求平衡时 的体积分数为
的体积分数为(2)肼(
 )高效清洁的火箭燃料.
)高效清洁的火箭燃料. 气态肼在氧气中完全燃烧生成氮气和气态水,放出
气态肼在氧气中完全燃烧生成氮气和气态水,放出 热量,则肼燃烧的热化学方程式为
热量,则肼燃烧的热化学方程式为(3)金刚石、
 具有优良的耐磨、耐腐蚀特性,应用广泛;
具有优良的耐磨、耐腐蚀特性,应用广泛;①一定条件下,Na与
 可制备金刚石,反应结束冷却至室温后,回收其中的
可制备金刚石,反应结束冷却至室温后,回收其中的 的实验操作名称为
的实验操作名称为A.分解反应 B.置换反应 C.氧化还原反应 D.离子反应
②已知:
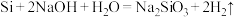 在高温电炉中碳和
在高温电炉中碳和 反应可制得
反应可制得 ,同时生成CO,其粗产品中杂质为Si和
,同时生成CO,其粗产品中杂质为Si和 ;
;I.请写出电炉中所发生主反应的化学方程式
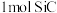 生成时,转移电子的数目为
生成时,转移电子的数目为Ⅱ.现将
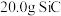 粗产品加入到过量的
粗产品加入到过量的 溶液中充分反应,收集到
溶液中充分反应,收集到 氢气,过滤得
氢气,过滤得 固体
固体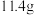 ,滤液稀释到
,滤液稀释到 ,则硅酸盐的物质的量浓度为
,则硅酸盐的物质的量浓度为③下列关于金刚石、
 和单质Si的说法不正确的是
和单质Si的说法不正确的是A.金刚石、
 和单质Si都属于无机非金属材料
和单质Si都属于无机非金属材料B.金刚石和石墨、晶体硅和无定形硅分别互为同素异形体
C.金刚石和单质硅都是良好的半导体材料
您最近一年使用:0次
名校
9 . 按要求书写方程式:
(1)工业合成氨每转移7.2mol电子放热112.8kJ,其热化学方程式为______ 。
(2)11.2g铁与2.7g水蒸气反应吸收30kJ热量,其热化学方程式为______ 。
(3)燃烧1.3g乙炔( )气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为
)气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为______ 。已知: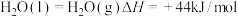 ,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是
,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是______ kJ。
(4)2.3g的 气体溶于水,放出akJ热量,其热化学方程式为
气体溶于水,放出akJ热量,其热化学方程式为______ 。
(5) 溶液中滴加硫酸,其离子方程式为
溶液中滴加硫酸,其离子方程式为______ 。
(6)工业上由黄铁矿制硫酸的第二步反应,其化学方程式为______ 。
(7)请用化学方程式解释,在无氧环境中才能观察到氢氧化亚铁沉淀颜色______ 。
(8)检验 的方法,其离子方程式为
的方法,其离子方程式为______ 。
(9)工业制漂白粉,其化学方程式为______ 。
(10)氨水与稀硫酸反应生成1mol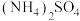 放热24.2kJ;已知
放热24.2kJ;已知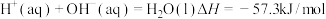 ,
, 电离的热化学方程式为
电离的热化学方程式为______ 。
(1)工业合成氨每转移7.2mol电子放热112.8kJ,其热化学方程式为
(2)11.2g铁与2.7g水蒸气反应吸收30kJ热量,其热化学方程式为
(3)燃烧1.3g乙炔(
 )气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为
)气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为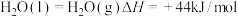 ,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是
,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是(4)2.3g的
 气体溶于水,放出akJ热量,其热化学方程式为
气体溶于水,放出akJ热量,其热化学方程式为(5)
 溶液中滴加硫酸,其离子方程式为
溶液中滴加硫酸,其离子方程式为(6)工业上由黄铁矿制硫酸的第二步反应,其化学方程式为
(7)请用化学方程式解释,在无氧环境中才能观察到氢氧化亚铁沉淀颜色
(8)检验
 的方法,其离子方程式为
的方法,其离子方程式为(9)工业制漂白粉,其化学方程式为
(10)氨水与稀硫酸反应生成1mol
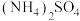 放热24.2kJ;已知
放热24.2kJ;已知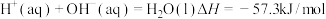 ,
, 电离的热化学方程式为
电离的热化学方程式为
您最近一年使用:0次
名校
10 . 下列热化学方程式及有关应用的叙述中,正确的是
A. 的燃烧热为 的燃烧热为 ,则 ,则 燃烧热的热化学方程式可表示为 燃烧热的热化学方程式可表示为 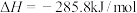 |
B.取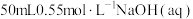 和 和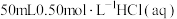 进行中和反应反应热的测定,用温度计测定 进行中和反应反应热的测定,用温度计测定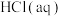 起始温度后,直接测定 起始温度后,直接测定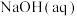 的温度,会使中和反应反应热 的温度,会使中和反应反应热 偏小 偏小 |
C.已知 、101KPa条件下: 、101KPa条件下: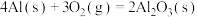  , ,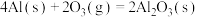 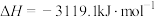 ,则 ,则 比 比 稳定 稳定 |
D. 、30MPa下,将 、30MPa下,将 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学方程式可表示为 ,放热19.3kJ,其热化学方程式可表示为 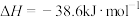 |
您最近一年使用:0次





 )
)