1 . 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理如下:
①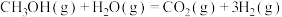
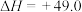 kJ⋅mol
kJ⋅mol
②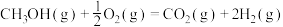
 kJ⋅mol
kJ⋅mol
下列说法正确的是
①
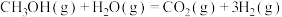
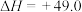 kJ⋅mol
kJ⋅mol
②
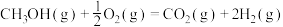
 kJ⋅mol
kJ⋅mol
下列说法正确的是

A. 的燃烧热 的燃烧热 kJ⋅mol kJ⋅mol |
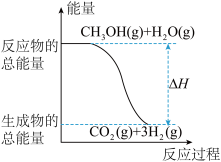
| B.反应①中的能量变化如图所示 |
C. 转变成 转变成 的过程一定要吸收能量 的过程一定要吸收能量 |
D.根据②推知反应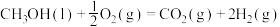  kJ⋅mol kJ⋅mol |
您最近一年使用:0次
2023-06-20更新
|
234次组卷
|
97卷引用:2011-2012学年吉林省油田高中高一下学期期初考试化学试卷
(已下线)2011-2012学年吉林省油田高中高一下学期期初考试化学试卷(已下线)2011-2012学年江西上饶中学高一零点、实验班下期末化学试卷(已下线)2012-2013学年河北省石家庄市第一中学高一下学期期中考试化学试卷2014-2015辽宁省沈阳市东北育才高一下学期第一次阶段考试化学试卷河北省石家庄市第一中学2016-2017学年高一下学期期中考试化学试题江苏省南京师范大学附属扬子中学、江浦高级中学两校2022-2023学年高一下学期联合调研化学试题安徽省安庆二中2022-2023学年高一下学期5月月考化学试题(已下线)2012届广西桂林十八中高三上学期第三次月考化学试卷(已下线)2012届辽宁省沈阳四校协作体高三上学期12月月考化学试卷(已下线)2011-2012学年四川省南山中学高二上学期期末模拟考试化学试卷(已下线)2011-2012学年黑龙江龙东地区高二第一学期高中教学联合体期末考试化学试卷(已下线)2011-2012学年甘肃兰州一中高二上学期期末考试化学试卷(已下线)2011-2012学年江苏省射阳中学高二上学期期末考试化学(选修)试卷(已下线)2012届吉林省吉林市高三上学期期末考试化学试卷(已下线)2011-2012天津南开中学高二第一学期期中考试理科化学试卷(已下线)2013-2014学年江西赣州市四所重点中学高二上学期期末联考化学试卷(已下线)2014年高考化学 题型八 能量变化型专题练习卷(已下线)2012届南京师大附中高三模拟考试试卷(十)化学试卷(已下线)2014-2015学年黑龙江安达市高级中学高二第一次月考试题化学试卷(已下线)2015届福建省安溪第八中学高三上学期期中质量检测化学试卷2014-2015江西省上高县二中高二上第三次月考化学试卷2014-2015四川省邛崃市高埂中学高二下学期第一次月考化学试卷2015-2016学年内蒙古奋斗中学高二上9月质检化学试卷2015-2016学年河南省南阳部分高中高二上学期第一次联考化学试卷2015-2016学年陕西省镇安中学高二上期中质检化学试卷2016届河北省行唐启明中学高三上学期12月月考化学试卷2015-2016学年江西省樟树中学、高安二中高二上期中联考化学试卷2015-2016学年宁夏育才中学高二上期末考试化学试卷2016-2017学年四川省成都外国语学校高二上10月月考化学试卷2016-2017学年广东佛山一中高二上第一次段考化学卷2016-2017学年贵州省思南中学高二上半期考试化学卷2016-2017学年山西省大同一中高二上期中化学试卷2016-2017学年浙江省温州市十校联合体高二上期末化学试卷2016-2017学年湖南省长沙市第一中学高二下学期第一次模块检测化学试卷2017届江苏省南通市高三高考全真模拟(五)化学 试卷吉林省延边安图第一中学2016-2017学年高二练习化学试题河北省景县中学2017-2018学年高二开学摸底考试化学试题江苏省盐城中学2018届高三上学期第一次阶段性考试化学试题安徽省江淮名校2017-2018学年高二期中考试化学试题江苏省盐城市阜宁县2017-2018学年高二上学期期中考试化学(选修)试题河南省中原名校(即豫南九校)2017-2018学年高二上学期第二次联考化学试题浙江省温州市“十五校联合体”2017-2018学年高二上学期期末考试化学试题高二化学(人教版)选修四专题同步练习卷:燃烧热 能源2018-2019学年人教版高中化学选修四 章末综合测评1 化学反应与能量【全国百强校】海南省海南中学2017-2018学年高二(理)上学期期末考试化学试题【全国百强校】河北省武邑中学2018-2019学年高二上学期第二次月考化学试题【市级联考】四川省达州市2018-2019学年高二上学期期末检测化学试题山西省晋中市平遥县第二中学2019-2020学年高二10月月考化学试题辽宁省六校协作体2020届高三上学期初考化学试题(已下线)考点08 化学反应中的能量变化——《备战2020年高考精选考点专项突破题集》湖南省常德市石门县第二中学2019-2020学年高二上学期第二次月考化学试题四川省绵阳市三台县芦溪中学2017-2018学年高二上学期第五次月考化学试题海南省海口市第四中学2019-2020学年高二上学期期末考试化学试题2020年春季人教版高中化学选修4第一章《化学反应与能量》测试卷江苏省淮安市涟水县第一中学2020届高三上学期第二次月考化学试题云南省昆明市寻甸县民族中学2019-2020学年高二下学期第一次月考化学试题山西省临猗县临晋中学2020-2021学年高二9月月考化学试题江西省南昌市第十中学2020-2021学年高二上学期第一次月考化学试题人教版(2019)高二选择性必修第一册 第一章 化学反应的热效应 第一节 反应热1山东省济南市山东师范大学附属中学2020-2021学年高二上学期10月学业质量检测化学试题(已下线)【南昌新东方】7. 南昌十中 徐钢 刘惠文.山东省莱州市第一中学2020-2021学年高二上学期10月月考化学试题人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 过模拟 2年模拟精编精练安徽省广德县实验中学2020-2021学年高二上学期10月月考化学试题河南省郑州市第106中学2020-2021学年高二上学期9月月考化学(理)试题四川省射洪中学校2020-2021学年高二上学期第二次月考化学试题甘肃省天水市武山县三校2020-2021学年高二上学期期中联考化学试题 河南省长垣市第十中学2020-2021学年高二上学期第二次月考化学试题广西玉林市普通中学2020-2021学年高二下学期月考化学试题江苏省盐城市阜宁中学2017-2018学年高二上学期期中考试化学(选修)试题选择性必修1(SJ)专题1第一单元专项拓展训练1 利用盖斯定律书写热化学方程式及反应焓变的相关计算四川省凉山州西昌天立学校高2021-2022学年高二上学期入学考试化学试题山东省滕州市第五中学2021-2022学年高二上学期第一次单元测试化学试题山东省德州市夏津第一中学2021-2022学年高二上学期第一次月考化学试卷(已下线)专题18 化学反应与能量(限时精练)-2022年高三毕业班化学常考点归纳与变式演练黑龙江省大庆市东风中学2021-2022学年高三上学期10月质量检测化学试题黑龙江省哈尔滨市德强高中2021-2022学年高二上学期期中考试化学试题第一节 反应热 第2课时 热化学方程式 燃烧热甘肃省兰州市西固区三校2021-2022学年高二上学期期中联考化学(理科)试题安徽省滁州市定远县育才学校2021-2022学年高二上学期期末考试(实验班)化学试题山东省德州市陵城区祥龙高级中学2022-2023学年高二上学期9月月考化学试题安徽省芜湖市无为襄安中学2022-2023高二上学期第一次月考化学试题黑龙江省哈尔滨市第三中学2022-2023学年高二上学期第二次验收化学试题天津市第二中学2022-2023学年高二上学期第一次月考化学试题河北省石家庄市第二十一中学2022-2023学年高二上学期十月月考化学试题四川省广元市八二一中学2021-2022学年高二上学期期中考试化学试题陕西宝鸡市眉县槐芽中学2022-2023学年高二上学期期中考试化学试题北京市顺义牛栏山第一中学2022-2023学年高二上学期10月月考化学试题贵州省贵阳市花溪第六中学2021-2022学年高二上学期月考化学试题吉林省长春市实验中学2022-2023学年高二上学期期末考试化学试题湖南省长沙市芙蓉高级中学2022-2023学年高二上学期期中考试化学试题广东省东莞市众美中学2022-2023学年高三上学期10月月考化学试题辽宁省辽东南协作校2023-2024学年高二上学期10月月考化学试题宁夏回族自治区石嘴山市第三中学2023-2024学年高二9月月考化学试题黑龙江省齐齐哈尔市普高联谊校2023-2024学年高三上学期11月月考化学试题广东省深圳市南山为明学校2023-2024学年高二上学期期中考试化学试题(已下线)化学反应的热效应
名校
2 . 已知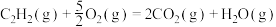
 kJ/mol,下列说法正确的是
kJ/mol,下列说法正确的是
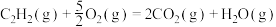
 kJ/mol,下列说法正确的是
kJ/mol,下列说法正确的是A.乙炔( )的燃烧热为1256 kJ/mol )的燃烧热为1256 kJ/mol |
B.若转移10 mol电子,则消耗2.5 mol  |
C.若生成2 mol液态水,则 kJ/mol kJ/mol |
| D.若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ |
您最近一年使用:0次
2023-06-20更新
|
233次组卷
|
3卷引用:安徽省安庆二中2022-2023学年高一下学期5月月考化学试题
名校
解题方法
3 . 下列关于燃烧热的描述中不正确的是
| A.化学方程式前的化学计量数扩大,燃烧热也相应扩大 |
B.CO(g)的燃烧热是283.0 ,则 ,则 反应的 反应的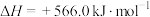 |
| C.1mol石墨和3mol石墨的燃烧热相等 |
D.表示 燃烧热的热化学方程式为: 燃烧热的热化学方程式为: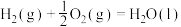 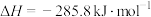 |
您最近一年使用:0次
名校
4 . 下列有关热化学方程式的书写和叙述正确的是
A.已知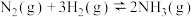  ,则在一定条件下向密闭容器中充入0.5mol ,则在一定条件下向密闭容器中充入0.5mol  (g)和1.5mol (g)和1.5mol  (g)充分反应后放出46.1kJ的热量 (g)充分反应后放出46.1kJ的热量 |
B.根据热化学方程式  ,我们可知:1mol ,我们可知:1mol  (g)所具有的能量小于1mol S(s)与1mol (g)所具有的能量小于1mol S(s)与1mol  (g)所具有的能量之和 (g)所具有的能量之和 |
C.CuCl(s)与 (g)反应生成 (g)反应生成 (s)和CuO(s)。在25℃、101kPa下,已知该反应每消耗1mol CuCl(s),放热44.4kJ,则该反应的热化学方程式是: (s)和CuO(s)。在25℃、101kPa下,已知该反应每消耗1mol CuCl(s),放热44.4kJ,则该反应的热化学方程式是:   |
D.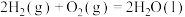 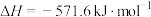 ,表示2个氢分子完全燃烧生成液态水时放出571.6kJ的热量 ,表示2个氢分子完全燃烧生成液态水时放出571.6kJ的热量 |
您最近一年使用:0次
2023-06-17更新
|
262次组卷
|
2卷引用:河北省张家口市尚义县第一中学2022-2023学年高一下学期6月月考化学试题
名校
解题方法
5 . 下列说法正确的是
| A.化合反应全都是放热反应,分解反应全都是吸热反应 |
| B.燃烧热是指1 mol任何物质完全燃烧生成稳定氧化物所放出的热量 |
C.由C(石墨)→C(金刚石) 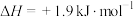 可知,金刚石比石墨稳定 可知,金刚石比石墨稳定 |
| D.若可逆反应的正反应为吸热反应,则相同条件下其逆反应一定是放热反应 |
您最近一年使用:0次
6 . 下列说法正确的是
| A.若2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ∆H=-1478kJ•mol-1,则CH3OH(l)的燃烧热为739kJ•mol-1 |
| B.S(g)+O2(g)=SO2(g) ∆H1,S(s)+O2(g)=SO2(g) ∆H2;∆H1<∆H2 |
| C.已知H+(aq)+OH-(aq)=H2O(l) ∆H=-57.3kJ•mol-1,则20.0gNaOH固体与稀盐酸完全中和,放出28.65kJ的热量 |
| D.Ba(OH)2•8H2O与NH4Cl常温下即可反应,因此该反应为放热反应 |
您最近一年使用:0次
解题方法
7 . 下列有关说法正确的是
A.已知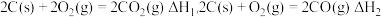 ,则 ,则 |
B.已知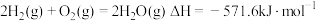 ,则 ,则 的燃烧热为 的燃烧热为 |
C.已知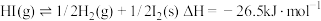 ,由此可知,在密闭容器中充入 ,由此可知,在密闭容器中充入 气体,充分分解后可以放出 气体,充分分解后可以放出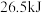 的热量 的热量 |
D. 和 和 反应中和热: 反应中和热: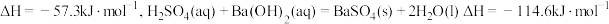 |
您最近一年使用:0次
8 . 下列反应属于吸热反应的是
| A.氢气燃烧 | B.煅烧石灰石 | C.酸碱中和反应 | D.黑火药爆炸 |
您最近一年使用:0次
9 . 下列有关说法正确的是
A.已知HI(g)  H2(g)+ H2(g)+ I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量 I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量 |
| B.已知2H2(g)+O2(g)=2H2O(g) ΔH= -571.6 kJ·mol-1,则氢气的燃烧热为ΔH= -285.8 kJ·mol-1 |
| C.已知2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2 |
| D.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH=-57.4 kJ·mol-1 |
您最近一年使用:0次
2023-06-06更新
|
1837次组卷
|
31卷引用:湖北省武汉市第十一中学2019-2020学年高一下学期期中测试化学试题
湖北省武汉市第十一中学2019-2020学年高一下学期期中测试化学试题广东省广州大学附属中学2019-2020学年高一下学期期末考试化学试题广东省广州大学附属中学等三校2019~2020学年高一下学期期末联考化学试题辽宁省大连市一0三中学2020-2021学年高一4月月考化学试题四川省南充市李渡中学2020-2021学年高一下学期期中考试化学试题黑龙江省大庆铁人中学2022-2023学年高一下学期期中考试化学试题陕西省宝鸡市金台区2022-2023学年高一下学期期末考试化学试题【全国百强校】四川省成都市石室中学2018-2019学年高二上学期期中考试化学试题湖南省长沙市明德中学2019-2020学年高二下学期第一次月考化学试题河南省南阳市第一中学2019-2020学年高二下学期第三次月考(6月)化学试题(已下线)1.1.2 热化学方程式 燃烧热(练习)——2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)(已下线)1.3.2 反应热的计算(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)第一章 化学反应与能量(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)1.3.1+盖斯定律-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)山东省德州市夏津第一中学2020-2021学年高二上学期9月月考化学试题江西省南昌县莲塘第三中学2020-2021学年高二上学期期中考试化学试题江西省赣州市会昌县第五中学2020-2021学年高二上学期第一次月考化学试题吉林省延边第二中学2020-2021学年高二上学期第二次考试月考化学试题重庆市朝阳中学2021-2022学年高二10月月考化学试题广西贵港市江南中学2021-2022学年高二上学期12月月考化学(理科)试题甘肃省甘南藏族自治州舟曲县第一中学2021-2022学年高二上学期期中考试化学试题云南省富源县第一中学2020-2021学年高二上学期第一次统测化学试题黑龙江省大兴安岭呼玛县高级中学2021-2022学年高二上学期期末考试化学试题吉林省汪清县第六中学2021-2022学年高二12月月考化学试题内蒙古赤峰市第四中学分校2021-2022学年高二上学期9月月考化学试题(已下线)考点巩固卷07 化学反应与能量(3大考点45题)-2024年高考化学一轮复习考点通关卷(新高考通用)黑龙江省佳木斯市第一中学2023-2024学年高二上学期10月月考化学试题河南省商丘市第一高级中学2023-2024学年高三上学期10月份月考化学试题江西省宜春市上高二中2023-2024学年高二上学期第一次月考化学试题陕西省汉中市乡县第一中学2023-2024学年高二上学期10月月考化学试题广东省深圳市罗湖外语学校2023-2024学年高二上学期期中考试化学试题
名校
解题方法
10 . 研究化学反应中的能量变化具有重要意义:
Ⅰ.写出下列反应的热化学方程式
(1)1mol (g)在
(g)在 中完全燃烧生成
中完全燃烧生成 和液态水,放出1299.6kJ的热量
和液态水,放出1299.6kJ的热量___________ 。
(2)23g (l)在
(l)在 中完全燃烧生成
中完全燃烧生成 和液态水,放出683.4kJ的热量
和液态水,放出683.4kJ的热量________ 。
Ⅱ.50 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热。回答下列问题:

(3)从实验装置上看,图中尚缺少的一种玻璃仪器是___________ 。
(4)隔热层的作用是___________ 。
(5)倒入NaOH溶液的正确操作是___________ (填字母)。
a.沿玻璃棒缓慢倒入 b.分三次少量倒入 c.一次迅速倒入
Ⅲ.学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致。
(6)键能也可以用于估算化学反应的反应热(ΔH),下表是部分化学键的键能数据:
已知白磷的燃烧热为2378.0kJ/mol,白磷(白磷的结构如图)完全燃烧的产物结构如图所示,则上表中X=___________ 。
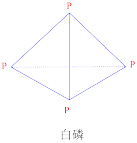
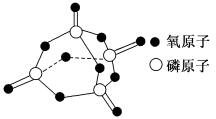
(7)1840年,俄国化学家盖斯在分析了许多化学反应热效应的基础上,总结出一条规律:“一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的。”这个规律被称为盖斯定律。有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得。
已知3.6g碳在6.4g的氧气中燃烧,至反应物耗尽,放出xkJ热量。已知单质碳的燃烧热为ykJ/mol,则1molC与O2反应生成CO的反应热△H为___________ kJ/mol(用x、y表示)。
Ⅰ.写出下列反应的热化学方程式
(1)1mol
 (g)在
(g)在 中完全燃烧生成
中完全燃烧生成 和液态水,放出1299.6kJ的热量
和液态水,放出1299.6kJ的热量(2)23g
 (l)在
(l)在 中完全燃烧生成
中完全燃烧生成 和液态水,放出683.4kJ的热量
和液态水,放出683.4kJ的热量Ⅱ.50 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热。回答下列问题:

(3)从实验装置上看,图中尚缺少的一种玻璃仪器是
(4)隔热层的作用是
(5)倒入NaOH溶液的正确操作是
a.沿玻璃棒缓慢倒入 b.分三次少量倒入 c.一次迅速倒入
Ⅲ.学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致。
(6)键能也可以用于估算化学反应的反应热(ΔH),下表是部分化学键的键能数据:
| 化学键 | P-P | P-O | O=O | P=O |
| 键能/(kJ·mol-1) | 172 | 335 | 498 | X |


(7)1840年,俄国化学家盖斯在分析了许多化学反应热效应的基础上,总结出一条规律:“一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的。”这个规律被称为盖斯定律。有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得。
已知3.6g碳在6.4g的氧气中燃烧,至反应物耗尽,放出xkJ热量。已知单质碳的燃烧热为ykJ/mol,则1molC与O2反应生成CO的反应热△H为
您最近一年使用:0次



