解题方法
1 . 在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
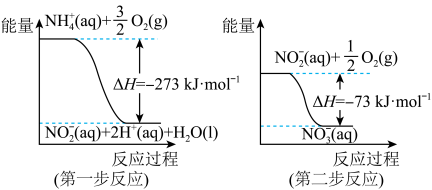
(1)第一步反应是___________ (填“放热”或“吸热”)反应,判断依据是___________ 。
(2)1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是___________ 。
(3)在0℃、101kPa时,44.8LH2在足量O2中完全燃烧生成H2O(l)放出571.6kJ的热量,则表示H2燃烧热的热化学方程式为___________ 。
(4)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g)ΔH1
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g) +H2(g)ΔH2
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g)ΔH3
2H2(g)+O2(g)=2H2O(g)ΔH4
则ΔH2=___________ (用ΔH1、ΔH3、ΔH4表示) 。
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
(1)第一步反应是
(2)1molNH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(3)在0℃、101kPa时,44.8LH2在足量O2中完全燃烧生成H2O(l)放出571.6kJ的热量,则表示H2燃烧热的热化学方程式为
(4)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g)ΔH1
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g) +H2(g)ΔH2
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g)ΔH3
2H2(g)+O2(g)=2H2O(g)ΔH4
则ΔH2=
您最近一年使用:0次
解题方法
2 . 根据题意回答下列问题。
(1)下列属于放热反应的是___________ 。
① 与
与 反应
反应
② 溶于水
溶于水
③
④碳与水蒸气反应
⑤ 与
与 反应
反应
(2)用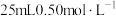 硫酸与
硫酸与 溶液在如图所示的装置中进行中和热的测定。
溶液在如图所示的装置中进行中和热的测定。
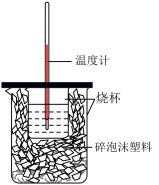
①从实验装置上看,图中尚缺少的一种玻璃仪器是___________ 。
②通过测定,计算出产生的热量为1.42kJ,请写出该反应的中和热的热化学方程式___________ 。
③若用相同浓度和体积的氨水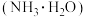 代替NaOH溶液进行上述实验,测得的中和热的数值会
代替NaOH溶液进行上述实验,测得的中和热的数值会___________ (填“偏大”“偏小”或“无影响”)
(3)家用液化气的成分之一是丁烷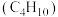 ,当
,当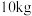 丁烷完全燃烧生成
丁烷完全燃烧生成 和液态水时,放出
和液态水时,放出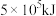 的热量。请写出丁烷燃烧热的热化学反应方程式
的热量。请写出丁烷燃烧热的热化学反应方程式___________ 。
(4)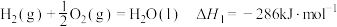
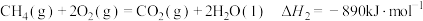
在25℃、101kPa, 和
和 的混合气体
的混合气体 完全燃烧生成
完全燃烧生成 和
和 ,放出热量
,放出热量 的热量。计算该混合气体
的热量。计算该混合气体 和
和 的体积比
的体积比___________ 。
(5)葡萄糖是人体所需能量的重要来源之一,设他在人体组织中完全氧化时的热化学方程式:
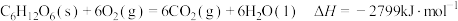 。计算100克葡萄糖在人体组织中完全氧化时产生的热量为
。计算100克葡萄糖在人体组织中完全氧化时产生的热量为___________ 。
(1)下列属于放热反应的是
①
 与
与 反应
反应②
 溶于水
溶于水③

④碳与水蒸气反应
⑤
 与
与 反应
反应(2)用
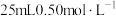 硫酸与
硫酸与 溶液在如图所示的装置中进行中和热的测定。
溶液在如图所示的装置中进行中和热的测定。
①从实验装置上看,图中尚缺少的一种玻璃仪器是
②通过测定,计算出产生的热量为1.42kJ,请写出该反应的中和热的热化学方程式
③若用相同浓度和体积的氨水
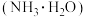 代替NaOH溶液进行上述实验,测得的中和热的数值会
代替NaOH溶液进行上述实验,测得的中和热的数值会(3)家用液化气的成分之一是丁烷
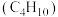 ,当
,当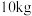 丁烷完全燃烧生成
丁烷完全燃烧生成 和液态水时,放出
和液态水时,放出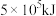 的热量。请写出丁烷燃烧热的热化学反应方程式
的热量。请写出丁烷燃烧热的热化学反应方程式(4)
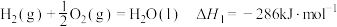
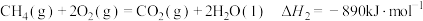
在25℃、101kPa,
 和
和 的混合气体
的混合气体 完全燃烧生成
完全燃烧生成 和
和 ,放出热量
,放出热量 的热量。计算该混合气体
的热量。计算该混合气体 和
和 的体积比
的体积比(5)葡萄糖是人体所需能量的重要来源之一,设他在人体组织中完全氧化时的热化学方程式:
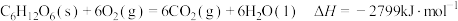 。计算100克葡萄糖在人体组织中完全氧化时产生的热量为
。计算100克葡萄糖在人体组织中完全氧化时产生的热量为
您最近一年使用:0次
解题方法
3 . 依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_______ 。
(2)若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量,则表示该反应的热化学方程式为_______ 。
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量,则表示该反应的热化学方程式为_______ 。
(4)已知拆开1molH—H,1molN—H,1molNN分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_______ 。
(5)HCl和NaOH反应的中和热ΔH=-57.3kJ·mol-1,则H2SO4和NaOH反应的中和热的热化学方程式为_______ 。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(2)若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量,则表示该反应的热化学方程式为
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量,则表示该反应的热化学方程式为
(4)已知拆开1molH—H,1molN—H,1molNN分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(5)HCl和NaOH反应的中和热ΔH=-57.3kJ·mol-1,则H2SO4和NaOH反应的中和热的热化学方程式为
您最近一年使用:0次
4 . 回答下列问题:
(1)一定条件下,由稳定单质反应生成1 mol化合物的反应热叫该化合物的生成热(ΔH)。图为VIA族元素氢化物a、b、c、d的生成热数据示意图。

①非金属元素氢化物的稳定性与氢化物的生成热△H的关系为_______ 。
②硫化氢发生分解反应的热化学方程式为_______ 。
(2)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
a)CH4(g)+CO2(g) 2CO(g)+2H2(g) △H1
2CO(g)+2H2(g) △H1
b)CO2(g)+H2(g) CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
c)CH4(g) C(s)+2H2(g) △H3
C(s)+2H2(g) △H3
d)2CO(g) CO2(g)+C(s) △H4
CO2(g)+C(s) △H4
e)CO(g)+H2(g) H2O(g)+C(s) △H5
H2O(g)+C(s) △H5
根据盖斯定律,反应a的△H1=_______ (写出一个代数式即可)
(3)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25°C时,相关物质的燃烧热数据如表:
则25°C时H2(g)和C(石墨,s)生成C6H6(l)的热化学方程式为_______ 。
(4)已知5C2H4(g)+12MnO (aq)+36H+(aq)=12Mn2+(aq)+10CO2(g)+28H2O(l) △H=-m kJ·mol-1,当放出的热量为n kJ时,该反应转移的电子数为
(aq)+36H+(aq)=12Mn2+(aq)+10CO2(g)+28H2O(l) △H=-m kJ·mol-1,当放出的热量为n kJ时,该反应转移的电子数为_______ (用含m、n的代数式表示)
(1)一定条件下,由稳定单质反应生成1 mol化合物的反应热叫该化合物的生成热(ΔH)。图为VIA族元素氢化物a、b、c、d的生成热数据示意图。

①非金属元素氢化物的稳定性与氢化物的生成热△H的关系为
②硫化氢发生分解反应的热化学方程式为
(2)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
a)CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H1
2CO(g)+2H2(g) △H1b)CO2(g)+H2(g)
 CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2c)CH4(g)
 C(s)+2H2(g) △H3
C(s)+2H2(g) △H3d)2CO(g)
 CO2(g)+C(s) △H4
CO2(g)+C(s) △H4e)CO(g)+H2(g)
 H2O(g)+C(s) △H5
H2O(g)+C(s) △H5根据盖斯定律,反应a的△H1=
(3)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25°C时,相关物质的燃烧热数据如表:
| 物质 | H2(g) | C(石墨,s) | C6H6(l) |
| 燃烧热△H(kJ·mol-1) | -285.8 | -393.5 | -3267.5 |
(4)已知5C2H4(g)+12MnO
 (aq)+36H+(aq)=12Mn2+(aq)+10CO2(g)+28H2O(l) △H=-m kJ·mol-1,当放出的热量为n kJ时,该反应转移的电子数为
(aq)+36H+(aq)=12Mn2+(aq)+10CO2(g)+28H2O(l) △H=-m kJ·mol-1,当放出的热量为n kJ时,该反应转移的电子数为
您最近一年使用:0次
解题方法
5 . 写出下列反应的热化学方程式:
(1)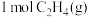 与适量
与适量 反应,生成
反应,生成 和
和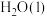 ,放出
,放出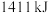 的热。
的热。___________ 。
(2)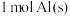 与适量
与适量 发生反应,生成
发生反应,生成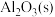 ,放出
,放出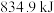 的热。
的热。___________ 。
(1)
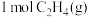 与适量
与适量 反应,生成
反应,生成 和
和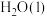 ,放出
,放出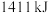 的热。
的热。(2)
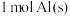 与适量
与适量 发生反应,生成
发生反应,生成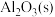 ,放出
,放出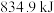 的热。
的热。
您最近一年使用:0次
2021-06-05更新
|
380次组卷
|
3卷引用:(苏教版2019)必修第二册专题6 化学反应与能量变化 第二单元 化学反应中的热 课时1 化学反应中的能量变化
解题方法
6 . 依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1mol甲醇(CH3OH)燃烧生成CO2和液态水时放热725.76kJ。则表示甲醇燃烧热的热化学方程式为_______
(2)若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量_______ 。
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量_______ 。
(4)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_______ 。
(1)在25℃、101kPa下,1mol甲醇(CH3OH)燃烧生成CO2和液态水时放热725.76kJ。则表示甲醇燃烧热的热化学方程式为
(2)若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量
(4)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
您最近一年使用:0次
7 . (1)若5.2g乙炔(C2H2气态)完全燃烧生成液态水和CO2(g)时放热260kJ。该反应的热化学方程式为___________ ;乙炔的燃烧热为___________ kJ·mol-1。
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___________ 。
(3)已知:2Fe(s)+O2(g)=2FeO(s) ΔH=-544.0kJ·mol-1 ;4Al(s)+3O2(g)=2Al2O3(s) ΔH=-3351.4kJ·mol-1;则Al和FeO发生铝热反应的热化学方程式为:___________ 。
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(3)已知:2Fe(s)+O2(g)=2FeO(s) ΔH=-544.0kJ·mol-1 ;4Al(s)+3O2(g)=2Al2O3(s) ΔH=-3351.4kJ·mol-1;则Al和FeO发生铝热反应的热化学方程式为:
您最近一年使用:0次
名校
解题方法
8 . 填空
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石___ (填“>”或“<”)石墨。
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1____ (填“>”或“<”)ΔH2。
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:________ 。
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=____ 。
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=______ 。
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是________ 。
(1)已知C(s,石墨)=C(s,金刚石) ΔH>0,则稳定性:金刚石
(2)已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2;则ΔH1
(3)“嫦娥五号”发射时,用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1;
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式:
(4)25 ℃、101 kPa时,14 g CO在足量的O2中充分燃烧,放出141.3 kJ热量,则CO的燃烧热ΔH=
(5)0.50 L 2.00 mol·L-1H2SO4溶液与2.10 L 1.00 mol·L-1 KOH溶液完全反应,放出114.6 kJ热量,该反应的中和热ΔH=
(6)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是
您最近一年使用:0次
2020-12-15更新
|
319次组卷
|
6卷引用:河北省安平中学2017-2018学年高一下学期期末考试化学试题1
河北省安平中学2017-2018学年高一下学期期末考试化学试题12015届四川省成都郫县高三第二次阶诊断性考试理综化学试卷贵州省毕节市七星关区毕节市实验高级中学2020-2021学年高二上学期期中考试化学试题(已下线)第六章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)专题18 化学反应与能量(限时精练)-2022年高三毕业班化学常考点归纳与变式演练重庆市沙坪坝实验中学校2021-2022学年高二上学期12月月考化学试题
名校
9 . (1)已知:
试计算N2+3H2=2NH3的∆H是多少?___
(2)已知:H2和CH4的燃烧热分别为∆H=-286KJ/mol和∆H-890KJ/mol,则112L标况下的H2和CH4的混合气体完全燃烧生成的CO2和液态水时放出3695KJ的热量,则混合气体中H2和CH4的物质的量之比是多少?___
| 化学键 | H-H | N≡N | N-H |
| 拆开1mol该键吸收能量KJ/mol | 436 | 946 | 391 |
试计算N2+3H2=2NH3的∆H是多少?
(2)已知:H2和CH4的燃烧热分别为∆H=-286KJ/mol和∆H-890KJ/mol,则112L标况下的H2和CH4的混合气体完全燃烧生成的CO2和液态水时放出3695KJ的热量,则混合气体中H2和CH4的物质的量之比是多少?
您最近一年使用:0次
名校
10 . 为了合理利用化学能,确保安全生产,进行化工设计时需要充分考虑化学反应的反应热,并采取相应措施。化学反应的反应热通常可以通过实验进行测定,也可通过理论进行推算。
(1)实验测得5g甲醇(CH3OH)液体在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,则表示甲醇燃烧热的热化学方程式为___ 。
(2)现有如下两个热化学方程式:
2H2(g)+O2(g)=2H2O(g) ΔH1=akJ•mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=bkJ•mol-1
则a___ (填“>”“=”或“<”)b。
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程。在化学反应过程中,断裂化学键需要消耗能量,形成化学键又会释放能量。
已知:N2(g)+3H2(g) 2NH3(g)ΔH=akJ•mol-1,根据下表中所列键能数据可计算出a=
2NH3(g)ΔH=akJ•mol-1,根据下表中所列键能数据可计算出a=___ 。
(1)实验测得5g甲醇(CH3OH)液体在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,则表示甲醇燃烧热的热化学方程式为
(2)现有如下两个热化学方程式:
2H2(g)+O2(g)=2H2O(g) ΔH1=akJ•mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=bkJ•mol-1
则a
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程。在化学反应过程中,断裂化学键需要消耗能量,形成化学键又会释放能量。
已知:N2(g)+3H2(g)
 2NH3(g)ΔH=akJ•mol-1,根据下表中所列键能数据可计算出a=
2NH3(g)ΔH=akJ•mol-1,根据下表中所列键能数据可计算出a=| 化学键 | H—H | N—H | N≡N |
| 键能/(kJ•mol-1) | 436 | 391 | 945 |
您最近一年使用:0次
2020-09-02更新
|
279次组卷
|
2卷引用:黑龙江省哈尔滨市第一中学校2019-2020学年高一下学期期末考试化学试题



