名校
解题方法
1 . 下列关于反应能量的说法正确的是
| A.若反应A(g)=B(g) ΔH<0,说明物质A(g)比物质B(g)稳定,分子内共价键键能 A比B大 |
| B.若Mg(s)+CuSO4 (aq)=MgSO4 (aq)+Cu(s) ΔH=a kJ·mol-1,则a<0 |
| C.101 kPa时,2H2(g)+O2(g)=2H2O(l) ΔH= -Q kJ·mol-1,则H2的燃烧热为1/2Q kJ·mol-1 |
| D.H+(aq)+OH-(aq)=H2O(l) ΔH= -57.3 kJ·mol-1,则含1 mol NaOH的氢氧化钠溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量 |
您最近一年使用:0次
2021-11-03更新
|
790次组卷
|
2卷引用:河南省范县第一中学2021-2022学年高二上学期第一次月考检测化学试题
名校
解题方法
2 . 下列关于热化学反应的描述中正确的是
| A.HCl和NaOH反应的中和热∆H=-57.3 kJ/mol |
| B.甲烷的标准燃烧热∆H=-890.3kJ/mol,则CH4(g)+2O2(g)=CO2(g)+2H2O(g)∆H<-890.3 kJ/mol |
| C.500℃、30 MPa下,N2(g)+3H2(g)⇌2NH3(g)∆H =-92.4kJ/mol,将1.5mol H2和过量的N2在此条件下充分反应,放出热量46.2kJ |
| D.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g)的∆H=+566.0kJ/mol |
您最近一年使用:0次
2021-01-14更新
|
715次组卷
|
25卷引用:合肥八中、阜阳一中2017-2018学年第一学期高二年级期末考试化学试题
合肥八中、阜阳一中2017-2018学年第一学期高二年级期末考试化学试题福建省晋江市季延中学2017-2018学年高二下学期期末考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期10月月考化学试题【全国百强校】吉林省实验中学2018-2019学年高二上学期期中考试化学试题【校级联考】福建省长汀、连城一中等六校2018-2019学年高二年上学期期中考联考化学试题【市级联考】吉林省吉林市普通高中2018-2019学年高二上学期期中考试化学试题新疆维吾尔自治区石河子二中2018-2019学年高二上学期第二次月考化学试题黑龙江省齐齐哈尔市第八中学2018-2019学年高二上学期期末考试化学试题贵州省思南中学2019-2020学年高二上学期期中考试化学试题安徽省滁州市定远县育才学校2019-2020学年高二上学期期中考试(普通班)化学试题甘肃省张掖市高台县第一中学2018-2019学年高二上学期期末考试理科化学试题重庆市凤鸣山中学2018-2019学年高二上学期期中考试化学试题福建省三明第一中学2019-2020学年高二下学期期中考试化学试题(已下线)第01章 化学反应与能量(A卷基础篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)山西省朔州市怀仁县怀仁一中云东校区2020-2021学年高二9月月考化学试题(已下线)【南昌新东方】9.湾里一中 梁莎吉林公主岭范家屯一中2020-2021学年高二上学期期中考试化学试题福建省莆田第二十五中学2021届高三上学期期中考试化学试题陕西省榆林市第十二中学2021届高三上学期第三次月考(12月)化学试题河北省张家口市崇礼区第一中学2021届高三上学期期中考试化学试题 江苏省苏州实验中学2020-2021学年高二下学期3月份学情调研考试化学试题(已下线)第17讲 化学能与热能(精讲)-2022年一轮复习讲练测江西省赣县第三中学2021-2022学年高二上学期入学考试化学试题(已下线)专题1 化学反应与能量(章末培优)-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)河北省顺平县中学2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
3 . 下列关于热化学反应的描述正确的是
A.已知 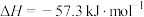 ,则HCl和 ,则HCl和 反应的反应热 反应的反应热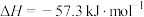 |
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是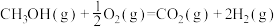 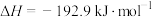 ,则 ,则 的标准燃烧热 的标准燃烧热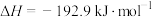 |
C.已知  ; ;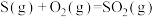  ,则 ,则 |
D.葡萄糖的标准燃烧热 ,则 ,则 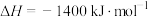 |
您最近一年使用:0次
名校
4 . 下列图示与对应叙述相符的是
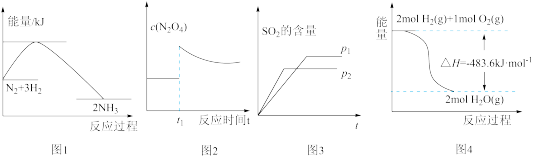

| A.图1反应达平衡后,升高温度,平衡常数K值减小 |
B.图2表示平衡2NO2(g) N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 |
C.图3表示可逆反应“2SO2+O2 2SO3”中SO2的含量与压强的关系,且P2>P1 2SO3”中SO2的含量与压强的关系,且P2>P1 |
| D.图4表示H2与O2发生反应过程中的能量变化,则H2的燃烧热ΔH=-241.8kJ•mol-1 |
您最近一年使用:0次
2022-09-27更新
|
328次组卷
|
3卷引用:江苏省如皋中学2022-2023学年高二上学期8月综合测试化学试题
名校
5 . 下列热化学方程正确的是( 的绝对值均正确)
的绝对值均正确)
 的绝对值均正确)
的绝对值均正确)A.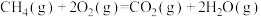 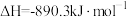 (燃烧热) (燃烧热) |
B. 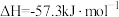 (中和热) (中和热) |
C. 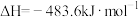 (反应热) (反应热) |
D.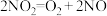 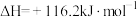 (反应热) (反应热) |
您最近一年使用:0次
2022-07-01更新
|
327次组卷
|
6卷引用:2016-2017学年四川省资阳市高二上学期期末化学试卷
名校
解题方法
6 . 下列推论不正确的是
A. ⇌ ⇌ 为放热反应,则 为放热反应,则 的能量一定高于 的能量一定高于 的能量 的能量 |
B.C(s,石墨)=C(s,金刚石)  ,则石墨比金刚石稳定 ,则石墨比金刚石稳定 |
C.葡萄糖的燃烧热是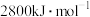 ,则 ,则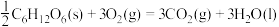  |
D. 时, 时, 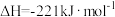 ,则碳的燃烧热为110.5KJ/mol ,则碳的燃烧热为110.5KJ/mol |
您最近一年使用:0次
2022-01-18更新
|
436次组卷
|
4卷引用:湖南省岳阳市临湘市2021-2022学年高二上学期期末教学质量检测化学试题
7 . 已知反应:① 2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
② 稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol
下列结论正确的是
② 稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol
下列结论正确的是
| A.碳的燃烧热大于110.5 kJ/mol |
| B.①的反应热为221 kJ/mol |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量 |
您最近一年使用:0次
2023-03-28更新
|
286次组卷
|
2卷引用:海南省白沙中学2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
8 . 下列说法或表示正确的是
| A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由C(石墨)→C(金刚石) ΔH=+1.9kJ·mol-1可知,金刚石不如石墨稳定 |
| C.在稀溶液中:H+(aq)+OH—(aq)=H2O(l) ΔH=—57.3kJ·mol-1,若将含1molCH3COOH的醋酸溶液与含1molNaOH的溶液混合,放出的热量小于57.3kJ |
| D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) ΔH=—285.8kJ·mol-1 |
您最近一年使用:0次
2022-10-08更新
|
272次组卷
|
2卷引用:山东省德州市陵城区祥龙高级中学2022-2023学年高二上学期9月月考化学试题
9 . 已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.6kJ·mol-1.以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的图示与过程如图:
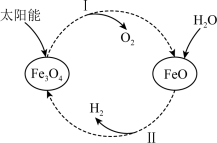
过程Ⅰ:……
过程Ⅱ:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ·mol-1
下列说法正确的是

过程Ⅰ:……
过程Ⅱ:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ·mol-1
下列说法正确的是
| A.该过程能量转化形式是太阳能→化学能→热能 |
B.过程Ⅰ热化学方程式为:Fe3O4(s)=3FeO(s)+ O2(g) ΔH=-156.6kJ·mol-1 O2(g) ΔH=-156.6kJ·mol-1 |
| C.氢气的燃烧热为ΔH=-285.8 kJ·mol-1 |
| D.铁氧化合物循环制H2具有成本低、产物易分离等优点 |
您最近一年使用:0次
2021-12-29更新
|
495次组卷
|
2卷引用:河北省盐山中学2021-2022学年高二上学期期中考试化学试题
10 . H2在O2中燃烧的能量变化如图所示。

下列叙述错误的是

下列叙述错误的是
| A.1molH2O(g)的能量比1molH2O(l)高44kJ |
| B.过程II生成的O-H键比过程III生成的O-H键更牢固 |
C.过程I可表示为:H2(g)+ O2(g)=O(g)+2H(g)△H=+685kJ·mol-1 O2(g)=O(g)+2H(g)△H=+685kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(g)的△H等于-244kJ·mol-1 |
您最近一年使用:0次
2022-05-13更新
|
220次组卷
|
2卷引用:山东省潍坊安丘市、高密市、诸城市2021-2022学年高一下学期期中考试化学试题



