1 . 金属镓有“电子工业脊梁”的美誉,镓及其化合物应用广泛。
(1) 镓(Ga)的原子结构示意图为 ,镓元素在周期表中的位置是
,镓元素在周期表中的位置是_______ 。
(2)镓能与沸水剧烈反应生成氢气和氢氧化镓,该反应的化学方程式是______________ 。
(3)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。
资料:镓的熔点较低(29.8℃),沸点很高(2403℃)。
①传统的氮化镓(GaN)制备方法是采用GaCl3与NH3在一定条件下反应,该反应的化学方程式是____________________ 。
②当代工业上固态氮化镓(GaN)的制备方法是利用镓与NH3在1000℃高温下合成,同时生成氢气,每生成l mol H2时放出10.27 kJ热量。该可逆反应的热化学方程式是____________________________________ 。
③在密闭容器中,充入一定量的Ga与NH3发生上述反应,实验测得反应平衡体系中NH3的体积分数与压强P和温度T的关系曲线如图1所示。

图中A点和C点化学平衡常数的关系是:KA_____ KC (填“>”“=”或“<”),理由是_____________________________ 。
(4)电解法可以提纯粗镓,具体原理如图2所示:
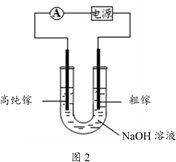
①粗镓与电源____ 极相连。(填“正”或“负”)
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电的电极反应式是
_____________________________ 。
(1) 镓(Ga)的原子结构示意图为
 ,镓元素在周期表中的位置是
,镓元素在周期表中的位置是(2)镓能与沸水剧烈反应生成氢气和氢氧化镓,该反应的化学方程式是
(3)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。
资料:镓的熔点较低(29.8℃),沸点很高(2403℃)。
①传统的氮化镓(GaN)制备方法是采用GaCl3与NH3在一定条件下反应,该反应的化学方程式是
②当代工业上固态氮化镓(GaN)的制备方法是利用镓与NH3在1000℃高温下合成,同时生成氢气,每生成l mol H2时放出10.27 kJ热量。该可逆反应的热化学方程式是
③在密闭容器中,充入一定量的Ga与NH3发生上述反应,实验测得反应平衡体系中NH3的体积分数与压强P和温度T的关系曲线如图1所示。

图中A点和C点化学平衡常数的关系是:KA
(4)电解法可以提纯粗镓,具体原理如图2所示:

①粗镓与电源
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电的电极反应式是
您最近一年使用:0次
名校
2 . 氧、硫、硒( )、碲(
)、碲( )、钋(
)、钋(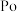 )是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:
)是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:
(1) 在周期表中的位置为
在周期表中的位置为_______ 。
(2)某温度时,该族单质与 反应生成气态
反应生成气态 的热化学方程式如下:
的热化学方程式如下:
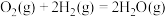

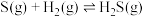


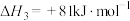
①硫和硒的氢化物的热稳定性:H2S_____ H2Se (填>、=或<);用原子结构知识解释你的判断结果_______ 。
②写出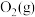 与
与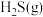 反应生成
反应生成 和
和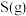 的热化学方程式
的热化学方程式_______ 。
(3)生物浸出法可有效回收含硫矿石中的有色金属,某种生物浸出法中主要物质的转化路径如图。

①步骤I反应的离子方程式为_______ 。
②生物浸出时的总反应的氧化剂是_______ 。
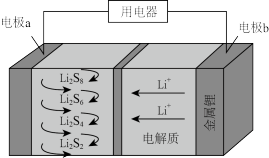
(4)全固态锂硫电池能量密度高,其工作原理如图所示,其中电极 常用掺有石墨烯的
常用掺有石墨烯的 材料,电池反应为:
材料,电池反应为: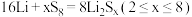 。下列说法
。下列说法错误 的是_______
 )、碲(
)、碲( )、钋(
)、钋(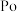 )是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:
)是元素周期表中原子序数依次增大的同主族元素。该族元素及其化合物在生产生活中发挥着巨大作用。回答下列问题:(1)
 在周期表中的位置为
在周期表中的位置为(2)某温度时,该族单质与
 反应生成气态
反应生成气态 的热化学方程式如下:
的热化学方程式如下: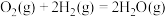

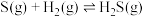


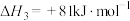
①硫和硒的氢化物的热稳定性:H2S
②写出
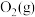 与
与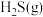 反应生成
反应生成 和
和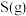 的热化学方程式
的热化学方程式(3)生物浸出法可有效回收含硫矿石中的有色金属,某种生物浸出法中主要物质的转化路径如图。

①步骤I反应的离子方程式为
②生物浸出时的总反应的氧化剂是
(4)全固态锂硫电池能量密度高,其工作原理如图所示,其中电极
 常用掺有石墨烯的
常用掺有石墨烯的 材料,电池反应为:
材料,电池反应为: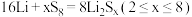 。下列说法
。下列说法
A.电池工作时,正极可发生反应: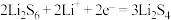 |
B.电池工作时,外电路中流过 电子,负极材料减重 电子,负极材料减重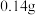 |
C.石墨烯的作用主要是提高电极 的导电性 的导电性 |
D.电池充电时间越长,电池中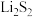 的量越多 的量越多 |
您最近一年使用:0次
2022-07-05更新
|
130次组卷
|
2卷引用:北京市第十二中学2021-2022学年高一下学期6月月考化学试题
名校
3 . 工业上,一氧化碳是一碳化学的基础,可用于物质的合成与纯化等。
(1)二氧化碳和木炭还原法是工业制备CO的方法之一,利用如图关系计算:C(石墨)

___________ 。

(2)羰基硫(COS)是一种粮食熏蒸剂,能防止某些昆虫和真菌的危害,一氧化碳可用于羰基硫的合成。在容积不变的密闭容器中,使CO和H2S发生下列反应并达到平衡: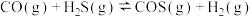

①若反应前CO物质的量为10mol,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1。下列说法正确的是___________ (填字母)。
a.通入CO后,正反应速率逐渐增大
b.反应前H2S物质的量为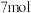
c.达到平衡时CO的转化率为80%
②画出在不同温度下达到化学平衡时,H2S的转化率随温度变化示意图___________ (画出变化趋势即可)。
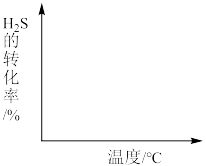
③已知羰基硫(COS)分子中所有原子的最外层都满足8电子结构,则下列有关说法正确的是________ 。
A.羰基硫属于非极性分子
B.羰基硫的沸点比CO2低
C.羰基硫分子中三个原子处于同一直线上
(3)羰化冶金工艺是气化冶金技术的重要分支,其原理是利用Ⅷ族过渡金属与一氧化碳反应,生成易挥发的羰基化合物进行分离提取金属的一种方法。以某镍合金为原料的羰基工艺流程如下图所示:

“热交换”步骤涉及的反应有:
I.
II.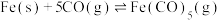
III.
IV.
①温度不变时提高反应I中Ni(CO)4的产率,可采取的措施___________ (答一条即可)。
②Ni(CO)4的沸点为:43℃,其分解温度也只有60℃,Fe(CO)5的沸点为:106℃,精馏的温度范围应控制在___________ ℃。
③实际生产中要调整合成原料中铜元素与硫元素的质量比为___________ 。
④Cu、Au不在VIII族,不易生成羰基化合物。在元素周期表中Au跟Cu处在同一列,则Au位于_____ 族。
(1)二氧化碳和木炭还原法是工业制备CO的方法之一,利用如图关系计算:C(石墨)



(2)羰基硫(COS)是一种粮食熏蒸剂,能防止某些昆虫和真菌的危害,一氧化碳可用于羰基硫的合成。在容积不变的密闭容器中,使CO和H2S发生下列反应并达到平衡:
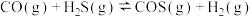

①若反应前CO物质的量为10mol,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1。下列说法正确的是
a.通入CO后,正反应速率逐渐增大
b.反应前H2S物质的量为
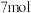
c.达到平衡时CO的转化率为80%
②画出在不同温度下达到化学平衡时,H2S的转化率随温度变化示意图

③已知羰基硫(COS)分子中所有原子的最外层都满足8电子结构,则下列有关说法正确的是
A.羰基硫属于非极性分子
B.羰基硫的沸点比CO2低
C.羰基硫分子中三个原子处于同一直线上
(3)羰化冶金工艺是气化冶金技术的重要分支,其原理是利用Ⅷ族过渡金属与一氧化碳反应,生成易挥发的羰基化合物进行分离提取金属的一种方法。以某镍合金为原料的羰基工艺流程如下图所示:

“热交换”步骤涉及的反应有:
I.

II.
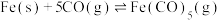
III.

IV.

①温度不变时提高反应I中Ni(CO)4的产率,可采取的措施
②Ni(CO)4的沸点为:43℃,其分解温度也只有60℃,Fe(CO)5的沸点为:106℃,精馏的温度范围应控制在
③实际生产中要调整合成原料中铜元素与硫元素的质量比为
④Cu、Au不在VIII族,不易生成羰基化合物。在元素周期表中Au跟Cu处在同一列,则Au位于
您最近一年使用:0次
2010·北京海淀·一模
4 . A、B、C是三种常见短周期元素的单质。常温下D为无色液体,E是一种常见的温室气体。其转化关系如图(反应条件和部分产物略去)。试回答:

(1)E的电子式是______ 。
(2)单质X和B或D均能反应生成黑色固体Y,Y的化学式是_______ 。
(3)物质Z常用于对空气进行杀菌,净化和水果保鲜等。Z和B的组成元素相同,Z分子中各原子最外层电子数之和为18。Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是______ 。
(4)取0.3 mol F与足量D充分混合后,所得溶液中再通入0.2 mol E充分反应,最后得到的水溶液中各种离子的浓度由大到小的顺序是(不考虑H+)____________________ 。
(5)E的大量排放会引发很多环境问题。有科学家提出,用E和H2合成CH3OH和H2O,对E进行综合利用。25℃,101 kPa时,该反应的热化学方程式是__________________ 。(已知甲醇的燃烧热△H= -726.5kJ·mol-1,氢气的燃烧热△H= -285.8kJ·mol-1)

(1)E的电子式是
(2)单质X和B或D均能反应生成黑色固体Y,Y的化学式是
(3)物质Z常用于对空气进行杀菌,净化和水果保鲜等。Z和B的组成元素相同,Z分子中各原子最外层电子数之和为18。Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是
(4)取0.3 mol F与足量D充分混合后,所得溶液中再通入0.2 mol E充分反应,最后得到的水溶液中各种离子的浓度由大到小的顺序是(不考虑H+)
(5)E的大量排放会引发很多环境问题。有科学家提出,用E和H2合成CH3OH和H2O,对E进行综合利用。25℃,101 kPa时,该反应的热化学方程式是
您最近一年使用:0次



