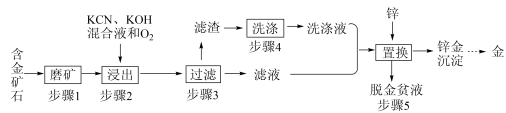
1 . 金是一种用途广泛的贵重金属。某化工厂利用氰化法从一种含金矿石中提取金的工艺流程如下:
资料:
① Zn + O2 + H2O = Zn(OH)2
O2 + H2O = Zn(OH)2
② Zn2+(aq) Zn(CN)2(s)
Zn(CN)2(s)  Zn(CN)42-(aq)
Zn(CN)42-(aq)
(1)步骤2中发生的反应有:
① 2Au(s) + 4CN-(aq) + 2H2O(l) + O2(g) = 2Au(CN)2-(aq) + 2OH-(aq) + H2O2(aq) ∆H = -197.61 kJ·mol-1
② 2Au(s) + 4CN-(aq)+ H2O2(aq) = 2Au(CN)2-(aq) + 2OH-(aq) ∆H = -386.93 kJ·mol-1
则2Au(s)+ 4CN-(aq)+ H2O(l) + 1/2O2(g) = 2Au(CN)2-(aq) + 2OH-(aq)的∆H =_______ 。
(2)下图是步骤2中金的溶解速率与温度的关系。80℃以后溶解速率降低的原因是___________ 。

(3)步骤4的目的是_________________ 。
(4)步骤5置换的总反应是:
2Au(CN)2- + 3Zn + 4CN- + 2H2O = 2Au + 2Zn(CN)42- + ZnO22- + 2H2↑
则以下说法正确的是________ (填字母序号)。
A 步骤5进行时要先脱氧,否则会增加锌的用量
B 若溶液中c(CN-)过小,会生成Zn(CN)2,减缓置换速率
C 实际生产中加入适量Pb(NO3)2的目的是形成原电池加快置换速率
(5)脱金贫液(主要含有CN-)会破坏环境,影响人类健康,可通过化学方法转化为无毒废水净化排放。碱性条件下,用Cl2将贫液中的CN-氧化成无毒的CO2和N2,该反应的离子方程式为_______________ 。

资料:
① Zn +
 O2 + H2O = Zn(OH)2
O2 + H2O = Zn(OH)2② Zn2+(aq)
 Zn(CN)2(s)
Zn(CN)2(s)  Zn(CN)42-(aq)
Zn(CN)42-(aq)(1)步骤2中发生的反应有:
① 2Au(s) + 4CN-(aq) + 2H2O(l) + O2(g) = 2Au(CN)2-(aq) + 2OH-(aq) + H2O2(aq) ∆H = -197.61 kJ·mol-1
② 2Au(s) + 4CN-(aq)+ H2O2(aq) = 2Au(CN)2-(aq) + 2OH-(aq) ∆H = -386.93 kJ·mol-1
则2Au(s)+ 4CN-(aq)+ H2O(l) + 1/2O2(g) = 2Au(CN)2-(aq) + 2OH-(aq)的∆H =
(2)下图是步骤2中金的溶解速率与温度的关系。80℃以后溶解速率降低的原因是

(3)步骤4的目的是
(4)步骤5置换的总反应是:
2Au(CN)2- + 3Zn + 4CN- + 2H2O = 2Au + 2Zn(CN)42- + ZnO22- + 2H2↑
则以下说法正确的是
A 步骤5进行时要先脱氧,否则会增加锌的用量
B 若溶液中c(CN-)过小,会生成Zn(CN)2,减缓置换速率
C 实际生产中加入适量Pb(NO3)2的目的是形成原电池加快置换速率
(5)脱金贫液(主要含有CN-)会破坏环境,影响人类健康,可通过化学方法转化为无毒废水净化排放。碱性条件下,用Cl2将贫液中的CN-氧化成无毒的CO2和N2,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 煤的洁净技术(包括固硫技术和脱硫技术两类)可有效降低燃煤废气中SO2的含量,已成为我国解决环境问题的主导技术之一。
I.固硫技术:通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。石灰石是常用的固硫剂,固硫过程中涉及的部分反应如下:
①CaCO3(s) CaO(s)+CO2(g) △H1=+178.30kJ/mol
CaO(s)+CO2(g) △H1=+178.30kJ/mol
②CaO(s)+SO2(g)+0.5O2(g) CaSO4(s) △H2=-501.92kJ/mol
CaSO4(s) △H2=-501.92kJ/mol
③CO(g)+0.5O2(g) CO2(g) △H3
CO2(g) △H3
④CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol
CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol
(1)温度升高,反应①的化学平衡常数____ (填“增大”“减小”或“不变”)。
(2)△H3=____ kJ/mol。
(3)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),结合反应②、③、④分析其原因:____ 。
II.电化学脱硫技术是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(·OH,氧元素为-1价)将燃煤中的含硫物质氧化除去。
(4)将煤打成煤浆加入电解槽的目的是____ 。
(5)补全用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式:____ 。
FeS2+·OH=Fe3++SO +H2O+_____。
+H2O+_____。
(6)对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如图所示。

pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;____ 。
I.固硫技术:通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。石灰石是常用的固硫剂,固硫过程中涉及的部分反应如下:
①CaCO3(s)
 CaO(s)+CO2(g) △H1=+178.30kJ/mol
CaO(s)+CO2(g) △H1=+178.30kJ/mol②CaO(s)+SO2(g)+0.5O2(g)
 CaSO4(s) △H2=-501.92kJ/mol
CaSO4(s) △H2=-501.92kJ/mol③CO(g)+0.5O2(g)
 CO2(g) △H3
CO2(g) △H3④CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol
CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol(1)温度升高,反应①的化学平衡常数
(2)△H3=
(3)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),结合反应②、③、④分析其原因:
II.电化学脱硫技术是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(·OH,氧元素为-1价)将燃煤中的含硫物质氧化除去。
(4)将煤打成煤浆加入电解槽的目的是
(5)补全用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式:
FeS2+·OH=Fe3++SO
 +H2O+_____。
+H2O+_____。(6)对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如图所示。

pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;
您最近一年使用:0次
2023·江苏淮安·模拟预测
名校
3 . 含氮化合物( 、
、 、
、 等)是环境污染物,可用以下方法消除其污染。
等)是环境污染物,可用以下方法消除其污染。
Ⅰ.苯酚( )是一种广泛使用、易氧化的化工产品。一种在
)是一种广泛使用、易氧化的化工产品。一种在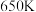 下用
下用 废气催化氧化苯制备苯酚的新方法为:
废气催化氧化苯制备苯酚的新方法为: 。
。
(1)已知



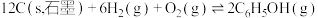
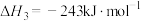
则

___________ 。
Ⅱ.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),以达到消除污染的目的,其工作原理如图-1所示。
),以达到消除污染的目的,其工作原理如图-1所示。
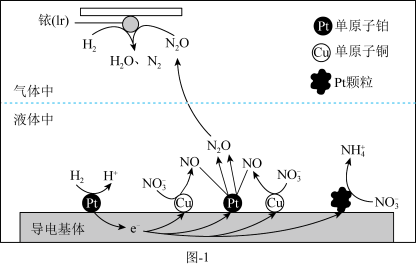
(2) 被
被 还原为
还原为 的过程可描述为:液体中,
的过程可描述为:液体中, 在导电基体的单原子铂上失去电子生成
在导电基体的单原子铂上失去电子生成 ,电子进入导电基体中进行传导,
,电子进入导电基体中进行传导,___________ 。
(3)若导电基体上的Pt颗粒增多,造成的后果是___________ 。
(4)单原子铂催化剂相比于Pt颗粒催化剂,优点有___________ 。
Ⅲ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图2为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。

(5)该装置可以生成大量氧化性更强的 ,
, 去除
去除 的离子方程式为
的离子方程式为___________ 。
(6)相比于传统的二维电极反应系统,三维电极的优点有___________ 。
 、
、 、
、 等)是环境污染物,可用以下方法消除其污染。
等)是环境污染物,可用以下方法消除其污染。Ⅰ.苯酚(
 )是一种广泛使用、易氧化的化工产品。一种在
)是一种广泛使用、易氧化的化工产品。一种在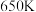 下用
下用 废气催化氧化苯制备苯酚的新方法为:
废气催化氧化苯制备苯酚的新方法为: 。
。(1)已知




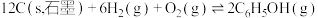
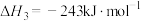
则


Ⅱ.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的
 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),以达到消除污染的目的,其工作原理如图-1所示。
),以达到消除污染的目的,其工作原理如图-1所示。
(2)
 被
被 还原为
还原为 的过程可描述为:液体中,
的过程可描述为:液体中, 在导电基体的单原子铂上失去电子生成
在导电基体的单原子铂上失去电子生成 ,电子进入导电基体中进行传导,
,电子进入导电基体中进行传导,(3)若导电基体上的Pt颗粒增多,造成的后果是
(4)单原子铂催化剂相比于Pt颗粒催化剂,优点有
Ⅲ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图2为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的
 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。
(5)该装置可以生成大量氧化性更强的
 ,
, 去除
去除 的离子方程式为
的离子方程式为(6)相比于传统的二维电极反应系统,三维电极的优点有
您最近一年使用:0次
名校
4 . 肼( )有较强的还原性,与
)有较强的还原性,与 等可组成火箭推进剂。
等可组成火箭推进剂。
(1)已知:Ⅰ.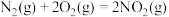

Ⅱ.
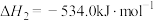
Ⅲ.

火箭发射时 与
与 反应生成
反应生成 和
和 。该反应的热化学方程式是
。该反应的热化学方程式是___________ 。
(2)肼的传统生产工艺为Raschig法,两步反应分别在不同容器的水溶液环境中进行:
i.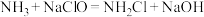 (快)
(快)
ii.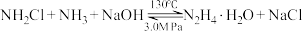 (慢)
(慢)
已知电负性N>Cl。下列说法正确的是___________ (填序号)。
a.反应i中NaClO做氧化剂
b.适当提高反应i温度,可显著提高相同时间内 的产量
的产量
c.采用3.0MPa压强可以增大 的溶解度,提高反应ii中
的溶解度,提高反应ii中 的利用率
的利用率
(3)采用Raschig法制得肼后,可采用分步蒸馏的方法将其从反应混合液中分离出来。
①水合肼( ,常温为液态)中
,常温为液态)中 与
与 间存在氢键,用“X-H…Y”表示
间存在氢键,用“X-H…Y”表示 与
与 间存在的氢键:
间存在的氢键:___________ 。
②蒸馏过程中首先馏出的物质是___________ (填序号)。
a. b.
b. c.NaCl
c.NaCl
(4)产品中肼含量的测定方法如下。
取0.50g产品加20mL水稀释,滴入2滴淀粉溶液,用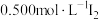 溶液滴定3次,平均每次消耗
溶液滴定3次,平均每次消耗 溶液20.00mL。已知:
溶液20.00mL。已知: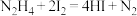
①样品中肼(以 计)的质量分数为
计)的质量分数为___________ 。
②若滴定过程中操作过于缓慢,则测定结果___________ (填“偏大”“偏小”或“不受影响”)。
(5)肼除做火箭推进剂外还可用于燃料电池中。某种碱性肼-空气燃料电池(电解质为KOH溶液)具有高效、无污染的特点,装置如右图所示。___________ 。
②电池工作一段时间后正极区KOH溶液pH基本保持不变,结合电极反应式解释原因___________ 。
 )有较强的还原性,与
)有较强的还原性,与 等可组成火箭推进剂。
等可组成火箭推进剂。(1)已知:Ⅰ.
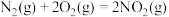

Ⅱ.

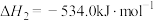
Ⅲ.


火箭发射时
 与
与 反应生成
反应生成 和
和 。该反应的热化学方程式是
。该反应的热化学方程式是(2)肼的传统生产工艺为Raschig法,两步反应分别在不同容器的水溶液环境中进行:
i.
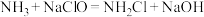 (快)
(快)ii.
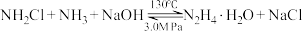 (慢)
(慢)已知电负性N>Cl。下列说法正确的是
a.反应i中NaClO做氧化剂
b.适当提高反应i温度,可显著提高相同时间内
 的产量
的产量c.采用3.0MPa压强可以增大
 的溶解度,提高反应ii中
的溶解度,提高反应ii中 的利用率
的利用率(3)采用Raschig法制得肼后,可采用分步蒸馏的方法将其从反应混合液中分离出来。
①水合肼(
 ,常温为液态)中
,常温为液态)中 与
与 间存在氢键,用“X-H…Y”表示
间存在氢键,用“X-H…Y”表示 与
与 间存在的氢键:
间存在的氢键:②蒸馏过程中首先馏出的物质是
a.
 b.
b. c.NaCl
c.NaCl(4)产品中肼含量的测定方法如下。
取0.50g产品加20mL水稀释,滴入2滴淀粉溶液,用
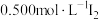 溶液滴定3次,平均每次消耗
溶液滴定3次,平均每次消耗 溶液20.00mL。已知:
溶液20.00mL。已知: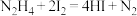
①样品中肼(以
 计)的质量分数为
计)的质量分数为②若滴定过程中操作过于缓慢,则测定结果
(5)肼除做火箭推进剂外还可用于燃料电池中。某种碱性肼-空气燃料电池(电解质为KOH溶液)具有高效、无污染的特点,装置如右图所示。
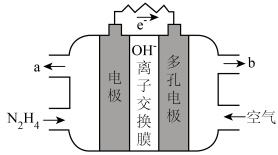
②电池工作一段时间后正极区KOH溶液pH基本保持不变,结合电极反应式解释原因
您最近一年使用:0次
名校
解题方法
5 . 肼(N2H4)有较强的还原性,与N2O4等可组成火箭推进剂。
(1)已知:I.N2(g)+2O2(g)=2NO2(g) ΔH1=-67.7kJ·mol-1
Ⅱ.N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.0kJ·mol-1
Ⅲ.NO2(g)
 N2O4(g) ΔH3=-26.4kJ·mol-1
N2O4(g) ΔH3=-26.4kJ·mol-1
火箭发射时N2H4与N2O4反应生成N2和H2O。该反应的热化学方程式是___________ 。
(2)肼的传统生产工艺为Raschig法,两步反应分别在不同容器的水溶液环境中进行:
i.NH3+NaClO=NH2Cl+NaOH (快)
ii.NH2Cl+NH3+NaOH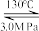 N2H4·H2O+NaCl (慢)
N2H4·H2O+NaCl (慢)
已知电负性N>Cl。下列说法正确的是___________ (填序号)。
a.反应i中NaClO做氧化剂
b.适当提高反应i温度,可显著提高相同时间内N2H4·H2O的产量
c.采用3.0MPa压强可以增大NH3的溶解度,提高反应ii中NH2Cl的利用率
(3)采用Raschig法制得肼后,可采用分步蒸馏的方法将其从反应混合液中分离出来。蒸馏过程中首先馏出的物质是___________ (填序号)。
a.NH3 b.N2H4·H2O c.NaCl
(4)产品中肼含量的测定方法如下。
取0.50g产品加20mL水稀释,滴入2滴淀粉溶液,用0.500mol·L-1 溶液滴定3次,平均每次消耗
溶液滴定3次,平均每次消耗 溶液20.00 mL。
溶液20.00 mL。
已知:N2H4+2 =4HI+N2。
=4HI+N2。
①样品中肼(以N2H4计)的质量分数为___________ 。
②若滴定过程中操作过于缓慢,则测定结果___________ (填“偏大”“偏小”“不受影响”)。
(5)肼除做火箭推进剂外还可用于燃料电池中。某种碱性肼-空气燃料电池(电解质为KOH溶液)具有高效、无污染的特点,装置如图所示。
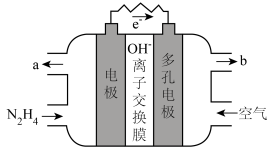
① 负极的电极反应式是___________ 。
② 电池工作一段时间后正极区KOH溶液pH基本保持不变,结合电极反应式解释原因___________ 。
(1)已知:I.N2(g)+2O2(g)=2NO2(g) ΔH1=-67.7kJ·mol-1
Ⅱ.N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.0kJ·mol-1
Ⅲ.NO2(g)

 N2O4(g) ΔH3=-26.4kJ·mol-1
N2O4(g) ΔH3=-26.4kJ·mol-1火箭发射时N2H4与N2O4反应生成N2和H2O。该反应的热化学方程式是
(2)肼的传统生产工艺为Raschig法,两步反应分别在不同容器的水溶液环境中进行:
i.NH3+NaClO=NH2Cl+NaOH (快)
ii.NH2Cl+NH3+NaOH
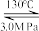 N2H4·H2O+NaCl (慢)
N2H4·H2O+NaCl (慢)已知电负性N>Cl。下列说法正确的是
a.反应i中NaClO做氧化剂
b.适当提高反应i温度,可显著提高相同时间内N2H4·H2O的产量
c.采用3.0MPa压强可以增大NH3的溶解度,提高反应ii中NH2Cl的利用率
(3)采用Raschig法制得肼后,可采用分步蒸馏的方法将其从反应混合液中分离出来。蒸馏过程中首先馏出的物质是
a.NH3 b.N2H4·H2O c.NaCl
(4)产品中肼含量的测定方法如下。
取0.50g产品加20mL水稀释,滴入2滴淀粉溶液,用0.500mol·L-1
 溶液滴定3次,平均每次消耗
溶液滴定3次,平均每次消耗 溶液20.00 mL。
溶液20.00 mL。已知:N2H4+2
 =4HI+N2。
=4HI+N2。①样品中肼(以N2H4计)的质量分数为
②若滴定过程中操作过于缓慢,则测定结果
(5)肼除做火箭推进剂外还可用于燃料电池中。某种碱性肼-空气燃料电池(电解质为KOH溶液)具有高效、无污染的特点,装置如图所示。

① 负极的电极反应式是
② 电池工作一段时间后正极区KOH溶液pH基本保持不变,结合电极反应式解释原因
您最近一年使用:0次
名校
解题方法
6 .  分子结构稳定,难以给出电子,较容易接受电子,较难活化。采用
分子结构稳定,难以给出电子,较容易接受电子,较难活化。采用 作为碳源,通过
作为碳源,通过 催化加氢方式,不仅可以减少温室气体的排放,还可以将
催化加氢方式,不仅可以减少温室气体的排放,还可以将 转化为高附加值的化学产品,具有重要的战略意义。
转化为高附加值的化学产品,具有重要的战略意义。
(1) 的结构与
的结构与 相似,写出
相似,写出 的电子式
的电子式_______ 。
(2)一种 直接加氢的反应机理如图a所示。
直接加氢的反应机理如图a所示。

①写出总反应的化学方程式_______ 。
②a、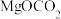 也可以写成
也可以写成 (难溶),写出
(难溶),写出 溶于乙酸的离子方程式
溶于乙酸的离子方程式_______ ;
b、 比
比 更难溶,加热
更难溶,加热 的水溶液可以生成
的水溶液可以生成 ,写出反应的化学方程式
,写出反应的化学方程式_______ 。
(3)①已知:主反应 催化加氢制甲醇是放热反应
催化加氢制甲醇是放热反应

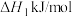

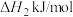
写出 催化加氢制甲醇的热化学方程式
催化加氢制甲醇的热化学方程式_______ ( 用含
用含 和
和 的代数式表示)。
的代数式表示)。
②已知
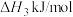 ,则
,则
_______  (填>、<或=)。
(填>、<或=)。
③我国科学家设计了离子液体电还原 合成
合成 工艺,写出碱性条件下
工艺,写出碱性条件下 生成甲醇的电极反应式
生成甲醇的电极反应式_______ 。
 分子结构稳定,难以给出电子,较容易接受电子,较难活化。采用
分子结构稳定,难以给出电子,较容易接受电子,较难活化。采用 作为碳源,通过
作为碳源,通过 催化加氢方式,不仅可以减少温室气体的排放,还可以将
催化加氢方式,不仅可以减少温室气体的排放,还可以将 转化为高附加值的化学产品,具有重要的战略意义。
转化为高附加值的化学产品,具有重要的战略意义。(1)
 的结构与
的结构与 相似,写出
相似,写出 的电子式
的电子式(2)一种
 直接加氢的反应机理如图a所示。
直接加氢的反应机理如图a所示。
①写出总反应的化学方程式
②a、
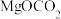 也可以写成
也可以写成 (难溶),写出
(难溶),写出 溶于乙酸的离子方程式
溶于乙酸的离子方程式b、
 比
比 更难溶,加热
更难溶,加热 的水溶液可以生成
的水溶液可以生成 ,写出反应的化学方程式
,写出反应的化学方程式(3)①已知:主反应
 催化加氢制甲醇是放热反应
催化加氢制甲醇是放热反应
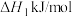

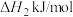
写出
 催化加氢制甲醇的热化学方程式
催化加氢制甲醇的热化学方程式 用含
用含 和
和 的代数式表示)。
的代数式表示)。②已知

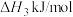 ,则
,则
 (填>、<或=)。
(填>、<或=)。③我国科学家设计了离子液体电还原
 合成
合成 工艺,写出碱性条件下
工艺,写出碱性条件下 生成甲醇的电极反应式
生成甲醇的电极反应式
您最近一年使用:0次
2022-06-19更新
|
146次组卷
|
2卷引用:北京市第十二中学2021-2022学年高一下学期6月月考化学试题
7 . CO2分子结构稳定,难以给出电子,较容易接受电子,较难活化。采用CO2作为碳源,通过CO2催化加氢方式,不仅可以减少温室气体的排放,还可以将CO2转化为高附加值的化学产品,具有重要的战略意义。
(1)若活化CO2,通常需要采取适当的方式使CO2的分子结构从_______ (填分子的空间结构名称)变为弯曲型,便于下一步反应。
(2)一种CO2直接加氢的反应机理如图a所示。

①写出总反应的化学方程式_______ 。
②MgOCO2也可以写成MgCO3,写出CO 的VSEPR模型名称
的VSEPR模型名称_______ 。
(3)①已知:主反应CO2催化加氢制甲醇是放热反应
2H2(g)+O2(g)=2H2O(g) ΔH1
2CH3OH(g)+3O2(g)=4H2O(g)+2CO2(g) ΔH2
写出CO2催化加氢制甲醇的热化学方程式_______ (ΔH用含ΔH1和ΔH2的代数式表示)。
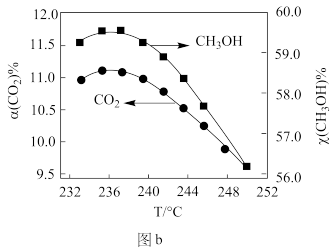
②CO2催化加氢制甲醇过程中的主要竞争反应为:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41kJ/mol,在恒温密闭容器中,维持压强和投料不变,将CO2和H2按一定流速通过反应器,CO2转化率和CH3OH选择性[x(CH3OH)%=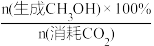 ]随温度变化关系如图b所示,分析236℃以后,图b中曲线下降的原因
]随温度变化关系如图b所示,分析236℃以后,图b中曲线下降的原因_______ 。
③我国科学家设计了离子液体电还原CO2合成CH3OH工艺,写出碱性条件下CO2生成甲醇的电极反应式_______ 。
(1)若活化CO2,通常需要采取适当的方式使CO2的分子结构从
(2)一种CO2直接加氢的反应机理如图a所示。

①写出总反应的化学方程式
②MgOCO2也可以写成MgCO3,写出CO
 的VSEPR模型名称
的VSEPR模型名称(3)①已知:主反应CO2催化加氢制甲醇是放热反应
2H2(g)+O2(g)=2H2O(g) ΔH1
2CH3OH(g)+3O2(g)=4H2O(g)+2CO2(g) ΔH2
写出CO2催化加氢制甲醇的热化学方程式
②CO2催化加氢制甲醇过程中的主要竞争反应为:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41kJ/mol,在恒温密闭容器中,维持压强和投料不变,将CO2和H2按一定流速通过反应器,CO2转化率和CH3OH选择性[x(CH3OH)%=
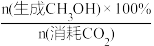 ]随温度变化关系如图b所示,分析236℃以后,图b中曲线下降的原因
]随温度变化关系如图b所示,分析236℃以后,图b中曲线下降的原因
③我国科学家设计了离子液体电还原CO2合成CH3OH工艺,写出碱性条件下CO2生成甲醇的电极反应式
您最近一年使用:0次
名校
8 . 将天然气(主要成分为CH4)中的CO2、H2S资源化转化在能源利用、环境保护等方面意义重大。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=-530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是___________
(2)CO2性质稳定,是一种“惰性”分子。对于反应iii,通过设计合适的催化剂可以降低___________ ,提高反应速率。
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应iii,工作原理如下所示。
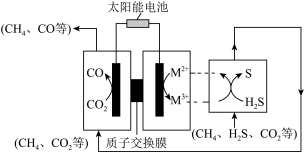
【方案1】若M3+/M2+=Fe3+/Fe2+。为了抑制离子水解,所含Fe3+、Fe2+的溶液调为较强的酸性。
①写出阳极区生成S的电极反应和离子方程式___________ 。
②结合电极反应和离子移动解释阴极区pH不变的原因(忽略溶液体积变化)___________
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+ (配合物)。
已知:电解效率η的定义:
η(B)=n(生成B所用的电子)/ n(通过电极的电子)×100%
③测得η(EDTA-Fe3+)≈100%,η(CO) ≈80%。阴极放电的物质有___________
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1.CO2通过电极反应产生CO
来源2.电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是___________ 。
方案2明显优于方案1.该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=-530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是
(2)CO2性质稳定,是一种“惰性”分子。对于反应iii,通过设计合适的催化剂可以降低
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应iii,工作原理如下所示。

【方案1】若M3+/M2+=Fe3+/Fe2+。为了抑制离子水解,所含Fe3+、Fe2+的溶液调为较强的酸性。
①写出阳极区生成S的电极反应和离子方程式
②结合电极反应和离子移动解释阴极区pH不变的原因(忽略溶液体积变化)
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+ (配合物)。
已知:电解效率η的定义:
η(B)=n(生成B所用的电子)/ n(通过电极的电子)×100%
③测得η(EDTA-Fe3+)≈100%,η(CO) ≈80%。阴极放电的物质有
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1.CO2通过电极反应产生CO
来源2.电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是
方案2明显优于方案1.该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
您最近一年使用:0次
9 . 将天然气(主要成分为CH4)中的CO2、H2S资源化转化在能源利用、环境保护等方面意义重大。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=﹣530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是___________ 。
(2)CO2性质稳定,是一种“惰性”分子。对于反应ⅲ,通过设计合适的催化剂可以降低______ ,提高反应速率。
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应ⅲ,工作原理如下所示。
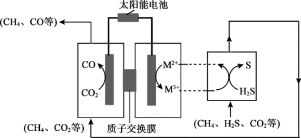
【方案1】若M3+/M2+=Fe3+/Fe2+
①所含Fe3+、Fe2+的溶液需为较强的酸性,原因是___________ 。
②结合反应式说明生成S、CO的原理:___________ 。
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+(配合物)
已知:电解效率η的定义:
③测得η(EDTA-Fe3+)≈100%,η(CO)≈80%。阴极放电的物质有___________ 。
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1:CO2通过电极反应产生CO
来源2:电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是___________ 。
结论:方案2明显优于方案1,该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=﹣530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是
(2)CO2性质稳定,是一种“惰性”分子。对于反应ⅲ,通过设计合适的催化剂可以降低
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应ⅲ,工作原理如下所示。

【方案1】若M3+/M2+=Fe3+/Fe2+
①所含Fe3+、Fe2+的溶液需为较强的酸性,原因是
②结合反应式说明生成S、CO的原理:
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+(配合物)
已知:电解效率η的定义:

③测得η(EDTA-Fe3+)≈100%,η(CO)≈80%。阴极放电的物质有
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1:CO2通过电极反应产生CO
来源2:电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是
结论:方案2明显优于方案1,该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
您最近一年使用:0次
2022-01-16更新
|
387次组卷
|
3卷引用:北京市朝阳区2021-2022学年高三上学期期末考试化学试题
解题方法
10 . 人类向大气中排放的NOx对环境会产生危害,脱除NOx是科学家研究的重要课题。
(1) NOx对环境的一种危害是____ 。
(2) NH3还原法可将NOx还原为N2进行脱除。
已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H1=-1530kJ/mol
N2(g)+O2(g)=2NO(g)△H2=+180kJ/mol
写出NH3还原NO反应的热化学方程式:____ 。
(3)碱性KMnO4氧化法也可将NOx进行脱除。
①用KMnO4(NaOH)溶液进行烟气中NO的脱除,将该离子方程式补充完整。____ NO+____ MnO4-+____ =NO2-+3NO3-+__ MnO42-+______
②下列叙述正确的是____ (填字母序号)。
A.将脱除后的混合溶液进行分离可获得氮肥
B.反应后混合溶液中:c( MnO4-)+2c(MnO42-)=c(K+)
C.在不同酸碱性条件下,KMnO4发生氧化还原反应的产物可能不同
③在实验室用KMnO4 ( NaOH)溶液对模拟烟气中的NO进行脱除。若将标准状况下224 L含NO体积分数为10%的模拟烟气进行处理,假设NO最终全部转化为NO3-,理论上需要KMnO4的质量为____ g(KMnO4摩尔质量为158 g·mol-l)。
(4)用Pl-g-C3N4光催化氧化法脱除NO的过程如下图所示。

①该脱除过程中,太阳能转化为___ 能。
②在酸性水溶液中,光催化脱除原理和电化学反应原理类似。g-C3N4端的反应:O2+2H++2e-=H2O2;Pl端的反应:___ ;NO2最终转化为HNO3的化学方程式:___________ 。
(1) NOx对环境的一种危害是
(2) NH3还原法可将NOx还原为N2进行脱除。
已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H1=-1530kJ/mol
N2(g)+O2(g)=2NO(g)△H2=+180kJ/mol
写出NH3还原NO反应的热化学方程式:
(3)碱性KMnO4氧化法也可将NOx进行脱除。
①用KMnO4(NaOH)溶液进行烟气中NO的脱除,将该离子方程式补充完整。
②下列叙述正确的是
A.将脱除后的混合溶液进行分离可获得氮肥
B.反应后混合溶液中:c( MnO4-)+2c(MnO42-)=c(K+)
C.在不同酸碱性条件下,KMnO4发生氧化还原反应的产物可能不同
③在实验室用KMnO4 ( NaOH)溶液对模拟烟气中的NO进行脱除。若将标准状况下224 L含NO体积分数为10%的模拟烟气进行处理,假设NO最终全部转化为NO3-,理论上需要KMnO4的质量为
(4)用Pl-g-C3N4光催化氧化法脱除NO的过程如下图所示。

①该脱除过程中,太阳能转化为
②在酸性水溶液中,光催化脱除原理和电化学反应原理类似。g-C3N4端的反应:O2+2H++2e-=H2O2;Pl端的反应:
您最近一年使用:0次



