1 . Bi、In及BiIn合金均可催化 (g)和
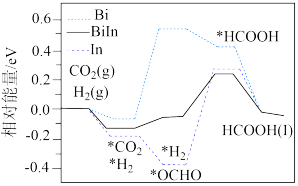
(g)和 (g)合成,其相对能量变化如图(带“*”表示物质处于吸附态)。下列说法正确的是
(g)合成,其相对能量变化如图(带“*”表示物质处于吸附态)。下列说法正确的是
 (g)和
(g)和 (g)合成,其相对能量变化如图(带“*”表示物质处于吸附态)。下列说法正确的是
(g)合成,其相对能量变化如图(带“*”表示物质处于吸附态)。下列说法正确的是
A. (g)和 (g)和 (g)合成HCOOH(l)的反应为吸热反应 (g)合成HCOOH(l)的反应为吸热反应 |
| B.催化效果最好的金属为BiIn合金 |
C. 和 和 在催化剂表面吸附的过程需吸收能量 在催化剂表面吸附的过程需吸收能量 |
| D.温度一定时,增大压强无法提高原料的平衡转化率 |
您最近一年使用:0次
解题方法
2 . 1905年哈伯实现了以氨气和氢气为原料合成氨气,生产的氮制造氨肥服务于农业,养活了地球三分之一的人口,哈伯也因此获得了1918年的诺贝尔化学奖。一百多年过去了,对合成氨的研究依然没有止步。
(1)工业合成氨的反应如下: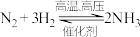 。已知断裂1mol
。已知断裂1mol  中的共价键吸收的能量为946kJ,断裂1mol
中的共价键吸收的能量为946kJ,断裂1mol  中的共价键吸收的能量为436kJ,形成1mol N—H键放出的能量为391kJ,则由
中的共价键吸收的能量为436kJ,形成1mol N—H键放出的能量为391kJ,则由 和
和 生成2mol
生成2mol 的能量变化为
的能量变化为_______ kJ。下图能正确表示该反应中能量变化的是_______ (填“A”或“B”)。
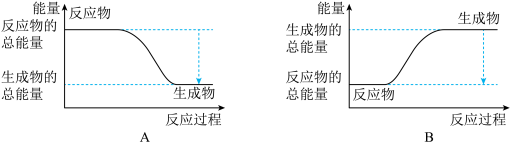
(2)反应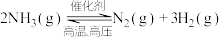 在三种不同条件下进行,
在三种不同条件下进行, 、
、 的起始浓度为0,反应物
的起始浓度为0,反应物 的浓度
的浓度 随时间(min)的变化情况如下表所示。
随时间(min)的变化情况如下表所示。
根据上表数据回答:
①实验I、II中,有一个实验使用了催化剂,它是实验_______ (填序号);在实验Ⅱ中,从0~20min用 表示的速率
表示的速率
_______  。
。
②在不同条件下进行的氨的分解反应。根据在相同时间内测定的结果,判断该反应的速率由大到小的顺序是_______ (填字母)。
A. B.
B.
C. D.
D.
③在恒温恒容条件下,判断该反应达到化学平衡状态的标志是_______ (填字母)。
a. 的正反应速率等于逆反应速率 b.混合气体的密度不变
的正反应速率等于逆反应速率 b.混合气体的密度不变
c.混合气体的压强不变 d.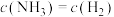
(1)工业合成氨的反应如下:
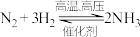 。已知断裂1mol
。已知断裂1mol  中的共价键吸收的能量为946kJ,断裂1mol
中的共价键吸收的能量为946kJ,断裂1mol  中的共价键吸收的能量为436kJ,形成1mol N—H键放出的能量为391kJ,则由
中的共价键吸收的能量为436kJ,形成1mol N—H键放出的能量为391kJ,则由 和
和 生成2mol
生成2mol 的能量变化为
的能量变化为
(2)反应
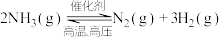 在三种不同条件下进行,
在三种不同条件下进行, 、
、 的起始浓度为0,反应物
的起始浓度为0,反应物 的浓度
的浓度 随时间(min)的变化情况如下表所示。
随时间(min)的变化情况如下表所示。| 序号 | 温度 | 时间 | ||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | ||
| I | 400℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| II | 400℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| III | 500℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上表数据回答:
①实验I、II中,有一个实验使用了催化剂,它是实验
 表示的速率
表示的速率
 。
。②在不同条件下进行的氨的分解反应。根据在相同时间内测定的结果,判断该反应的速率由大到小的顺序是
A.
 B.
B.
C.
 D.
D.
③在恒温恒容条件下,判断该反应达到化学平衡状态的标志是
a.
 的正反应速率等于逆反应速率 b.混合气体的密度不变
的正反应速率等于逆反应速率 b.混合气体的密度不变c.混合气体的压强不变 d.
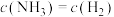
您最近一年使用:0次
名校
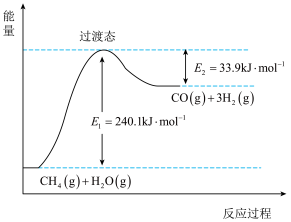
3 . 甲烷在自然界的分布很广,是天然气、沼气、煤矿坑道气的主要成分,它可用来作为燃料以及制造合成气、炭黑等物质的原料。甲烷用于生产合成气的反应为 。请回答下列问题:
。请回答下列问题:
(1)反应过程中的能量变化如下图所示,1mol 参加反应时
参加反应时___________ (填“吸收”或“放出”)的能量为___________ kJ。
(2)T℃时,向2L恒容密闭容器中投入1mol 和1mol
和1mol ,发生反应:
,发生反应:
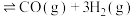 ,经过5min,反应达到平衡,已知平衡时
,经过5min,反应达到平衡,已知平衡时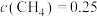 mol∙L
mol∙L 。
。
①0~5min内,该反应的平均反应速率
___________ ,平衡时CO的物质的量为___________ 。
②下列表述能说明该反应达到化学平衡状态的是___________ 。
a.反应速率
b. 的物质的量浓度不再改变
的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内断裂1molH—O键同时断裂3molH—H键
(3)科学家利用甲烷生产的合成气,发明了一种以熔融碳酸盐为离子导体的新型燃料电池,工作原理如下图所示。
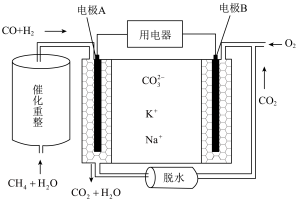
内电路中阴离子向电极___________ (填A或B)移动,试写出B电极的电极反应式___________ 。
 。请回答下列问题:
。请回答下列问题:(1)反应过程中的能量变化如下图所示,1mol
 参加反应时
参加反应时
(2)T℃时,向2L恒容密闭容器中投入1mol
 和1mol
和1mol ,发生反应:
,发生反应:
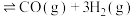 ,经过5min,反应达到平衡,已知平衡时
,经过5min,反应达到平衡,已知平衡时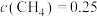 mol∙L
mol∙L 。
。①0~5min内,该反应的平均反应速率

②下列表述能说明该反应达到化学平衡状态的是
a.反应速率

b.
 的物质的量浓度不再改变
的物质的量浓度不再改变c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内断裂1molH—O键同时断裂3molH—H键
(3)科学家利用甲烷生产的合成气,发明了一种以熔融碳酸盐为离子导体的新型燃料电池,工作原理如下图所示。

内电路中阴离子向电极
您最近一年使用:0次
名校
4 . 化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是__ (填字母)。
A.Na2O与水反应 B.甲烷的燃烧反应
C.Ba(OH)2·8H2O与氯化铵反应 D.锌与盐酸反应
(2)获取能量变化的途径通过化学键的键能计算。已知:
计算可得:H2(g)+Cl2(g)=2HCl(g)△H=__ kJ·mol-1。
(3)以CO(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。

某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。
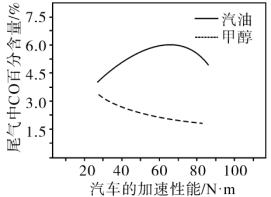
据图信息分析,与汽油相比,甲醇作为燃料的优点是__ 。
(1)下列反应中,属于吸热反应的是
A.Na2O与水反应 B.甲烷的燃烧反应
C.Ba(OH)2·8H2O与氯化铵反应 D.锌与盐酸反应
(2)获取能量变化的途径通过化学键的键能计算。已知:
| 化学键种类 | H—H | Cl—Cl | H—Cl |
| 键能(kJ/mol) | 436 | 247 | 434 |
计算可得:H2(g)+Cl2(g)=2HCl(g)△H=
(3)以CO(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。

某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。

据图信息分析,与汽油相比,甲醇作为燃料的优点是
您最近一年使用:0次
名校
5 . 化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是___________ (填字母)。
A.Na2O与水反应 B.甲烷的燃烧反应
C.Ba(OH)2·8H2O与氯化铵反应 D.锌与盐酸反应
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
计算可得:H2(g)+Cl2(g)=2HCl(g) △H= ___________ kJ·mol-1
②通过盖斯定律可计算。已知在25℃、101 kPa时:
I.2Na(s)+ O2(g)=Na2O(s) △H=-414 kJ·mol-1
O2(g)=Na2O(s) △H=-414 kJ·mol-1
II.2Na(s)+O2(g)=Na2O2(s) △H=-511 kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式:___________ 。
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。
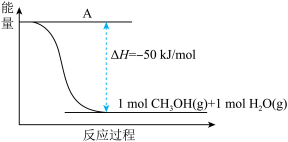
①补全上图:图中A处应填入___________ 。
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的△H___________ (填“变大”“变小”或“不变” )。
)。
③某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。
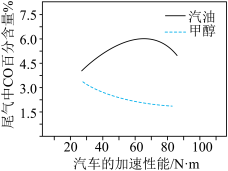
据图信息分析,与汽油相比,甲醇作为燃料的优点是___________ 。
(1)下列反应中,属于吸热反应的是
A.Na2O与水反应 B.甲烷的燃烧反应
C.Ba(OH)2·8H2O与氯化铵反应 D.锌与盐酸反应
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
| 化学键种类 | H-H | Cl-Cl | H-Cl |
| 键能(kJ/mol) | 436 | 247 | 434 |
②通过盖斯定律可计算。已知在25℃、101 kPa时:
I.2Na(s)+
 O2(g)=Na2O(s) △H=-414 kJ·mol-1
O2(g)=Na2O(s) △H=-414 kJ·mol-1II.2Na(s)+O2(g)=Na2O2(s) △H=-511 kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式:
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。

①补全上图:图中A处应填入
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的△H
 )。
)。③某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。

据图信息分析,与汽油相比,甲醇作为燃料的优点是
您最近一年使用:0次
2021-01-28更新
|
458次组卷
|
6卷引用:湖北省部分高中2020-2021学年高二上学期期中考试化学试题



