1 . 生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面___________ (填字母)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水
(3)已知:2mol H2 与足量O2充分燃烧生成液态水时放出 572kJ 热量。
①该反应的能量变化可用图中的___________ (填字母)表示。

②写出H2 燃烧生成液态水的热化学反应方程式:___________ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
A.生石灰和水 B.浓硫酸和水
(3)已知:2mol H2 与足量O2充分燃烧生成液态水时放出 572kJ 热量。
①该反应的能量变化可用图中的

②写出H2 燃烧生成液态水的热化学反应方程式:
您最近一年使用:0次
2 . 化学反应原理在生产、生活中用途广泛。氮是地球上含量丰富的一种元素,氮及其化合物对我们的生产、生活有重要的影响。请回答下列问题:
(1)机动车发动机工作时会引发 与
与 的反应(如图所示),请用热化学方程式表示以下反应
的反应(如图所示),请用热化学方程式表示以下反应___________ 。
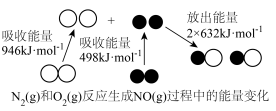
(2)已知
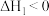 ,
,
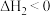 ,下列能量变化示意图中,正确的是___________。
,下列能量变化示意图中,正确的是___________。
(1)机动车发动机工作时会引发
 与
与 的反应(如图所示),请用热化学方程式表示以下反应
的反应(如图所示),请用热化学方程式表示以下反应
(2)已知

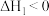 ,
,
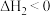 ,下列能量变化示意图中,正确的是___________。
,下列能量变化示意图中,正确的是___________。A.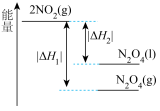 | B.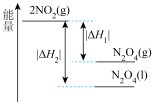 |
C.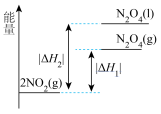 | D.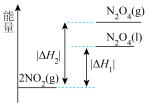 |
您最近一年使用:0次
3 . 陈述I和Ⅱ均正确且具有因果关系的是
| 选项 | 陈述I | 陈述Ⅱ |
| A | 硝酸铵与水合碳酸钠可用于制作冰敷袋 | 该反应的反应物总能量高于生成物总能量 |
| B | 不锈钢性质比较稳定、不易生锈、用途广泛 | 不锈钢硬度、熔点均比纯铁大 |
| C | 原生铜的硫化物经氧化、淋滤渗透与 可生成 可生成 |  具有氧化性 具有氧化性 |
| D | 成熟苹果的汁液能与银氨溶液反应 | 成熟的苹果汁液中含有葡萄糖 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 从物质分类的角度看, 和
和 都属于氧化物,但二者的性质存在很大差异。查阅资料得知,
都属于氧化物,但二者的性质存在很大差异。查阅资料得知, 可在呼吸面具和潜水艇中做供氧剂,某实验小组欲通过实验探究
可在呼吸面具和潜水艇中做供氧剂,某实验小组欲通过实验探究 的性质与用途。
的性质与用途。
【实验I】探究 与水的反应
与水的反应
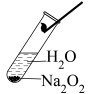
(1)如图,将1~2mL水滴入盛有1~2g过氧化钠固体的试管中,立即把带火星的小木条伸入试管中,观察到带火星的小木条复燃,说明生成了______ ,用手触摸试管外壁,感觉发烫,说明该反应是______ (填“吸热”或“放热”)反应。用pH计测得溶液呈碱性,说明该反应还生成了______ 。
【实验II】探究 与
与 的反应
的反应
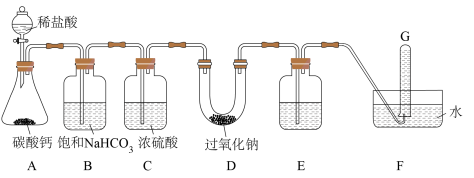
(2)装置A用于制备______ 气体,盛装稀盐酸的仪器名称是______ 。
(3)装置B的作用是______ 。
(4)写出D中发生反应的化学方程式:______ 。
(5)装置E的作用是除去过量的 ,则装置E中盛装的试剂是
,则装置E中盛装的试剂是______ 。
(6)G中得到的物质是______ ,证明 可用作呼吸面具和潜水艇的供氧剂。
可用作呼吸面具和潜水艇的供氧剂。
 和
和 都属于氧化物,但二者的性质存在很大差异。查阅资料得知,
都属于氧化物,但二者的性质存在很大差异。查阅资料得知, 可在呼吸面具和潜水艇中做供氧剂,某实验小组欲通过实验探究
可在呼吸面具和潜水艇中做供氧剂,某实验小组欲通过实验探究 的性质与用途。
的性质与用途。【实验I】探究
 与水的反应
与水的反应
(1)如图,将1~2mL水滴入盛有1~2g过氧化钠固体的试管中,立即把带火星的小木条伸入试管中,观察到带火星的小木条复燃,说明生成了
【实验II】探究
 与
与 的反应
的反应
(2)装置A用于制备
(3)装置B的作用是
(4)写出D中发生反应的化学方程式:
(5)装置E的作用是除去过量的
 ,则装置E中盛装的试剂是
,则装置E中盛装的试剂是(6)G中得到的物质是
 可用作呼吸面具和潜水艇的供氧剂。
可用作呼吸面具和潜水艇的供氧剂。
您最近一年使用:0次
5 . 冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途,下列物质可用作冷敷袋中试剂的是
| A.生石灰和水 | B.烧碱和水 | C.硝酸铵和水 | D.浓硫酸和水 |
您最近一年使用:0次
2023-06-14更新
|
106次组卷
|
4卷引用:青海省海东市2022-2023学年高一下学期6月联考化学试题
6 . 化学是一门实用性很强的科学,请根据题意填空:
(1)运输浓硫酸和浓硝酸常用铝罐车,试解释其原因:___________ 。
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是___________ (填化学式)。
(3)常用的打火机中充有丁烷, 的一氯代物有
的一氯代物有___________ 种,分子式为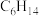 的长链(无支链)有机物的名称为
的长链(无支链)有机物的名称为___________ 。
(4)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(5)航天技术上使用的氢氧燃料电池具有高能、轻便和不污染环境等优点。氢氧燃料电池(简化装置如图)有酸式和碱式两种,它们放电时的电池总反应式都可表示为 。
。
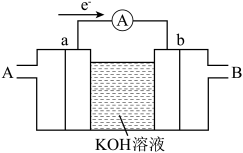
①碱式氢氧燃料电池的电解质溶液是 溶液,其正极的电极反应式为
溶液,其正极的电极反应式为___________ 。
②电池工作时,A极通入的是___________ 。
③电池工作时每消耗标准状况下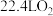 ,电路中转移电子的数目为
,电路中转移电子的数目为___________  。
。
(1)运输浓硫酸和浓硝酸常用铝罐车,试解释其原因:
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(3)常用的打火机中充有丁烷,
 的一氯代物有
的一氯代物有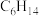 的长链(无支链)有机物的名称为
的长链(无支链)有机物的名称为(4)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(5)航天技术上使用的氢氧燃料电池具有高能、轻便和不污染环境等优点。氢氧燃料电池(简化装置如图)有酸式和碱式两种,它们放电时的电池总反应式都可表示为
 。
。
①碱式氢氧燃料电池的电解质溶液是
 溶液,其正极的电极反应式为
溶液,其正极的电极反应式为②电池工作时,A极通入的是
③电池工作时每消耗标准状况下
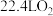 ,电路中转移电子的数目为
,电路中转移电子的数目为 。
。
您最近一年使用:0次
名校
7 . Ⅰ.肼(N2H4)是一种重要的化工产品,有广泛用途,常用于火箭推进剂和燃料电池。回答下列问题:
(1)N2H4的电子式为________ 。
(2)已知N2H4(g)+O2(g)=N2(g)+2H2O(g)的能量变化如图所示:
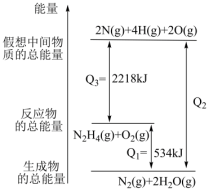
①则该反应为______ (填“吸热反应”或“放热反应”)。
②2molN原子、4molH原子、2molO原子生成1molN2(g)和2molH2O(g)的过程中放出_____ kJ能量。
Ⅱ.“绿色办奥”是北京冬奥会四大办奥理念之首,在“双碳”目标驱动下,全球首次服务体育赛事的大批量氢燃料客车在北京冬奥会上闪亮登场。工作原理如图所示:
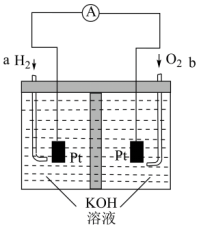
(3)氢燃料电池工作时H2从______ (填“正极”或“负极”)通入。
(4)负极发生的反应方程式为_______ 。
(5)溶液中OH-向_____ 电极(填“a”或“b”)移动。
(6)当有16g气体被还原时,回路中转移的电子数为_____ 。
(1)N2H4的电子式为
(2)已知N2H4(g)+O2(g)=N2(g)+2H2O(g)的能量变化如图所示:

①则该反应为
②2molN原子、4molH原子、2molO原子生成1molN2(g)和2molH2O(g)的过程中放出
Ⅱ.“绿色办奥”是北京冬奥会四大办奥理念之首,在“双碳”目标驱动下,全球首次服务体育赛事的大批量氢燃料客车在北京冬奥会上闪亮登场。工作原理如图所示:

(3)氢燃料电池工作时H2从
(4)负极发生的反应方程式为
(5)溶液中OH-向
(6)当有16g气体被还原时,回路中转移的电子数为
您最近一年使用:0次
2024-01-06更新
|
51次组卷
|
2卷引用:四川省安岳中学2023-2024学年高三10月月考理科综合试题
解题方法
8 . Ⅰ.CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知CH3OH(g)+ O2(g)
O2(g) CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是_____ (填字母)。

a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1molH-O键断裂的同时2molC=O键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol•L-1,4min内平均反应速率v(H2)=_____ ,则CH3OH的转化率为______ 。
(3)已知断开1molH-H键吸收的能量为436kJ,形成1molH-N键放出的能量为391kJ,根据化学方程式N2+3H2=2NH3,反应完1molN2放出的能量为92.4kJ,则断开1molN≡N键需吸收的能量是_____ kJ。
Ⅱ.将等物质的量的A和B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),5min后测得c(D)=0.5mol•L-1,c(A)∶c(B)=1∶2,C的反应速率是0.15mol•L-1•min-1。
xC(g)+2D(g),5min后测得c(D)=0.5mol•L-1,c(A)∶c(B)=1∶2,C的反应速率是0.15mol•L-1•min-1。
(4)x=______ 。
(5)A在5min末的浓度是______ 。
(6)此时容器内的压强与开始时之比为______ 。
(1)已知CH3OH(g)+
 O2(g)
O2(g) CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1molH-O键断裂的同时2molC=O键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol•L-1,4min内平均反应速率v(H2)=
(3)已知断开1molH-H键吸收的能量为436kJ,形成1molH-N键放出的能量为391kJ,根据化学方程式N2+3H2=2NH3,反应完1molN2放出的能量为92.4kJ,则断开1molN≡N键需吸收的能量是
Ⅱ.将等物质的量的A和B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g)+2D(g),5min后测得c(D)=0.5mol•L-1,c(A)∶c(B)=1∶2,C的反应速率是0.15mol•L-1•min-1。
xC(g)+2D(g),5min后测得c(D)=0.5mol•L-1,c(A)∶c(B)=1∶2,C的反应速率是0.15mol•L-1•min-1。(4)x=
(5)A在5min末的浓度是
(6)此时容器内的压强与开始时之比为
您最近一年使用:0次
9 . 回答下列问题:
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。制作冷敷袋可以利用______(填序号,下同)。
(2)下列变化过程中放出热的是______ 。
①液态水汽化 ②稀释浓硫酸
③高温下碳酸钙分解 ④镁条与盐酸反应
⑤硝酸铵固体溶于水 ⑥铁丝在纯氧中燃烧
⑦氢氧化钾溶液与硝酸反应 ⑧八水合氢氧化钡固体与氯化铵固体混合搅拌
(3)下列变化:①碘的升华 ②烧碱熔化 ③氯化钠溶于水④氯化氢溶于水 ⑤氯气溶于水 ⑥氯化铵受热分解
未发生化学键破坏的是___________ ;仅发生离子键破坏的是___________ 。上述涉及的主要物质为纯净物时,属于共价化合物的是___________ ;属于离子化合物的是___________ 。
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。制作冷敷袋可以利用______(填序号,下同)。
| A.放热的化学变化 | B.吸热的化学变化 |
| C.放热的物理变化 | D.吸热的物理变化 |
①液态水汽化 ②稀释浓硫酸
③高温下碳酸钙分解 ④镁条与盐酸反应
⑤硝酸铵固体溶于水 ⑥铁丝在纯氧中燃烧
⑦氢氧化钾溶液与硝酸反应 ⑧八水合氢氧化钡固体与氯化铵固体混合搅拌
(3)下列变化:①碘的升华 ②烧碱熔化 ③氯化钠溶于水④氯化氢溶于水 ⑤氯气溶于水 ⑥氯化铵受热分解
未发生化学键破坏的是
您最近一年使用:0次
23-24高一上·全国·假期作业
10 . 现代社会生活离不开能量。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用_______ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面_______ (填序号)反应释放的热量加热食物。
A.生石灰和水 B.Ba(OH)2·8H2O和NH4Cl
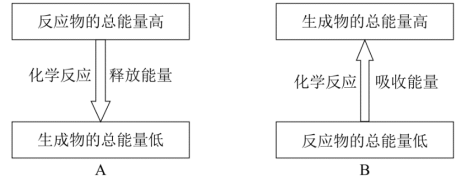
(3)硫在氧气中燃烧是_______ (填“放热”或“吸热”)反应,其能量变化可用如图中的_______ (填序号)表示。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
A.生石灰和水 B.Ba(OH)2·8H2O和NH4Cl
(3)硫在氧气中燃烧是

您最近一年使用:0次



