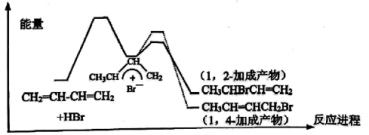
1 . 1,3—丁二烯与HBr发生加成反应分两步:第一步 进攻1,3—丁二烯生成碳正离子;第二步
进攻1,3—丁二烯生成碳正离子;第二步 进攻碳正离子发生1,2—加成或1,4—加成。反应进程中的能量变化如图,下列说法正确的是
进攻碳正离子发生1,2—加成或1,4—加成。反应进程中的能量变化如图,下列说法正确的是
 进攻1,3—丁二烯生成碳正离子;第二步
进攻1,3—丁二烯生成碳正离子;第二步 进攻碳正离子发生1,2—加成或1,4—加成。反应进程中的能量变化如图,下列说法正确的是
进攻碳正离子发生1,2—加成或1,4—加成。反应进程中的能量变化如图,下列说法正确的是
| A.1,2—加成产物比1,4—加成产物稳定 |
| B.1,2—加成产物与1,4—加成产物互为同系物 |
| C.两种产物均可发生加聚反应,且加聚反应后的产物不同 |
| D.1,3—丁二烯与HBr加成反应过程中的两步反应均为放热反应 |
您最近一年使用:0次
名校
解题方法
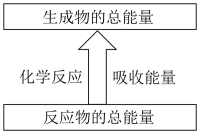
2 . 已知某化学反应的能量变化如图所示,则下列叙述正确的是

| A.图示可表示灼热的炭与二氧化碳反应的能量变化 |
| B.图示可表示镁条与盐酸反应的能量变化 |
| C.在该反应中,反应物断键吸收的总能量小于生成物成键释放的总能量 |
| D.该化学反应必须加热才能进行 |
您最近一年使用:0次
2021-07-11更新
|
215次组卷
|
2卷引用:广东省佛山市顺德区2020-2021学年高一下学期期末教学质量检测化学试题
解题方法
3 . 亚硝酰氯在有机合成中有重要应用。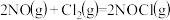 的反应历程如图所示。下列说法错误的是
的反应历程如图所示。下列说法错误的是
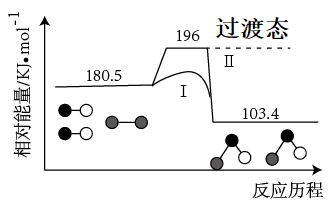
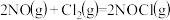 的反应历程如图所示。下列说法错误的是
的反应历程如图所示。下列说法错误的是
| A.催化剂能提高反应物的相对能量 |
| B.相对曲线Ⅱ,曲线Ⅰ表示加入催化剂 |
C.曲线Ⅱ的正反应活化能为 |
D. , , |
您最近一年使用:0次
2021-07-04更新
|
1091次组卷
|
12卷引用:广东省揭阳市揭东区2021-2022学年高三上学期期中考试化学试题
广东省揭阳市揭东区2021-2022学年高三上学期期中考试化学试题广东省深圳市第七高级中学2021-2022学年高三上学期第四次月考(12月)化学试题 湖北省2020-2021学年高二下学期7月统一调研测试化学试题江西省赣抚吉名校2022届高三上学期8月联合考试化学试题河南省延津县城北学校2021-2022学年高二上学期第二次例考化学试题(已下线)2.1.3 活化能(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)押新高考卷11题 反应机理分析-备战2022年高考化学临考题号押题(新高考通版)(已下线)第07讲 活化能(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)2.3.3 化学反应速率综合分析-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)(已下线)专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 题型专攻3 化学反应历程图像分析江西省上饶市2023-2024学年高二上学期期末教学质量测试化学试卷
解题方法
4 . 传统的定量化学实验受到计量手段的制约而研究范围狭窄、精确度不高,DIS数字化信息系统(由传感器、数据采集器和计算机组成)因为可以准确测量气压、浓度、pH、温度等而在化学实验研究中应用越来越广泛深入。
Ⅰ.将打磨后的镁条放入锥形瓶中,再将注射器中某浓度的盐酸压入锥形瓶中,通过数字传感器测定实验中密闭容器(气密性良好)内压强与时间的关系如图2所示。

(1)镁条与盐酸反应的离子方程式为___________ 。该反应为___________ (填“吸热”或“放热”)反应。
(2)图2中a、b、c、d四个点中,产生氢气最快的为___________ 点。
(3)图中c点镁条已完全溶解,cd段容器内压强逐渐减小的原因可能是___________ 。
Ⅱ.向恒温恒容的密闭容器中,加入足量的碳和一定量NO,发生如下反应
 ,数字传感器测得
,数字传感器测得 浓度随时间变化如表:
浓度随时间变化如表:
(4)若该反应在t s时恰好到达平衡,t所在时间段可能为___________
A.0s<t<80s B.80s≤t<90s C.90s<t<100s D.100s≤t<110s
(5)0〜80s用NO来表示反应的速率为___________
(6)下列能说明反应达到平衡状态是___________
A. B.容器内压强不再改变 C.
B.容器内压强不再改变 C.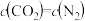 D.
D. 的体积分数不再改变
的体积分数不再改变
已知:反应体系中 的体积分数
的体积分数
Ⅰ.将打磨后的镁条放入锥形瓶中,再将注射器中某浓度的盐酸压入锥形瓶中,通过数字传感器测定实验中密闭容器(气密性良好)内压强与时间的关系如图2所示。

(1)镁条与盐酸反应的离子方程式为
(2)图2中a、b、c、d四个点中,产生氢气最快的为
(3)图中c点镁条已完全溶解,cd段容器内压强逐渐减小的原因可能是
Ⅱ.向恒温恒容的密闭容器中,加入足量的碳和一定量NO,发生如下反应

 ,数字传感器测得
,数字传感器测得 浓度随时间变化如表:
浓度随时间变化如表:| 反应时间/s | 0 | 80 | 90 | 100 | 110 |
 浓度/ 浓度/ | 0.00 | 0.30 | 0.32 | 0.33 | 0.33 |
A.0s<t<80s B.80s≤t<90s C.90s<t<100s D.100s≤t<110s
(5)0〜80s用NO来表示反应的速率为
(6)下列能说明反应达到平衡状态是
A.
 B.容器内压强不再改变 C.
B.容器内压强不再改变 C.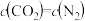 D.
D. 的体积分数不再改变
的体积分数不再改变已知:反应体系中
 的体积分数
的体积分数
您最近一年使用:0次
9-10高一下·江苏宿迁·期中
名校
解题方法
5 . 已知反应X+Y=M+N为吸热反应,下列说法中正确的是
| A.X的能量一定低于M的,Y的能量一定低于N的 |
| B.因为该反应为吸热反应,故一定要加热,反应才能进行 |
| C.断开反应物中的化学键所放出的能量小于形成生成物中化学键所吸收的能量 |
| D.X和Y的总能量低于M和N的总能量 |
您最近一年使用:0次
2021-06-26更新
|
499次组卷
|
101卷引用:广东省东莞市光明中学2020-2021学年高一下学期第一次月考化学试题
广东省东莞市光明中学2020-2021学年高一下学期第一次月考化学试题(已下线)09-10年深圳高中高一下学期期末测试化学卷(已下线)2010年广东省佛山市禅城区高一第二学期期末考试化学试题(已下线)2010年广东省龙川一中高一下学期期末考试化学试题(已下线)2010-2011学年广东省龙山中学高一下学期期中考试化学试卷(已下线)2010-2011学年广东省揭阳一中高一下学期期中考试化学试题(已下线)2010-2011学年广东省潮州金中高一下学期期中考试化学(文)试题(已下线)2010-2011学年广东省潮州金中高一下学期期中考试化学(理科班)化学卷2014-2015学年广东省潮州市饶平县一中高一下第三次阶段测化学试卷湖南省娄底市双峰八中2020-2021学年高一下学期期中测试化学试题(已下线)【浙江新东方】双师169高一下(已下线)【浙江新东方】双师173高一下甘肃省金昌市第一中学2020-2021学年高一下学期期中考试化学(文)试题河北省/唐山市第十一中学2020-2021学年高一下学期期中考试化学试题(已下线)【浙江新东方】高中化学20210621-012【2021】【高一下】(已下线)模块七 化学反应与能量(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)(已下线)09~10学年江苏宿迁中学高一下学期期中考试化学卷(已下线)09-10学年河北省衡水中学高一年级下学期期末考试化学试卷(已下线)09-10年邯郸市高一下学期期末质量检测化学卷(已下线)09-10学年滇池中学高一下学期期末化学试卷(已下线)2010年郑州市智林学校高一下学期期末考试化学试题(已下线)2010年山东省聊城四中高一第二学期期末考试化学试题(已下线)2010年黑龙江省五大连池市高级中学等五校联谊高一下学期期末考试(已下线)2010-2011学年内蒙古赤峰二中高一下学期期中考试化学试卷(已下线)2010-2011学年云南省武定一中高一下学期期中考试化学试卷(已下线)2010—2011学年山东省汶上一中高二下学期期末考试化学试卷(已下线)2011-2012学年山西省大同一中高二上学期期中考试化学试卷(已下线)2011-2012学年江西省横峰中学高一下学期期中考试化学试卷(已下线)2011-2012学年山东省济宁市金乡二中高一下学期期中考试化学试卷(已下线)2011-2012学年贵州省湄潭中学高一下学期期中考试化学试卷 (已下线)2011-2012学年黑龙江海林市高级中学高一下学期期中考试化学试卷 (已下线)2011-2012学年吉林省长春外国语学校高一下学期期末考试化学试卷(已下线)2011-2012学年贵州省盘县二中高一下学期期中考试化学试卷(已下线)2012-2013学年甘肃省甘谷县甘谷一中高一下学期期中考试化学试卷(已下线)2013-2014浙江省温州中学高一下学期期中化学试卷(已下线)2014届新疆乌鲁木齐市兵团二中高二(上)期末化学试卷2014-2015学年福建省清流一中高二上学期月考化学理试卷2014-2015山西省大同市一中高二上学期期中化学试卷2014-2015河北省邢台市高二上学期期末考试化学试卷2014-2015四川省绵阳市南山中学高一4月月考化学试卷2014-2015陕西省三原北城中学高一下学期第一次月考化学试卷2014-2015学年四川省德阳市第五中学高一下学期期中考试化学试卷2015-2016学年安徽省阜阳市亲情学校高二上第二次月考化学试卷2015-2016学年广西河池市高中高一下第一次月考化学试卷2015-2016学年甘肃会宁一中高一下期中理科化学试卷2015-2016学年宁夏育才中学高一下期中化学试卷2015-2016学年山东省济南一中高一下期中化学试卷2015-2016学年广西南宁二十六中高一下学期期中考试化学试卷2015-2016学年黑龙江省伊春市带岭高中高一下期中化学试卷2015-2016学年山西大学附中高一下期中化学试卷2015-2016学年湖南省长沙一中等三校高一下期末化学试卷2016-2017学年安徽省六安一中高二上开学测化学试卷2016-2017学年山西省山西大学附中高二上9月月考化学卷2016-2017学年山东省潍坊市高一下学期第一次月考模拟测试化学试卷2016-2017学年江西省宜春中学高一3月月考化学试卷2016-2017学年山东省济南第一中学高一3月阶段性考试化学试卷山东省烟台市2016-2017学年高一下学期期中考试化学试题河北省馆陶县第一中学2016-2017学年高一下学期期中考试化学试题黑龙江省伊春市第二中学2016-2017学年高一下学期期中考试(理)化学试题重庆市第一中学2016-2017学年高一下学期期中考试化学试卷重庆市江津田家炳中学2016-2017学年高一下学期期中考试化学试题山西省汾阳中学2016-2017学年高一下学期期中考试(理)化学试题湖北省部分重点中学2016-2017学年高一下学期期末考试化学试题安徽省阜阳市临泉县第一中学2016-2017学年高一下学期学科竞赛化学试题河北省石家庄市鹿泉一中2017-2018学年高一3月月考化学试题山东省菏泽市第一中学2017-2018学年高一自主检测化学试题河北省香河县第三中学2017-2018学年高一下学期第一次月考化学试题宁夏青铜峡市高级中学2017-2018学年高一下学期期中考试化学试题【全国校级联考】河南省商丘市九校2017-2018学年高一下学期期末联考化学试题【全国百强校】天津市静海县第一中学2018-2019学年高二上学期9月学生学业能力调研化学试题贵州省遵义市航天高级中学2018-2019学年高二(理)上学期第一次月考化学试题山东省德州市夏津一中2018-2019学年高二上学期第一次月考化学试题【全国百强校】贵州省遵义航天高级中学2018-2019学年高二上学期第一次月考化学试题河北省唐山市第十一中学2018-2019学年高一下学期期中考试化学试题宁夏回族自治区青铜峡市高级中学2018-2019学年高一下学期期中考试化学试题山西省阳泉市第二中学2018-2019学年高一下学期期中考试化学试题黑龙江省绥滨县第一中学2018-2019学年高一(理)下学期期中考试化学试题甘肃省东乡族自治县第二中学2016-2017学年高一下学期期末考试化学试题新疆奎屯市第一高级中学2018-2019学年高一下学期第一次月考化学试题河北省唐山市第十一中学2019-2020学年高二上学期期中考试化学(理)试题贵州省金沙中学2019-2020学年高一上学期期末考试化学试题甘肃省古浪县第二中学2019-2020学年高二12月基础知识竞赛化学试题福建省莆田市仙游县枫亭中学2019-2020学年高二上学期期中考试(1,3班)化学试题甘肃省甘南藏族自治州合作第一中学2018-2019学年高一下学期期中考试化学试题安徽省阜阳市临泉县第一中学2019-2020学年高一下学期第一次月考化学试题吉林省延边市长白山第一高级中学2019-2020学年高一下学期验收考试化学试题湖北省宜昌市第二中学2019-2020高一下学期4 月线上检测化学试题安徽省肥东县第二中学2019-2020学年高一下学期期中考试(共建班)化学试题江苏省泗洪县洪翔中学、沭阳县修远中学2019-2020学年高一5月月考化学试题四川省内江市威远中学2019-2020学年高一下学期第二次月考化学试题(已下线)考点05 化学反应中的能量变化-2020年【衔接教材·暑假作业】新高三一轮复习化学宁夏吴忠中学2019-2020学年高一下学期期末考试化学试题湖南省邵东县第一中学2019-2020学年高一下学期第三次月考化学试题内蒙古自治区赤峰市2019-2020学年高一下学期期末联考化学(B卷)试题安徽省蚌埠第三中学2019-2020学年高一下学期5月月考化学试题安徽省蚌埠第三中学2019-2020学年高二上学期开学考试化学试题陕西省子洲中学2018-2019学年高一下学期第二次月考化学试题湖北省石首市第一中学2020-2021学年高二上学期9月月考化学试题云南民族大学附属中学2019-2020学年高二上学期期中考试化学试题辽宁省滨海实验中学2019-2020学年高二上学期期末化学试题(已下线)专题06 化学反应与能量-2023年高考化学一轮复习小题多维练(全国通用)
6 . 金刚石与石墨燃烧过程中的能量变化如图所示。下列说法正确的是
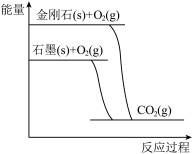

| A.金刚石与石墨之间的转化属于物理变化 |
| B.石墨比金刚石更稳定 |
| C.等质量的金刚石与石墨完全燃烧,前者吸热更多 |
| D.金刚石与石墨互为同分异构体 |
您最近一年使用:0次
2021-06-23更新
|
173次组卷
|
2卷引用:广东省普通高中2020-2021学年高一下学期教学质量联合测评化学试题
解题方法
7 . 下列说法中正确的是
| A.将1molHCl气体通入足量0.1mol·L-1NaOH溶液中充分反应,放出的热量可用于计算中和热 |
B.已知 O2(g)=O(g)△H=+249kJ·mol-1,则O=O键的键能为249kJ·mol-1 O2(g)=O(g)△H=+249kJ·mol-1,则O=O键的键能为249kJ·mol-1 |
| C.已知C(金刚石,s)=C(石墨,s)△H=-1.9kJ·mol-1,则金刚石的燃烧热△H1小于石墨的燃烧热△H2 |
| D.放热反应只有在低温时才能发生,吸热反应只有在高温时才能发生 |
您最近一年使用:0次
2021-06-21更新
|
307次组卷
|
3卷引用:广东省普通高中2020-2021学年高二下学期5月教学质量联合测评化学试题
8 . 下列变化过程属于放热反应的是
①碳酸钙高温分解②H2在Cl2中燃烧③镁与稀硫酸反应④水蒸气变成液态水⑤酸碱中和⑥NH4Cl晶体与Ba(OH)2•8H2O晶体混合搅拌⑦SO3与水反应
①碳酸钙高温分解②H2在Cl2中燃烧③镁与稀硫酸反应④水蒸气变成液态水⑤酸碱中和⑥NH4Cl晶体与Ba(OH)2•8H2O晶体混合搅拌⑦SO3与水反应
| A.①②③⑤ | B.②③④⑤ | C.②③⑤⑦ | D.②④⑤⑦ |
您最近一年使用:0次
2021-06-03更新
|
975次组卷
|
4卷引用:广东省潮州湘桥区南春中学2021-2022学年高二上学期第一次月考化学试题
广东省潮州湘桥区南春中学2021-2022学年高二上学期第一次月考化学试题河北省廊坊市河北省三河市第一中学2020-2021学年高一下学期第二次阶段考化学试题(已下线)第一节 化学反应与能量变化 (第2课时 热化学方程式 中和热的测定)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)甘肃省永昌县第一高级中学2021-2022学年高二上学期期末考试化学试题
名校
9 . 对下列实验现象或事实的结论正确的是
| 选项 | 现象或事实 | 结论 |
| A | 合成氨需在高温高压下才能进行反应 | 该反应为吸热反应 |
| B | 向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色 | 溶液中一定含有Fe3+ |
| C | 将CO2通入饱和CaCl2溶液中,无明显现象 | CO2与CaCl2不生成CaCO3 |
| D | 两支盛有5mL的H2O2的试管,向其中一支试管中加入绿豆粒大小FeI2固体,加入FeI2固体的试管中产生气泡速度快 | I-对H2O2分解具有催化作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-01更新
|
716次组卷
|
2卷引用:广东省广州市华南师范大学附属中学2021届高三下学期三模化学试题
名校
解题方法
10 . 为防止氮的氧化物污染空气,可用活性炭或一氧化碳还原氮氧化物。回答下列问题:
(1)消除NO污染物,可在一定条件下,用CO与NO反应生成CO2和N2,反应的化学方程式:2CO(g)+2NO(g) N2(g)+2CO2(g)。
N2(g)+2CO2(g)。
①为提高此反应的速率,下列措施可行的是___________ (填字母代号)。
A.增大压强 B.降低温度 C.使用适合催化剂 D.移出CO2
②该反应的能量变化关系如图所示:
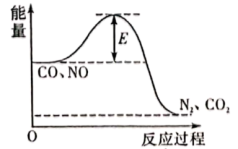
该反应属于___________ (填“放热反应”或“吸热反应”)。
(2)向两个1L的密闭容器中各加入活性炭(足量)和1.0molNO,发生反应为:C(s)+2NO(g) N2(g)+CO2(g)。实验测得不同温度下NO和N2的物质的量变化如表所示:
N2(g)+CO2(g)。实验测得不同温度下NO和N2的物质的量变化如表所示:
①T1时,0~5min内,以CO2表示的该反应速率v(CO2)=___________ mol·L-1·min-1。
②T1时,能确定反应达到最大限度(即平衡状态)的时间是___________ min,此时,容器中CO2的物质的量浓度是___________ mol/L,NO的转化率为___________ %。
③容器中的温度关系为T1___________ T2(填“>”“<”或“=”)。
(1)消除NO污染物,可在一定条件下,用CO与NO反应生成CO2和N2,反应的化学方程式:2CO(g)+2NO(g)
 N2(g)+2CO2(g)。
N2(g)+2CO2(g)。①为提高此反应的速率,下列措施可行的是
A.增大压强 B.降低温度 C.使用适合催化剂 D.移出CO2
②该反应的能量变化关系如图所示:

该反应属于
(2)向两个1L的密闭容器中各加入活性炭(足量)和1.0molNO,发生反应为:C(s)+2NO(g)
 N2(g)+CO2(g)。实验测得不同温度下NO和N2的物质的量变化如表所示:
N2(g)+CO2(g)。实验测得不同温度下NO和N2的物质的量变化如表所示:| 物质的量/mol | 温度为T1/℃ | 温度为T2/℃ | |||||||
| 0 | 5min | 9min | 10min | 12min | 0 | 5min | 9min | 10min | |
| NO | 1.0 | 0.58 | 0.42 | 0.40 | 0.40 | 1.0 | 0.50 | 0.34 | 0.34 |
| N2 | 0 | 0.21 | 0.29 | 0.30 | 0.30 | 0 | 0.25 | 0.33 | 0.33 |
②T1时,能确定反应达到最大限度(即平衡状态)的时间是
③容器中的温度关系为T1
您最近一年使用:0次
2021-05-31更新
|
268次组卷
|
3卷引用:广东省普宁市2020-2021学年高一下学期期末考试化学试题



