解题方法
1 . 回答下列问题
(1)依据事实,写出下列反应的热化学方程式:
①1 mol氨气和1 mol氯化氢气体化合生成氯化铵固体,放出176 kJ热量,该反应的热化方程式为:_______ 。
②25℃ 101 kPa时,氢气和氧气反应生成1 mol水蒸气放热241.8 kJ,该反应的热化方程式为:_______ 。
(2)甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
①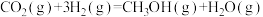 ∆H1
∆H1
②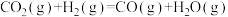 ∆H2
∆H2
③ ∆H3
∆H3
已知反应②中相关化学键键能(断裂1 mol化学键吸收或形成1 mol化学键放出的能量)数据如表:
由此计算∆H2=_______ kJ/mol。已知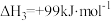 ,则∆H1=
,则∆H1=_______ kJ/mol。
(1)依据事实,写出下列反应的热化学方程式:
①1 mol氨气和1 mol氯化氢气体化合生成氯化铵固体,放出176 kJ热量,该反应的热化方程式为:
②25℃ 101 kPa时,氢气和氧气反应生成1 mol水蒸气放热241.8 kJ,该反应的热化方程式为:
(2)甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
①
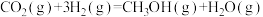 ∆H1
∆H1②
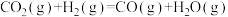 ∆H2
∆H2③
 ∆H3
∆H3已知反应②中相关化学键键能(断裂1 mol化学键吸收或形成1 mol化学键放出的能量)数据如表:
| 化学键 | H-H | C=O | C≡O | H-O |
 | 436 | 803 | 1076 | 465 |
由此计算∆H2=
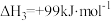 ,则∆H1=
,则∆H1=
您最近一年使用:0次
2 . 在下列各说法中,正确的是
| A.ΔH>0表示放热反应,ΔH<0表示吸热反应 |
| B.热化学方程式中的化学计量数表示物质的量,可以是分数 |
| C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |
| D.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多 |
您最近一年使用:0次
2022-09-15更新
|
408次组卷
|
5卷引用:天津市武清区四校2022-2023学年高二上学期第一次阶段性练习化学试题
3 . 已知2A2(g)+B2(g) 2C3(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达平衡后C3的浓度为ω mol·L-1,放出热量b kJ。
2C3(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达平衡后C3的浓度为ω mol·L-1,放出热量b kJ。
(1)比较a___________ b(填“>”“=”或“<”)。
(2)若将反应温度升高到700 ℃,该反应A的转化率将___________ (填“增大”“减小”或“不变”)。
(3)能说明该反应已经达到平衡状态的是___________
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的操作是___________
 2C3(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达平衡后C3的浓度为ω mol·L-1,放出热量b kJ。
2C3(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达平衡后C3的浓度为ω mol·L-1,放出热量b kJ。(1)比较a
(2)若将反应温度升高到700 ℃,该反应A的转化率将
(3)能说明该反应已经达到平衡状态的是___________
| A.v(C3)=2v(B2) | B.容器内压强保持不变 |
| C.v逆(A2)=2v正(B2) | D.容器内的密度保持不变 |
| A.及时分离出C3气体 | B.适当升高温度 |
| C.增大B2的浓度 | D.选择高效的催化剂 |
您最近一年使用:0次



