解题方法
1 . 氮是生命体重要的组成元素,自然界中氮的循环对生命活动有重要意义。
“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。___________ ;丙为钠盐,其化学式为___________ 。
(2)甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为___________ 。实验室用该反应原理制取并收集一瓶干燥的甲气体,从下图中选择合适的装置,其连接顺序为___________ 。(按从左到右的气流方向,用小写字母 和箭头表示)
(4)丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与KI按物质的量1:1恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式___________ 。
“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。

(2)甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为
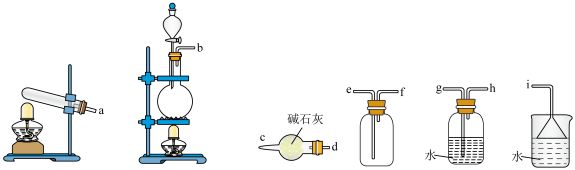
A. | B. | C. | D. |
(4)丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与KI按物质的量1:1恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式
您最近一年使用:0次
2 . 高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:___________ 。
(2)还原炉中发生的化学反应方程式为___________ 。
(3)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为___________ 。
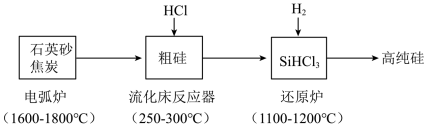
(2)还原炉中发生的化学反应方程式为
(3)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
您最近一年使用:0次
3 . 某兴趣小组设计实验模拟探究氨气催化还原焦炉煤气中的SO2,装置如图。
(1)装置a中盛装生石灰的仪器名称为___________ 。
(2)装置d中发生反应的化学方程式为___________ 。
(3)装置b中应盛装的药品为___________(填标号)。
(4)管式炉中反应一段时间后,催化剂表面开始有淡黄色固体生成,反应为 。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
过程Ⅰ:
过程Ⅱ: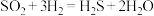
过程Ⅲ:___________ 。
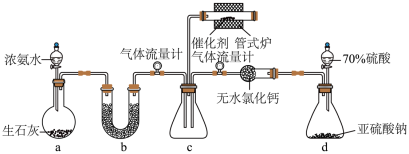
(1)装置a中盛装生石灰的仪器名称为
(2)装置d中发生反应的化学方程式为
(3)装置b中应盛装的药品为___________(填标号)。
A.无水 | B.无水 | C.浓硫酸 | D.碱石灰 |
(4)管式炉中反应一段时间后,催化剂表面开始有淡黄色固体生成,反应为
 。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。过程Ⅰ:

过程Ⅱ:
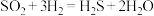
过程Ⅲ:
您最近一年使用:0次
解题方法
4 . 在宾馆、办公楼等公共场所,常使用一种电离式烟雾报警器,其主体是一个放有镅-241放射源的电离室。下列关于 的说法正确的是
的说法正确的是
 的说法正确的是
的说法正确的是A.质量数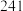 | B.中子数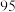 | C.电子数 | D.质子数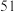 |
您最近一年使用:0次
5 . Ⅰ.已知X、Y两种元素的原子序数之和等于41。X元素原子的4p能级上有3个电子,Y元素原子的最外层2p能级上有4个电子。请回答下列问题。
(1)X元素基态原子的电子排布式__________ ,该元素的符号是__________ 。
(2)Y元素原子的价层电子排布式为__________ ,该元素的名称是__________ 。
Ⅱ.有四种短周期元素,与其相关的结构、性质等信息如下表所述:
请根据表中信息回答不列问题:
(3)A元素基态原子的电子排布式为__________ 。
(4)B元素在元素周期表中的位置为__________ 。
(5)C基态原子的轨道表示式是__________ ,其原子核外有__________ 个未成对电子,能量最高的电子为轨道上的电子,其原子轨道呈__________ 形。
(6)D原子的电子排布式为__________ , 的结构示意图为
的结构示意图为__________ 。
(1)X元素基态原子的电子排布式
(2)Y元素原子的价层电子排布式为
Ⅱ.有四种短周期元素,与其相关的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | B与A同周期,其最高价氧化物对应水化物具有两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最高的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(3)A元素基态原子的电子排布式为
(4)B元素在元素周期表中的位置为
(5)C基态原子的轨道表示式是
(6)D原子的电子排布式为
 的结构示意图为
的结构示意图为
您最近一年使用:0次
6 . 回答下列问题:
(1)如图为以惰性电极进行电解的装置:写出A、B、C、D各电极上的电极反应式和总反应方程式: 溶液
溶液  溶液
溶液
A:__________ ,B:__________ ,总反应方程式:__________ ,
C:__________ ,D:__________ ,总反应方程式:__________ 。
(2)两个烧杯中电解质溶液足量,则A、B、C、D四个电极产物的物质的量之比为__________ 。
(3)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:__________ 。
②正极上消耗 (标准状况)气体时,转移电子的物质的量为
(标准状况)气体时,转移电子的物质的量为__________ 。
(1)如图为以惰性电极进行电解的装置:写出A、B、C、D各电极上的电极反应式和总反应方程式:

 溶液
溶液  溶液
溶液A:
C:
(2)两个烧杯中电解质溶液足量,则A、B、C、D四个电极产物的物质的量之比为
(3)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

②正极上消耗
 (标准状况)气体时,转移电子的物质的量为
(标准状况)气体时,转移电子的物质的量为
您最近一年使用:0次
解题方法
7 . 现有常温下浓度均为 的下列五种溶液:
的下列五种溶液:
① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液
(1)这5种溶液pH由大到小的顺序是__________ (填序号)。
(2)②中各离子浓度由大到小的顺序是__________ 。
(3)向③中通入少量氨气,此时 的值
的值__________ (填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积__________ ④的体积(填“大于”“小于”或“等于”)。
(5)常温下,向 溶液中加入
溶液中加入 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为__________ ,若将所得悬浊液的pH值调整为4,则溶液中 的浓度为
的浓度为__________  (已知常温下
(已知常温下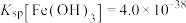 。
。
 的下列五种溶液:
的下列五种溶液:①
 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液(1)这5种溶液pH由大到小的顺序是
(2)②中各离子浓度由大到小的顺序是
(3)向③中通入少量氨气,此时
 的值
的值(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积
(5)常温下,向
 溶液中加入
溶液中加入 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为 的浓度为
的浓度为 (已知常温下
(已知常温下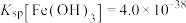 。
。
您最近一年使用:0次
解题方法
8 . 依据下列热化学方程式得出的结论中,正确的是
A.已知 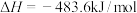 ,则氢气的燃烧热 ,则氢气的燃烧热 为 为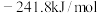 |
B.已知C(石墨,s)= C(金刚石,s)  ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C.已知 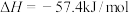 ,则含 ,则含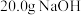 的稀溶液与稀盐酸完全中和,放出 的稀溶液与稀盐酸完全中和,放出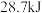 的热量 的热量 |
D.已知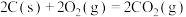  ; ;  ,则 ,则 |
您最近一年使用:0次
9 . 下列元素中,未成对电子最多的是
| A.Ne | B.P | C.Fe | D.Cr |
您最近一年使用:0次
解题方法
10 . 以下表示氦原子结构的化学用语中,对电子运动状态描述最详尽的是
A.电子式: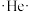 | B.原子结构示意图: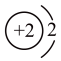 |
C.电子排布式: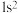 | D.轨道表示式: |
您最近一年使用:0次



