1 . Ⅰ.已知X、Y两种元素的原子序数之和等于41。X元素原子的4p能级上有3个电子,Y元素原子的最外层2p能级上有4个电子。请回答下列问题。
(1)X元素基态原子的电子排布式__________ ,该元素的符号是__________ 。
(2)Y元素原子的价层电子排布式为__________ ,该元素的名称是__________ 。
Ⅱ.有四种短周期元素,与其相关的结构、性质等信息如下表所述:
请根据表中信息回答不列问题:
(3)A元素基态原子的电子排布式为__________ 。
(4)B元素在元素周期表中的位置为__________ 。
(5)C基态原子的轨道表示式是__________ ,其原子核外有__________ 个未成对电子,能量最高的电子为轨道上的电子,其原子轨道呈__________ 形。
(6)D原子的电子排布式为__________ , 的结构示意图为
的结构示意图为__________ 。
(1)X元素基态原子的电子排布式
(2)Y元素原子的价层电子排布式为
Ⅱ.有四种短周期元素,与其相关的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | B与A同周期,其最高价氧化物对应水化物具有两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最高的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(3)A元素基态原子的电子排布式为
(4)B元素在元素周期表中的位置为
(5)C基态原子的轨道表示式是
(6)D原子的电子排布式为
 的结构示意图为
的结构示意图为
您最近一年使用:0次
2 . 回答下列问题:
(1)如图为以惰性电极进行电解的装置:写出A、B、C、D各电极上的电极反应式和总反应方程式: 溶液
溶液  溶液
溶液
A:__________ ,B:__________ ,总反应方程式:__________ ,
C:__________ ,D:__________ ,总反应方程式:__________ 。
(2)两个烧杯中电解质溶液足量,则A、B、C、D四个电极产物的物质的量之比为__________ 。
(3)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:__________ 。
②正极上消耗 (标准状况)气体时,转移电子的物质的量为
(标准状况)气体时,转移电子的物质的量为__________ 。
(1)如图为以惰性电极进行电解的装置:写出A、B、C、D各电极上的电极反应式和总反应方程式:

 溶液
溶液  溶液
溶液A:
C:
(2)两个烧杯中电解质溶液足量,则A、B、C、D四个电极产物的物质的量之比为
(3)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

②正极上消耗
 (标准状况)气体时,转移电子的物质的量为
(标准状况)气体时,转移电子的物质的量为
您最近一年使用:0次
解题方法
3 . 现有常温下浓度均为 的下列五种溶液:
的下列五种溶液:
① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液
(1)这5种溶液pH由大到小的顺序是__________ (填序号)。
(2)②中各离子浓度由大到小的顺序是__________ 。
(3)向③中通入少量氨气,此时 的值
的值__________ (填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积__________ ④的体积(填“大于”“小于”或“等于”)。
(5)常温下,向 溶液中加入
溶液中加入 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为__________ ,若将所得悬浊液的pH值调整为4,则溶液中 的浓度为
的浓度为__________  (已知常温下
(已知常温下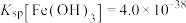 。
。
 的下列五种溶液:
的下列五种溶液:①
 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液(1)这5种溶液pH由大到小的顺序是
(2)②中各离子浓度由大到小的顺序是
(3)向③中通入少量氨气,此时
 的值
的值(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积
(5)常温下,向
 溶液中加入
溶液中加入 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为 的浓度为
的浓度为 (已知常温下
(已知常温下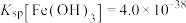 。
。
您最近一年使用:0次
解题方法
4 . 依据下列热化学方程式得出的结论中,正确的是
A.已知 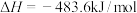 ,则氢气的燃烧热 ,则氢气的燃烧热 为 为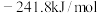 |
B.已知C(石墨,s)= C(金刚石,s)  ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C.已知 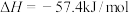 ,则含 ,则含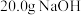 的稀溶液与稀盐酸完全中和,放出 的稀溶液与稀盐酸完全中和,放出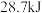 的热量 的热量 |
D.已知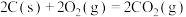  ; ;  ,则 ,则 |
您最近一年使用:0次
5 . 下列元素中,未成对电子最多的是
| A.Ne | B.P | C.Fe | D.Cr |
您最近一年使用:0次
解题方法
6 . 以下表示氦原子结构的化学用语中,对电子运动状态描述最详尽的是
A.电子式: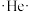 | B.原子结构示意图: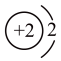 |
C.电子排布式: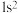 | D.轨道表示式: |
您最近一年使用:0次
7 . 某温度下,等体积、相同 的盐酸和醋酸溶液分别加水稀释,溶液中的
的盐酸和醋酸溶液分别加水稀释,溶液中的 随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
 的盐酸和醋酸溶液分别加水稀释,溶液中的
的盐酸和醋酸溶液分别加水稀释,溶液中的 随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
| A.Ⅱ表示的是盐酸的变化曲线 |
B.b点溶液中水电离的 小于c点溶液 小于c点溶液 |
C.取等体积的a点、b点对应的溶液,消耗的 的量相同 的量相同 |
| D.b点酸的总浓度大于a点酸的总浓度 |
您最近一年使用:0次
8 . 按要求回答下列问题。
(1)铁盐可用作净水剂,用离子方程式表示其原理:___________ 。配制 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的___________ 中,然后再加水稀释到所需的浓度。将 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是___________ (填化学式)。
(2)某 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的___________ ,充分反应后过滤,即可除去 。
。
(3)在 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成?___________ (填“是”或“否”)。向溶液中加入 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为___________ 。(已知 时
时 、
、 、
、 的
的 分别为
分别为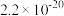 、
、 、
、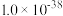 )
)
(1)铁盐可用作净水剂,用离子方程式表示其原理:
 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是(2)某
 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的 。
。(3)在
 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成? 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为 时
时 、
、 、
、 的
的 分别为
分别为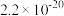 、
、 、
、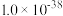 )
)
您最近一年使用:0次
9 . 已知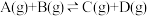 反应的平衡常数和温度的关系如下:
反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的平衡常数表达式
___________ ,
___________ 0(填“<”、“>”或“=”);
(2)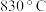 时,向一个
时,向一个 的密闭容器中充入
的密闭容器中充入 的A和
的A和 的B,若反应初始
的B,若反应初始 内A的平均反应速率
内A的平均反应速率 ,则
,则 时
时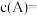
___________  ,C的物质的量为
,C的物质的量为___________  ;若反应一段时间后达到平衡,则A的转化率为
;若反应一段时间后达到平衡,则A的转化率为___________ ;如果这时向该密闭容器中再充入 氩气,平衡时A的转化率为
氩气,平衡时A的转化率为___________ 。
(3)判断该反应是否达到平衡的依据为___________ (填字母)。
a.压强不随时间改变 b.气体的密度不随时间改变
c.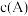 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等
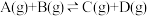 反应的平衡常数和温度的关系如下:
反应的平衡常数和温度的关系如下:| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的平衡常数表达式


(2)
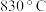 时,向一个
时,向一个 的密闭容器中充入
的密闭容器中充入 的A和
的A和 的B,若反应初始
的B,若反应初始 内A的平均反应速率
内A的平均反应速率 ,则
,则 时
时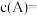
 ,C的物质的量为
,C的物质的量为 ;若反应一段时间后达到平衡,则A的转化率为
;若反应一段时间后达到平衡,则A的转化率为 氩气,平衡时A的转化率为
氩气,平衡时A的转化率为(3)判断该反应是否达到平衡的依据为
a.压强不随时间改变 b.气体的密度不随时间改变
c.
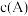 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等
您最近一年使用:0次
解题方法
10 . 用 盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。
盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。
(1)准确称取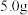 烧碱样品,所用主要仪器有托盘天平、砝码、药匙、
烧碱样品,所用主要仪器有托盘天平、砝码、药匙、___________ 。
(2)将样品配成 待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、
待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、___________ 。
(3)取 待测液,需要的仪器有
待测液,需要的仪器有___________ 、锥形瓶。
(4)酸碱中和滴定实验的操作步骤有:检查仪器、___________ 、加入反应液、调节起始读数、放出反应液、确定滴定终点、读取数据、重复上述实验步骤2次、处理数据。
(5)根据下表数据,计算被测烧碱溶液的浓度是___________ 。
(6)根据上述各数据,计算烧碱的纯度是___________ 。
(7)用蒸馏水洗涤完滴定管后,接着取标准液来滴定待测液,则导致计算出的待测液浓度___________ ;若滴定终点读取数据时俯视,则导致计算出的待测液浓度___________ (均填“偏大”“偏小”或“无影响”)。
 盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。
盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。(1)准确称取
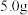 烧碱样品,所用主要仪器有托盘天平、砝码、药匙、
烧碱样品,所用主要仪器有托盘天平、砝码、药匙、(2)将样品配成
 待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、
待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、(3)取
 待测液,需要的仪器有
待测液,需要的仪器有(4)酸碱中和滴定实验的操作步骤有:检查仪器、
(5)根据下表数据,计算被测烧碱溶液的浓度是
| 滴定次数 | 待测溶液体积/ | 盐酸标准溶液体积/ | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
(6)根据上述各数据,计算烧碱的纯度是
(7)用蒸馏水洗涤完滴定管后,接着取标准液来滴定待测液,则导致计算出的待测液浓度
您最近一年使用:0次



