名校
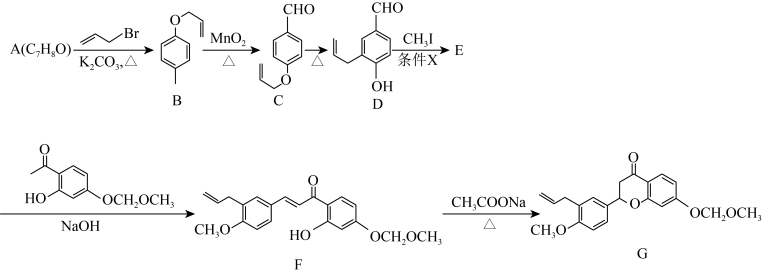
1 . 有机物G是合成一种抗癌药物的重要中间体,其合成路线如下:
(1)A的名称是___________ ,E的结构简式为___________ 。
(2)C中的含氧官能团的名称为___________ 。
(3)E→F实际上是经过两步反应,其反应类型分别是___________ ,___________ 。
(4)为了使D→E转化率更高,条件X最好选择___________ (填标号);
a.NaOH溶液 b. 溶液 c.NaClO溶液 d.稀盐酸
溶液 c.NaClO溶液 d.稀盐酸
(5)有机物C能使溴水褪色,写出C与足量的溴水反应的化学方程式___________ 。
(6)有机物D有多种同分异构体,符合下列条件的D的同分异构体有___________ 种(不考虑立体异构),其中核磁共振氢谱的峰面积比为 的结构简式是
的结构简式是___________ (任写一种)。
①能与 反应产生气体
反应产生气体
②能使溴的四氯化碳溶液褪色
③苯环上只有两侧链
(7)设计以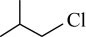 和
和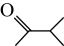 为原料制备
为原料制备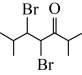 的合成路线
的合成路线________ (无机试剂和有机溶剂任用,合成路线示例见本题题干)。
已知:①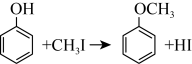 ;
;
②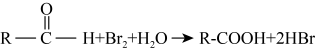 ;
;
(1)A的名称是
(2)C中的含氧官能团的名称为
(3)E→F实际上是经过两步反应,其反应类型分别是
(4)为了使D→E转化率更高,条件X最好选择
a.NaOH溶液 b.
 溶液 c.NaClO溶液 d.稀盐酸
溶液 c.NaClO溶液 d.稀盐酸(5)有机物C能使溴水褪色,写出C与足量的溴水反应的化学方程式
(6)有机物D有多种同分异构体,符合下列条件的D的同分异构体有
 的结构简式是
的结构简式是①能与
 反应产生气体
反应产生气体②能使溴的四氯化碳溶液褪色
③苯环上只有两侧链
(7)设计以
 和
和 为原料制备
为原料制备 的合成路线
的合成路线
您最近一年使用:0次
名校
解题方法
2 . 过渡元素在现代工农业生产和科技发展方面具有重要的用途。回答下列问题:
(1)已知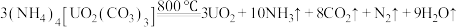 。
。
①基态N原子的核外电子中自旋状态相反的电子数之比为___________ 。
②反应中断裂的化学键有___________ (填标号)。
a.氢键 b.极性键 c.非极性键 d.离子键
③反应所得的气态产物中属于非极性分子的是___________ (填化学式,下同);氢化物中更易与 形成配离子的是
形成配离子的是___________ 。向 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出得到深蓝色溶液反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出得到深蓝色溶液反应的离子方程式___________ 。
(2)Ti的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,原因是
熔点高于其他三种卤化物,原因是___________ 。
(3)铁及其化合物在生产生活中有重要应用。Fe的某种硫化物的晶胞如图所示,该晶胞为立方体,晶胞棱长为anm。___________ 。
②已知阿伏加德罗常数的值为 ,该晶胞密度为
,该晶胞密度为___________  。
。
(1)已知
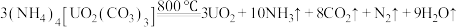 。
。①基态N原子的核外电子中自旋状态相反的电子数之比为
②反应中断裂的化学键有
a.氢键 b.极性键 c.非极性键 d.离子键
③反应所得的气态产物中属于非极性分子的是
 形成配离子的是
形成配离子的是 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出得到深蓝色溶液反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出得到深蓝色溶液反应的离子方程式(2)Ti的四卤化物熔点如下表所示,
 熔点高于其他三种卤化物,原因是
熔点高于其他三种卤化物,原因是| 化合物 |  |  |  |  |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)铁及其化合物在生产生活中有重要应用。Fe的某种硫化物的晶胞如图所示,该晶胞为立方体,晶胞棱长为anm。

②已知阿伏加德罗常数的值为
 ,该晶胞密度为
,该晶胞密度为 。
。
您最近一年使用:0次
名校
3 . 下列化学用语或表述错误的是
A.基态氧原子价电子的轨道表示式为: |
B.基态Al原子最高能级的电子云轮廓图: |
C.离子结构示意图 ,既可以表示 ,既可以表示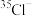 ,也可以表示 ,也可以表示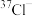 |
| D.次氯酸钠中含有的化学键类型:极性键、离子键 |
您最近一年使用:0次
名校
4 . 工业上可用一氧化碳合成可再生能源甲醇。
(1)已知:Ⅰ.
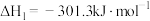 ;
;
 Ⅱ.
Ⅱ.
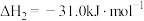 。
。
则CO与 合成气态甲醇的热化学方程式为
合成气态甲醇的热化学方程式为___________ 。
(2)某科研小组在 作催化剂的条件下,在500℃时,研究了
作催化剂的条件下,在500℃时,研究了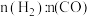 分别为
分别为 、
、 时CO的转化率变化情况(如图1所示),则图中表
时CO的转化率变化情况(如图1所示),则图中表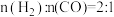 的变化曲线为:
的变化曲线为:___________ (填“曲线a”或“曲线b”)。 合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得
合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得 的产率与温度的关系如图2所示。下列说法正确的是
的产率与温度的关系如图2所示。下列说法正确的是___________ (填字母)。
b.在恒温恒压的平衡体系中充入氩气, 的产率降低
的产率降低
c.当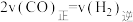 时,反应达到平衡状态
时,反应达到平衡状态
d.降低生成物甲醇的浓度,有利于提高甲醇的产率,加快反应速率
(4)一定温度下,在容积均为2L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
若甲容器平衡后气体的压强为开始时的 ,则该温度下,该反应的平衡常数K=
,则该温度下,该反应的平衡常数K=___________ ,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为___________ 。
(5)CO与日常生产生活相关。
①检测汽车尾气中CO含量,可用CO分析仪,工作原理类似于燃料电池,其中电解质是氧化钇( )和氧化锆(
)和氧化锆( )晶体,能传导
)晶体,能传导 。则负极的电极反应式为
。则负极的电极反应式为___________ 。
②碳酸二甲酯 毒性小,是一种绿色化工产品,用CO合成
毒性小,是一种绿色化工产品,用CO合成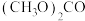 ,其电化学合成原理为
,其电化学合成原理为 ,装置如图3所示,写出阳极的电极反应式:
,装置如图3所示,写出阳极的电极反应式:___________ 。
(1)已知:Ⅰ.

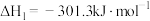 ;
; Ⅱ.
Ⅱ.
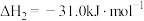 。
。则CO与
 合成气态甲醇的热化学方程式为
合成气态甲醇的热化学方程式为(2)某科研小组在
 作催化剂的条件下,在500℃时,研究了
作催化剂的条件下,在500℃时,研究了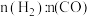 分别为
分别为 、
、 时CO的转化率变化情况(如图1所示),则图中表
时CO的转化率变化情况(如图1所示),则图中表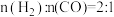 的变化曲线为:
的变化曲线为: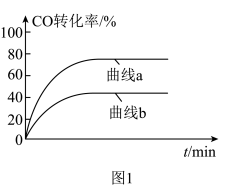
 合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得
合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得 的产率与温度的关系如图2所示。下列说法正确的是
的产率与温度的关系如图2所示。下列说法正确的是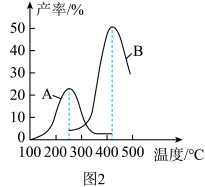
b.在恒温恒压的平衡体系中充入氩气,
 的产率降低
的产率降低c.当
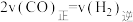 时,反应达到平衡状态
时,反应达到平衡状态d.降低生成物甲醇的浓度,有利于提高甲醇的产率,加快反应速率
(4)一定温度下,在容积均为2L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容器 | 甲 | 乙 |
| 反应物起始投入量 | 2molCO、 | amolCO、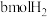 、 、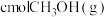 (a、b、c均不为零) (a、b、c均不为零) |
 ,则该温度下,该反应的平衡常数K=
,则该温度下,该反应的平衡常数K=(5)CO与日常生产生活相关。
①检测汽车尾气中CO含量,可用CO分析仪,工作原理类似于燃料电池,其中电解质是氧化钇(
 )和氧化锆(
)和氧化锆( )晶体,能传导
)晶体,能传导 。则负极的电极反应式为
。则负极的电极反应式为②碳酸二甲酯
 毒性小,是一种绿色化工产品,用CO合成
毒性小,是一种绿色化工产品,用CO合成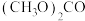 ,其电化学合成原理为
,其电化学合成原理为 ,装置如图3所示,写出阳极的电极反应式:
,装置如图3所示,写出阳极的电极反应式: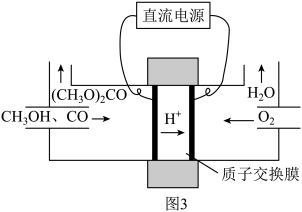
您最近一年使用:0次
名校
5 . 实验室常用如下方法制备少量 :
: ,
, 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 :
: ,
, 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A.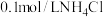 溶液中 溶液中 数目小于 数目小于 |
B.标准状况下,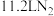 含π键数目为 含π键数目为 |
| C.氯化钠溶液可以导电,所以氯化钠溶液是电解质 |
D.上述反应中每生成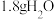 转移电子数目为 转移电子数目为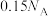 |
您最近一年使用:0次
名校
解题方法
6 . 在指定条件下,下列含氯物质间的转化能实现的是
A. (熔融) (熔融)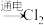 |
B.HCl(稀)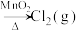 |
C.NaCl(饱和溶液)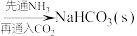 |
D.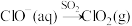 |
您最近一年使用:0次
名校
解题方法
7 . 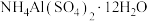 可用作净水剂、媒染剂等。下列说法正确的是
可用作净水剂、媒染剂等。下列说法正确的是
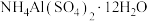 可用作净水剂、媒染剂等。下列说法正确的是
可用作净水剂、媒染剂等。下列说法正确的是| A.电负性:Al>S |
B.原子半径: |
C.第一电离能: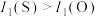 |
D.热稳定性: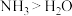 |
您最近一年使用:0次
8 . 2023年,我国科技事业收获丰硕成果。下列与科技成就相关的描述正确的是
| A.开启航运氢能时代——氢氧燃料电池工作时可将热能转化为电能 |
B.实施 海底封存—— 海底封存—— 液化时,其共价键被破坏 液化时,其共价键被破坏 |
C.打造北斗卫星系统——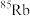 与星载铆钟所用 与星载铆钟所用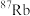 的物理性质不同 的物理性质不同 |
| D.突破量子通信技术——作为传输介质的光纤,其主要成分为晶体硅 |
您最近一年使用:0次
解题方法
9 . 氮是生命体重要的组成元素,自然界中氮的循环对生命活动有重要意义。
“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。___________ ;丙为钠盐,其化学式为___________ 。
(2)甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为___________ 。实验室用该反应原理制取并收集一瓶干燥的甲气体,从下图中选择合适的装置,其连接顺序为___________ 。(按从左到右的气流方向,用小写字母 和箭头表示)
(4)丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与KI按物质的量1:1恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式___________ 。
“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。

(2)甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为
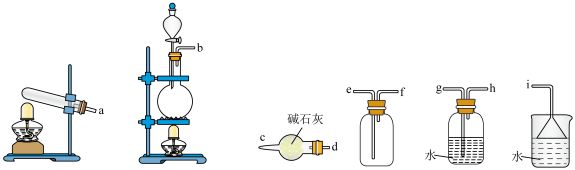
A. | B. | C. | D. |
(4)丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与KI按物质的量1:1恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式
您最近一年使用:0次
10 . 高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:___________ 。
(2)还原炉中发生的化学反应方程式为___________ 。
(3)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为___________ 。
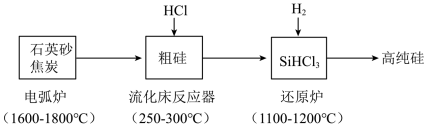
(2)还原炉中发生的化学反应方程式为
(3)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
您最近一年使用:0次



