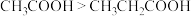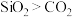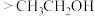解题方法
1 . 科学家发现金属钙可用于电化学驱动将 还原为
还原为 。已知:电解质溶液由
。已知:电解质溶液由 和少量
和少量 溶于有机溶剂形成。下列说法错误的是
溶于有机溶剂形成。下列说法错误的是
 还原为
还原为 。已知:电解质溶液由
。已知:电解质溶液由 和少量
和少量 溶于有机溶剂形成。下列说法错误的是
溶于有机溶剂形成。下列说法错误的是
A.阴极反应式为: |
B.推测用 代替 代替 更有利于生成 更有利于生成 |
C.理论上电解一段时间后 浓度基本不变 浓度基本不变 |
D.总反应方程式: |
您最近一年使用:0次
2 . 叔丁醇与羧酸发生酯化反应的机理可用下图表示。下列说法正确的是

| A.乙酸中氢氧键极性比中间体3中氢氧键极性强 |
B.叔丁醇中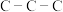 键角比中间体2的 键角比中间体2的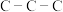 键角大 键角大 |
C.增大 ,有利于提高羧酸叔丁酯的平衡产率 ,有利于提高羧酸叔丁酯的平衡产率 |
| D.乙醇与乙酸发生酯化反应的机理与叔丁醇与羧酸发生酯化反应的机理不同 |
您最近一年使用:0次
3 . 利用反应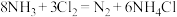 可检验氯气管道是否泄漏。下列说法正确的是
可检验氯气管道是否泄漏。下列说法正确的是
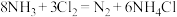 可检验氯气管道是否泄漏。下列说法正确的是
可检验氯气管道是否泄漏。下列说法正确的是A.键角: |
B. 的电子式: 的电子式: |
C.4种物质中均含有 键 键 |
D.每生成 ,转移电子数为 ,转移电子数为 (设 (设 为阿伏加德罗常数的值) 为阿伏加德罗常数的值) |
您最近一年使用:0次
解题方法
4 . 为解决实验室制备乙炔实验中存在的一些问题,某校化学兴趣小组设计出一套一体化实验装置如图所示。下列说法错误的是

| A.实验室常用电石与饱和食盐水制备乙炔 |
| B.电石放置位置为乙处 |
C.装置M中可盛装 溶液 溶液 |
| D.反应器中装有7mm玻璃珠的作用为形成空隙,促进固液分离,防堵塞 |
您最近一年使用:0次
5 . 已知 在一定条件下能和乙醚(
在一定条件下能和乙醚( 沸点
沸点 )生成缔合
)生成缔合 。实验室分离
。实验室分离 和
和 的流程如下,下列说法正确的是
的流程如下,下列说法正确的是
 在一定条件下能和乙醚(
在一定条件下能和乙醚( 沸点
沸点 )生成缔合
)生成缔合 。实验室分离
。实验室分离 和
和 的流程如下,下列说法正确的是
的流程如下,下列说法正确的是
A.反萃取操作时可加入 溶液 溶液 |
| B.分液操作时先倒出上层液体,再放出下层液体 |
| C.蒸馏操作时需要的仪器有铁架台、分液漏斗、烧杯、玻璃棒 |
D.浓盐酸酸化的作用是生成配离子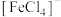 和抑制 和抑制 、 、 水解 水解 |
您最近一年使用:0次
名校
6 . 甲醇是重要的化工原料,甲醇的制备与应用也是国际研究的热点。
I.某温度下,利用 生产甲醇主要涉及以下反应。
生产甲醇主要涉及以下反应。
反应1.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)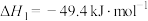 ;
;
反应2.CO2(g)+H2(g) ⇌ CO(g)+H2O(g) ;
;
(1)反应1自发进行的条件是___________ (填“高温”、“低温”或“任意温度”)。
(2)升高温度,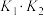 的值将
的值将___________ (填“增大”、“减小”或“不变”)。
(3)向绝热恒容密闭容器中充入等物质的量的CO2(g)和H2(g)发生上述反应,下列可说明反应已达平衡状态的是___________(填编号)。
(4)在恒温密闭容器中,发生反应1和反应2,CO2的平衡转化率[α(CO2)%]和甲醇选择性[CH3OH%= ]随着温度变化关系如图所示。
]随着温度变化关系如图所示。___________ 。
②分析温度高于236°C后CO2转化率下降的原因___________ 。
③在244°C,向容积为V的容器内投入1molCO2(g)和3molH2(g)充分反应,计算平衡时生成CH3OH的物质的量为___________ mol(计算结果保留两位有效数字)。
II.工业上也可用电化学法制备甲醇。
(5)采用如图原电池制备甲醇。通入CO的一端发生的电极反应为___________ 。
I.某温度下,利用
 生产甲醇主要涉及以下反应。
生产甲醇主要涉及以下反应。反应1.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
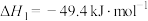 ;
;
反应2.CO2(g)+H2(g) ⇌ CO(g)+H2O(g)
 ;
;
(1)反应1自发进行的条件是
(2)升高温度,
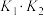 的值将
的值将(3)向绝热恒容密闭容器中充入等物质的量的CO2(g)和H2(g)发生上述反应,下列可说明反应已达平衡状态的是___________(填编号)。
| A.容器内温度不变 | B.混合气体平均密度保持不变 |
| C.CH3OH的体积分数保持不变 | D.v正(CO2)=v逆(CO) |
 ]随着温度变化关系如图所示。
]随着温度变化关系如图所示。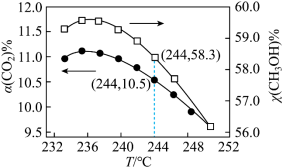
②分析温度高于236°C后CO2转化率下降的原因
③在244°C,向容积为V的容器内投入1molCO2(g)和3molH2(g)充分反应,计算平衡时生成CH3OH的物质的量为
II.工业上也可用电化学法制备甲醇。
(5)采用如图原电池制备甲醇。通入CO的一端发生的电极反应为

您最近一年使用:0次
解题方法
7 . 物质结构决定物质性质。下列物质差异与结构因素匹配错误的是
性质差异 | 结构因素 | |
A | 分子极性: | 中心原子电负性 |
B | 酸性: | 烷基的推电子效应 |
C | 熔点: | 晶体类型 |
D | 羟基中氢原子活泼性: | 不同烃基对羟基极性的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 纤维素水解的最终产物A可发生如下反应,下列说法错误的是

| A.化合物A是一种重要的营养物质 | B.化合物B含有3种官能团 |
C.强还原剂可用 | D.化合物E易溶于水 |
您最近一年使用:0次
9 . 回收废弃锂离子电池中的物质对工业可持续发展非常重要。利用 对废弃的锂离子电池的正极材料
对废弃的锂离子电池的正极材料 进行氯化处理并再生的一种工艺路线如下:
进行氯化处理并再生的一种工艺路线如下: ;
;
② 的溶液度曲线如图所示。
的溶液度曲线如图所示。
(1)基态Co原子的价层电子的轨道表示式为___________ 。
(2)“烧渣”是LiCl、 和
和 的混合物,“氯化焙烧”过程中发生反应的化学方程式为
的混合物,“氯化焙烧”过程中发生反应的化学方程式为___________ 。
(3)常温下,为了使“沉钴”过程中 沉淀完全,溶液的pH应该不低于
沉淀完全,溶液的pH应该不低于___________ [已知lg2≈0.3,c(Co2+)≤1×10-5mol/L时,可认为 沉淀完全]。
沉淀完全]。
(4)为提高 的析出量和纯度,“沉锂”操作后进行的操作依次为
的析出量和纯度,“沉锂”操作后进行的操作依次为___________ 、___________ 、洗涤、干燥。
(5)该工艺流程中可循环利用的物质为___________ 。
(6)“煅烧”过程中生成 的化学方程式为
的化学方程式为___________ 。
(7) 在空气中“焙烧”时固体残留率(固体残留率
在空气中“焙烧”时固体残留率(固体残留率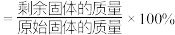 )随温度的变化如下图所示。为了获得纯净的
)随温度的变化如下图所示。为了获得纯净的 ,则该步骤应该控制的温度为___________。
,则该步骤应该控制的温度为___________。
 对废弃的锂离子电池的正极材料
对废弃的锂离子电池的正极材料 进行氯化处理并再生的一种工艺路线如下:
进行氯化处理并再生的一种工艺路线如下:
 ;
;②
 的溶液度曲线如图所示。
的溶液度曲线如图所示。
(1)基态Co原子的价层电子的轨道表示式为
(2)“烧渣”是LiCl、
 和
和 的混合物,“氯化焙烧”过程中发生反应的化学方程式为
的混合物,“氯化焙烧”过程中发生反应的化学方程式为(3)常温下,为了使“沉钴”过程中
 沉淀完全,溶液的pH应该不低于
沉淀完全,溶液的pH应该不低于 沉淀完全]。
沉淀完全]。(4)为提高
 的析出量和纯度,“沉锂”操作后进行的操作依次为
的析出量和纯度,“沉锂”操作后进行的操作依次为(5)该工艺流程中可循环利用的物质为
(6)“煅烧”过程中生成
 的化学方程式为
的化学方程式为(7)
 在空气中“焙烧”时固体残留率(固体残留率
在空气中“焙烧”时固体残留率(固体残留率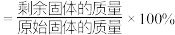 )随温度的变化如下图所示。为了获得纯净的
)随温度的变化如下图所示。为了获得纯净的 ,则该步骤应该控制的温度为___________。
,则该步骤应该控制的温度为___________。
| A.300~400℃ | B.500~800℃ | C.850~900℃ | D.1000℃以上 |
您最近一年使用:0次
10 .  NaOH溶液滴定20.00mL
NaOH溶液滴定20.00mL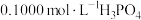 溶液时,
溶液时,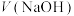 、各含磷元素微粒的
、各含磷元素微粒的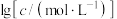 和pH的关系如图。下列说法错误的是
和pH的关系如图。下列说法错误的是
 NaOH溶液滴定20.00mL
NaOH溶液滴定20.00mL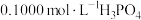 溶液时,
溶液时,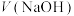 、各含磷元素微粒的
、各含磷元素微粒的 和pH的关系如图。下列说法错误的是
和pH的关系如图。下列说法错误的是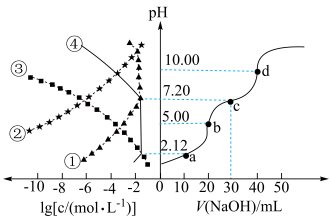
A. 的 的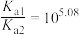 |
| B.水的电离程度:d>c>b>a |
C.③为 的 的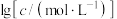 与pH的关系 与pH的关系 |
D.c点时,溶液中存在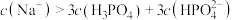 |
您最近一年使用:0次
今日更新
|
129次组卷
|
3卷引用:湖北省十堰市2023-2024学年高三下学期4月调研考试化学试题