名校
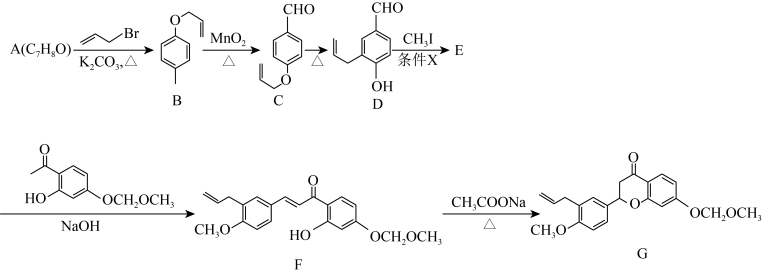
1 . 有机物G是合成一种抗癌药物的重要中间体,其合成路线如下:
(1)A的名称是___________ ,E的结构简式为___________ 。
(2)C中的含氧官能团的名称为___________ 。
(3)E→F实际上是经过两步反应,其反应类型分别是___________ ,___________ 。
(4)为了使D→E转化率更高,条件X最好选择___________ (填标号);
a.NaOH溶液 b. 溶液 c.NaClO溶液 d.稀盐酸
溶液 c.NaClO溶液 d.稀盐酸
(5)有机物C能使溴水褪色,写出C与足量的溴水反应的化学方程式___________ 。
(6)有机物D有多种同分异构体,符合下列条件的D的同分异构体有___________ 种(不考虑立体异构),其中核磁共振氢谱的峰面积比为 的结构简式是
的结构简式是___________ (任写一种)。
①能与 反应产生气体
反应产生气体
②能使溴的四氯化碳溶液褪色
③苯环上只有两侧链
(7)设计以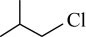 和
和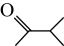 为原料制备
为原料制备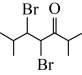 的合成路线
的合成路线________ (无机试剂和有机溶剂任用,合成路线示例见本题题干)。
已知:①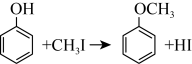 ;
;
②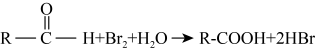 ;
;
(1)A的名称是
(2)C中的含氧官能团的名称为
(3)E→F实际上是经过两步反应,其反应类型分别是
(4)为了使D→E转化率更高,条件X最好选择
a.NaOH溶液 b.
 溶液 c.NaClO溶液 d.稀盐酸
溶液 c.NaClO溶液 d.稀盐酸(5)有机物C能使溴水褪色,写出C与足量的溴水反应的化学方程式
(6)有机物D有多种同分异构体,符合下列条件的D的同分异构体有
 的结构简式是
的结构简式是①能与
 反应产生气体
反应产生气体②能使溴的四氯化碳溶液褪色
③苯环上只有两侧链
(7)设计以
 和
和 为原料制备
为原料制备 的合成路线
的合成路线
您最近一年使用:0次
名校
解题方法
2 . 过渡元素在现代工农业生产和科技发展方面具有重要的用途。回答下列问题:
(1)已知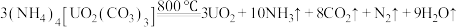 。
。
①基态N原子的核外电子中自旋状态相反的电子数之比为___________ 。
②反应中断裂的化学键有___________ (填标号)。
a.氢键 b.极性键 c.非极性键 d.离子键
③反应所得的气态产物中属于非极性分子的是___________ (填化学式,下同);氢化物中更易与 形成配离子的是
形成配离子的是___________ 。向 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出得到深蓝色溶液反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出得到深蓝色溶液反应的离子方程式___________ 。
(2)Ti的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,原因是
熔点高于其他三种卤化物,原因是___________ 。
(3)铁及其化合物在生产生活中有重要应用。Fe的某种硫化物的晶胞如图所示,该晶胞为立方体,晶胞棱长为anm。___________ 。
②已知阿伏加德罗常数的值为 ,该晶胞密度为
,该晶胞密度为___________  。
。
(1)已知
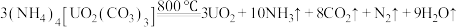 。
。①基态N原子的核外电子中自旋状态相反的电子数之比为
②反应中断裂的化学键有
a.氢键 b.极性键 c.非极性键 d.离子键
③反应所得的气态产物中属于非极性分子的是
 形成配离子的是
形成配离子的是 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出得到深蓝色溶液反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出得到深蓝色溶液反应的离子方程式(2)Ti的四卤化物熔点如下表所示,
 熔点高于其他三种卤化物,原因是
熔点高于其他三种卤化物,原因是| 化合物 |  |  |  |  |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)铁及其化合物在生产生活中有重要应用。Fe的某种硫化物的晶胞如图所示,该晶胞为立方体,晶胞棱长为anm。

②已知阿伏加德罗常数的值为
 ,该晶胞密度为
,该晶胞密度为 。
。
您最近一年使用:0次
名校
3 . 工业上可用一氧化碳合成可再生能源甲醇。
(1)已知:Ⅰ.
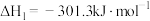 ;
;
 Ⅱ.
Ⅱ.
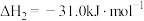 。
。
则CO与 合成气态甲醇的热化学方程式为
合成气态甲醇的热化学方程式为___________ 。
(2)某科研小组在 作催化剂的条件下,在500℃时,研究了
作催化剂的条件下,在500℃时,研究了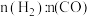 分别为
分别为 、
、 时CO的转化率变化情况(如图1所示),则图中表
时CO的转化率变化情况(如图1所示),则图中表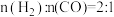 的变化曲线为:
的变化曲线为:___________ (填“曲线a”或“曲线b”)。 合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得
合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得 的产率与温度的关系如图2所示。下列说法正确的是
的产率与温度的关系如图2所示。下列说法正确的是___________ (填字母)。
b.在恒温恒压的平衡体系中充入氩气, 的产率降低
的产率降低
c.当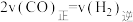 时,反应达到平衡状态
时,反应达到平衡状态
d.降低生成物甲醇的浓度,有利于提高甲醇的产率,加快反应速率
(4)一定温度下,在容积均为2L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
若甲容器平衡后气体的压强为开始时的 ,则该温度下,该反应的平衡常数K=
,则该温度下,该反应的平衡常数K=___________ ,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为___________ 。
(5)CO与日常生产生活相关。
①检测汽车尾气中CO含量,可用CO分析仪,工作原理类似于燃料电池,其中电解质是氧化钇( )和氧化锆(
)和氧化锆( )晶体,能传导
)晶体,能传导 。则负极的电极反应式为
。则负极的电极反应式为___________ 。
②碳酸二甲酯 毒性小,是一种绿色化工产品,用CO合成
毒性小,是一种绿色化工产品,用CO合成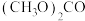 ,其电化学合成原理为
,其电化学合成原理为 ,装置如图3所示,写出阳极的电极反应式:
,装置如图3所示,写出阳极的电极反应式:___________ 。
(1)已知:Ⅰ.

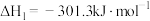 ;
; Ⅱ.
Ⅱ.
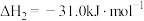 。
。则CO与
 合成气态甲醇的热化学方程式为
合成气态甲醇的热化学方程式为(2)某科研小组在
 作催化剂的条件下,在500℃时,研究了
作催化剂的条件下,在500℃时,研究了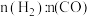 分别为
分别为 、
、 时CO的转化率变化情况(如图1所示),则图中表
时CO的转化率变化情况(如图1所示),则图中表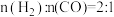 的变化曲线为:
的变化曲线为: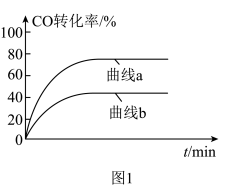
 合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得
合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得 的产率与温度的关系如图2所示。下列说法正确的是
的产率与温度的关系如图2所示。下列说法正确的是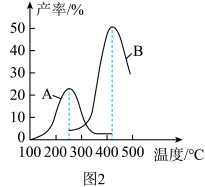
b.在恒温恒压的平衡体系中充入氩气,
 的产率降低
的产率降低c.当
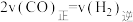 时,反应达到平衡状态
时,反应达到平衡状态d.降低生成物甲醇的浓度,有利于提高甲醇的产率,加快反应速率
(4)一定温度下,在容积均为2L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容器 | 甲 | 乙 |
| 反应物起始投入量 | 2molCO、 | amolCO、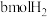 、 、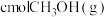 (a、b、c均不为零) (a、b、c均不为零) |
 ,则该温度下,该反应的平衡常数K=
,则该温度下,该反应的平衡常数K=(5)CO与日常生产生活相关。
①检测汽车尾气中CO含量,可用CO分析仪,工作原理类似于燃料电池,其中电解质是氧化钇(
 )和氧化锆(
)和氧化锆( )晶体,能传导
)晶体,能传导 。则负极的电极反应式为
。则负极的电极反应式为②碳酸二甲酯
 毒性小,是一种绿色化工产品,用CO合成
毒性小,是一种绿色化工产品,用CO合成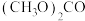 ,其电化学合成原理为
,其电化学合成原理为 ,装置如图3所示,写出阳极的电极反应式:
,装置如图3所示,写出阳极的电极反应式: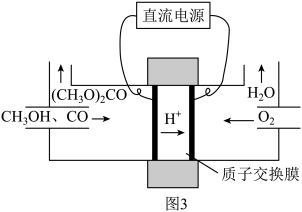
您最近一年使用:0次
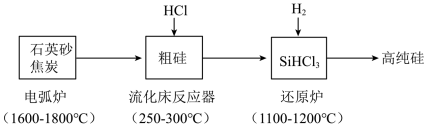
4 . 高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:___________ 。
(2)还原炉中发生的化学反应方程式为___________ 。
(3)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为___________ 。
(2)还原炉中发生的化学反应方程式为
(3)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
您最近一年使用:0次
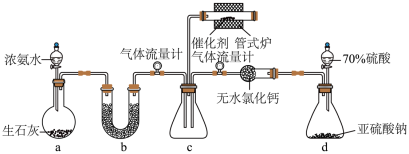
5 . 某兴趣小组设计实验模拟探究氨气催化还原焦炉煤气中的SO2,装置如图。
(1)装置a中盛装生石灰的仪器名称为___________ 。
(2)装置d中发生反应的化学方程式为___________ 。
(3)装置b中应盛装的药品为___________(填标号)。
(4)管式炉中反应一段时间后,催化剂表面开始有淡黄色固体生成,反应为 。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
过程Ⅰ:
过程Ⅱ: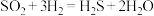
过程Ⅲ:___________ 。
(1)装置a中盛装生石灰的仪器名称为
(2)装置d中发生反应的化学方程式为
(3)装置b中应盛装的药品为___________(填标号)。
A.无水 | B.无水 | C.浓硫酸 | D.碱石灰 |
(4)管式炉中反应一段时间后,催化剂表面开始有淡黄色固体生成,反应为
 。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。过程Ⅰ:

过程Ⅱ:
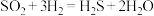
过程Ⅲ:
您最近一年使用:0次
6 . Ⅰ.已知X、Y两种元素的原子序数之和等于41。X元素原子的4p能级上有3个电子,Y元素原子的最外层2p能级上有4个电子。请回答下列问题。
(1)X元素基态原子的电子排布式__________ ,该元素的符号是__________ 。
(2)Y元素原子的价层电子排布式为__________ ,该元素的名称是__________ 。
Ⅱ.有四种短周期元素,与其相关的结构、性质等信息如下表所述:
请根据表中信息回答不列问题:
(3)A元素基态原子的电子排布式为__________ 。
(4)B元素在元素周期表中的位置为__________ 。
(5)C基态原子的轨道表示式是__________ ,其原子核外有__________ 个未成对电子,能量最高的电子为轨道上的电子,其原子轨道呈__________ 形。
(6)D原子的电子排布式为__________ , 的结构示意图为
的结构示意图为__________ 。
(1)X元素基态原子的电子排布式
(2)Y元素原子的价层电子排布式为
Ⅱ.有四种短周期元素,与其相关的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | B与A同周期,其最高价氧化物对应水化物具有两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最高的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(3)A元素基态原子的电子排布式为
(4)B元素在元素周期表中的位置为
(5)C基态原子的轨道表示式是
(6)D原子的电子排布式为
 的结构示意图为
的结构示意图为
您最近一年使用:0次
7 . 已知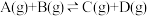 反应的平衡常数和温度的关系如下:
反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的平衡常数表达式
___________ ,
___________ 0(填“<”、“>”或“=”);
(2)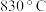 时,向一个
时,向一个 的密闭容器中充入
的密闭容器中充入 的A和
的A和 的B,若反应初始
的B,若反应初始 内A的平均反应速率
内A的平均反应速率 ,则
,则 时
时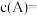
___________  ,C的物质的量为
,C的物质的量为___________  ;若反应一段时间后达到平衡,则A的转化率为
;若反应一段时间后达到平衡,则A的转化率为___________ ;如果这时向该密闭容器中再充入 氩气,平衡时A的转化率为
氩气,平衡时A的转化率为___________ 。
(3)判断该反应是否达到平衡的依据为___________ (填字母)。
a.压强不随时间改变 b.气体的密度不随时间改变
c.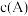 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等
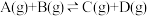 反应的平衡常数和温度的关系如下:
反应的平衡常数和温度的关系如下:| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的平衡常数表达式


(2)
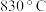 时,向一个
时,向一个 的密闭容器中充入
的密闭容器中充入 的A和
的A和 的B,若反应初始
的B,若反应初始 内A的平均反应速率
内A的平均反应速率 ,则
,则 时
时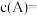
 ,C的物质的量为
,C的物质的量为 ;若反应一段时间后达到平衡,则A的转化率为
;若反应一段时间后达到平衡,则A的转化率为 氩气,平衡时A的转化率为
氩气,平衡时A的转化率为(3)判断该反应是否达到平衡的依据为
a.压强不随时间改变 b.气体的密度不随时间改变
c.
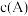 不随时间改变 d.单位时间里生成C和D的物质的量相等
不随时间改变 d.单位时间里生成C和D的物质的量相等
您最近一年使用:0次
解题方法
8 . 用 盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。
盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。
(1)准确称取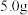 烧碱样品,所用主要仪器有托盘天平、砝码、药匙、
烧碱样品,所用主要仪器有托盘天平、砝码、药匙、___________ 。
(2)将样品配成 待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、
待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、___________ 。
(3)取 待测液,需要的仪器有
待测液,需要的仪器有___________ 、锥形瓶。
(4)酸碱中和滴定实验的操作步骤有:检查仪器、___________ 、加入反应液、调节起始读数、放出反应液、确定滴定终点、读取数据、重复上述实验步骤2次、处理数据。
(5)根据下表数据,计算被测烧碱溶液的浓度是___________ 。
(6)根据上述各数据,计算烧碱的纯度是___________ 。
(7)用蒸馏水洗涤完滴定管后,接着取标准液来滴定待测液,则导致计算出的待测液浓度___________ ;若滴定终点读取数据时俯视,则导致计算出的待测液浓度___________ (均填“偏大”“偏小”或“无影响”)。
 盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。
盐酸作标准液,用中和滴定法测定某烧碱的纯度。若烧碱中不含与盐酸反应的杂质,试根据实验回答下列问题。(1)准确称取
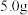 烧碱样品,所用主要仪器有托盘天平、砝码、药匙、
烧碱样品,所用主要仪器有托盘天平、砝码、药匙、(2)将样品配成
 待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、
待测液,需要的仪器有烧杯、玻璃棒、胶头滴管、(3)取
 待测液,需要的仪器有
待测液,需要的仪器有(4)酸碱中和滴定实验的操作步骤有:检查仪器、
(5)根据下表数据,计算被测烧碱溶液的浓度是
| 滴定次数 | 待测溶液体积/ | 盐酸标准溶液体积/ | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
(6)根据上述各数据,计算烧碱的纯度是
(7)用蒸馏水洗涤完滴定管后,接着取标准液来滴定待测液,则导致计算出的待测液浓度
您最近一年使用:0次
解题方法
9 . 采用如图装置制取一定量的饱和氯水,并进行氯水的性质实验。
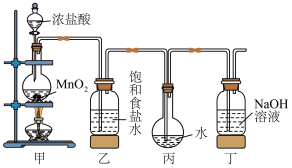
(1)在装入药品前应进行的操作_______ 。
(2)写出甲装置中发生反应的化学方程式为_______ 。
(3)请写出丁装置中发生的反应,用离子方程式表示:_______ 。
(4)已知高锰酸钾与浓盐酸反应也可产生氯气,反应如下: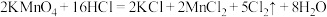 。反应中被氧化的元素是
。反应中被氧化的元素是_______ ,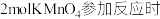 ,被氧化的
,被氧化的 物质的量为
物质的量为_______  。
。

(1)在装入药品前应进行的操作
(2)写出甲装置中发生反应的化学方程式为
(3)请写出丁装置中发生的反应,用离子方程式表示:
(4)已知高锰酸钾与浓盐酸反应也可产生氯气,反应如下:
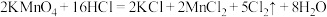 。反应中被氧化的元素是
。反应中被氧化的元素是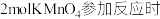 ,被氧化的
,被氧化的 物质的量为
物质的量为 。
。
您最近一年使用:0次
解题方法
10 . 短周期元素X、Y、Z在元素周期表中的位置如图所示,回答下列问题。
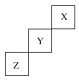
(1)元素X单质分子是_______ (写化学式)。
(2)Y位于元素周期表中的第_______ 周期第_______ 族。
(3)Z的同主族下一周期的元素的原子序数是_______ 。
(4)与Z的同一周期的金属元素中,与氢氧化钠溶液反应的的化学反应方程式为_______ 。

(1)元素X单质分子是
(2)Y位于元素周期表中的第
(3)Z的同主族下一周期的元素的原子序数是
(4)与Z的同一周期的金属元素中,与氢氧化钠溶液反应的的化学反应方程式为
您最近一年使用:0次



