1 . 下列表述正确的是
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以通过先加稀硝酸,再加氯化钡溶液的方法
③锌与稀硝酸反应主要产物有氢气
④足量的铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑤将浓硫酸滴到纸上,纸变黑,说明浓硫酸具有脱水性
⑥二氧化硫和二氧化氮都能形成酸雨,酸雨的pH≥7
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以通过先加稀硝酸,再加氯化钡溶液的方法
③锌与稀硝酸反应主要产物有氢气
④足量的铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑤将浓硫酸滴到纸上,纸变黑,说明浓硫酸具有脱水性
⑥二氧化硫和二氧化氮都能形成酸雨,酸雨的pH≥7
| A.①③④ | B.①②⑥ | C.①⑤ | D.①⑤⑥ |
您最近一年使用:0次
2024-03-05更新
|
597次组卷
|
6卷引用:天津市武清区黄花店中学2023-2024学年高一下学期第一次月考化学试题(理科)
名校
2 . 下列实验方案中,不能达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热。冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
D | 验证AgI的溶解度小于AgCl | 将NaI浓溶液加入AgCl悬浊液中,振荡,可观察到沉淀由白色变为黄色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-04-01更新
|
450次组卷
|
3卷引用:2017届天津市武清区杨村第一中学高三下学期第一次月考化学试卷
3 . NaOH和盐酸都是中学化学常见的试剂。
Ⅰ.某同学用0.200 0 mol·L-1标准盐酸滴定待测烧碱溶液浓度
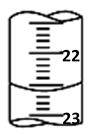
(1)将5.0 g烧碱样品(杂质不与酸反应)配成250 mL待测液,取10.00 mL待测液,如图是某次滴定时的滴定管中的液面,其读数为________ mL。________ 。
Ⅱ.氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将2 mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20 mL l.0×l0﹣4 mol/L的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式_____________________ 。
(2)滴定时,将KMnO4溶液装在________ (填“酸式”或“碱式”)滴定管中。
(3)判断滴定终点的方法是________________________ 。
(4)误差分析:(填“偏高”、“偏低”或“无影响”)
①如果滴定管用蒸馏水洗后未用酸性KMnO4标准液润洗,则测量结果________ 。
②滴定前后读数都正确,但滴定前有气泡,而滴定后气泡消失,则测量结果________ 。
(5)计算:血液中含钙离子的浓度为________ mol/L。
Ⅲ.50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液测定计算中和反应的反应热。回答下列问题:__________ 。如改用0.0275 mol NaOH固体与该盐酸进行实验,则实验中测得的“中和热”数值将________ (填“偏大”、“偏小”或“无影响”)。
(2)已知盐酸和NaOH稀溶液发生中和反应生成0.1 mol H2O时,放出5.73 kJ的热量,则表示该反应中和热的热化学方程式为:___________________________ 。
Ⅰ.某同学用0.200 0 mol·L-1标准盐酸滴定待测烧碱溶液浓度
(1)将5.0 g烧碱样品(杂质不与酸反应)配成250 mL待测液,取10.00 mL待测液,如图是某次滴定时的滴定管中的液面,其读数为
| 滴定次数 | 待测NaOH溶液体积(mL) | 标准盐酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
①可将2 mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20 mL l.0×l0﹣4 mol/L的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式
(2)滴定时,将KMnO4溶液装在
(3)判断滴定终点的方法是
(4)误差分析:(填“偏高”、“偏低”或“无影响”)
①如果滴定管用蒸馏水洗后未用酸性KMnO4标准液润洗,则测量结果
②滴定前后读数都正确,但滴定前有气泡,而滴定后气泡消失,则测量结果
(5)计算:血液中含钙离子的浓度为
Ⅲ.50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液测定计算中和反应的反应热。回答下列问题:
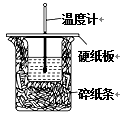
(2)已知盐酸和NaOH稀溶液发生中和反应生成0.1 mol H2O时,放出5.73 kJ的热量,则表示该反应中和热的热化学方程式为:
您最近一年使用:0次
2018-12-06更新
|
200次组卷
|
2卷引用:【区级联考】天津市武清区2018-2019学年高二上学期期中质量调查化学试题



