解题方法
1 . 过氧化钠保存不当容易变质。某课外活动小组为了粗略测定过氧化钠的质量分数,他们称取2.0g样品,并设计用下图装置来测定过氧化钠的质量分数。图中的E和F构成量气装置,用来测定O2的体积。

(1)写出装置A中两种主要玻璃仪器的名称__________ 、_______ 。
(2)写出装置A中发生的离子方程式____________________________ 。
(3)装置B的作用是______________________________ 。
(4)写出装置C中发生反应的主要化学方程式:______________________________ 。
(5)装置D中 NaOH的作用是________________________________________ 。
(6)他们在读出量筒内水的体积数后,折算成标准状况下氧气的体积为224mL,则样品中过氧化钠的质量分数为__________

(1)写出装置A中两种主要玻璃仪器的名称
(2)写出装置A中发生的离子方程式
(3)装置B的作用是
(4)写出装置C中发生反应的主要化学方程式:
(5)装置D中 NaOH的作用是
(6)他们在读出量筒内水的体积数后,折算成标准状况下氧气的体积为224mL,则样品中过氧化钠的质量分数为
您最近一年使用:0次
名校
2 . 下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向包有Na2O2粉末的脱脂棉滴2滴水 | 脱脂棉燃烧 | Na2O2与水反应放热 |
| B | Fe(NO3)2样品中加入稀硫酸,再滴加KSCN溶液 | 溶液变为血红色 | Fe(NO3)2样品已经变质 |
| C | 向FeCl3溶液中加入Mg(OH)2悬浊液,振荡 | 沉淀由白色变为红褐色 | Fe(OH)3的溶度积小于Mg(OH)2 |
| D | 向蔗糖溶液中加入稀硫酸,加热几分钟后加入新制Cu(OH)2悬浊液,加热煮沸 | 无红色沉淀生成 | 蔗糖没有发生水解反应生成葡萄糖 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-04-01更新
|
1118次组卷
|
3卷引用:西藏拉萨中学2020届高三上学期第二次月考理综化学试题
名校
3 . 由下列实验及现象不能推出相应结论的是
选项 | 实验 | 现象 | 结论 |
A | 用煮沸过的蒸馏水将Na2SO3固体样品溶解,加入足量稀盐酸酸化,再加入氯化钡溶液 | 有白色沉淀产生 | Na2SO3样品已变质 |
B | 向硅酸钠溶液中滴加1滴酚酞溶液,然后逐滴加入稀盐酸至红色变浅并接近消失时停止 | 试管里出现凝胶 | 非金属性:Cl>Si |
C | 向盛有浓氨水的锥形瓶中通入氧气, 并将灼热的铂丝置于液面上方 | 铂丝保持红热,且瓶内有白烟产生 | 氨水易挥发 |
D | 将金属钠放入燃烧匙中,点燃,迅速伸入集满SO2的集气瓶 | 产生大量黄色的烟,且瓶内有白色颗粒生成 | SO2具有氧化性 |
| A.A | B..B | C.C | D.D |
您最近一年使用:0次
2017-11-01更新
|
307次组卷
|
2卷引用:西藏自治区拉萨中学2018届高三上学期第四次月考理综化学试题
名校
4 . 钴酸锂(LiCoO2)电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
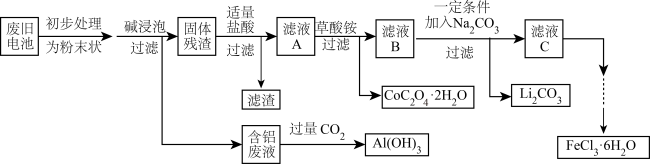
已知:①还原性:Cl->Co2+;
②Fe3+和 结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
(1)钴的价格高,仅产于非洲的一部分地区。据此你推测此类电池的一个缺点是_______ 。此类废旧电池初步处理为粉末状的目的是_______ 。
(2)碱浸泡过滤过程中使用的碱的化学式为_______ 。从含铝废液得到Al(OH)3的离子方程式为_______
(3)滤液A中的溶质除HCl、LiCl外还有_______ (填化学式)。写出LiCoO2和盐酸反应的化学方程式_______ 。
(4)滤渣的主要成分为_______ (填化学式)。
(5)在空气中加热一定质量的CoC2O4·2H2O固体样品时,其固体失重率数据见下表,请补充完整表中问题。
已知:①CoC2O4在空气中加热时的气体产物为CO2。
②固体失重率=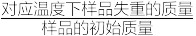 。
。
(6)已知Li2CO3的溶度积常数Ksp=8.64×10-4,将浓度为0.02mol·L-1的Li2SO4和浓度为0.02mol·L-1的Na2CO3溶液等体积混合,则溶液中的Li+浓度为_______ mol·L-1。

已知:①还原性:Cl->Co2+;
②Fe3+和
 结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:(1)钴的价格高,仅产于非洲的一部分地区。据此你推测此类电池的一个缺点是
(2)碱浸泡过滤过程中使用的碱的化学式为
(3)滤液A中的溶质除HCl、LiCl外还有
(4)滤渣的主要成分为
(5)在空气中加热一定质量的CoC2O4·2H2O固体样品时,其固体失重率数据见下表,请补充完整表中问题。
已知:①CoC2O4在空气中加热时的气体产物为CO2。
②固体失重率=
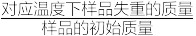 。
。| 序号 | 温度范围/℃ | 化学方程式 | 固体失重率 |
| Ⅰ | 120~220 | CoC2O4·2H2O=CoC2O4+2H2O | 19.67% |
| Ⅱ | 300~350 | 59.02% |
(6)已知Li2CO3的溶度积常数Ksp=8.64×10-4,将浓度为0.02mol·L-1的Li2SO4和浓度为0.02mol·L-1的Na2CO3溶液等体积混合,则溶液中的Li+浓度为
您最近一年使用:0次
5 . I.人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
配制KMnO4标准溶液:如图是配制50mLKMnO4标准溶液的过程示意图。

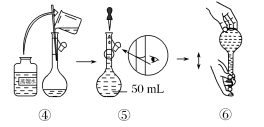
(1)请你观察图示判断,其中不正确的操作有_______ (填序号)。
(2)其中确定50mL溶液体积的容器是_______ (填名称)。
(3)如果用上图所示操作配制溶液则浓度将_______ (填“偏大”或“偏小”或“无影响”)。
II.实验室利用如下原理制备Cl2,MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:
(4)制备Cl2的反应中氧化剂是_______ ,还原剂是_______ ,氧化产物是_______ ,盐酸表现的性质有_______ 和_______ 。
配制KMnO4标准溶液:如图是配制50mLKMnO4标准溶液的过程示意图。


(1)请你观察图示判断,其中不正确的操作有
(2)其中确定50mL溶液体积的容器是
(3)如果用上图所示操作配制溶液则浓度将
II.实验室利用如下原理制备Cl2,MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:(4)制备Cl2的反应中氧化剂是
您最近一年使用:0次
6 . 某化学小组用部分氧化的FeSO4为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧化铁(Fe2O3),并进行铁含量的测定。主要操作步骤如下:
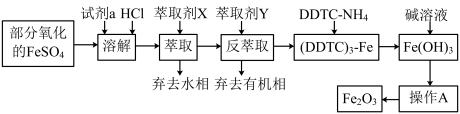
已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
②3DDTC-NH4+Fe3+=(DDTC)3-Fe↓+3NH 。
。
请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式_________ 。
(2)溶液中加入萃取剂X,转移至分液漏斗中,塞上玻璃塞振摇,振摇几次后需打开分液漏斗的___ 放气;为提高萃取率和产品产量,实验时应进行的操作是__________ 。
(3)可作反萃取的萃取剂Y的最佳试剂是(填试剂名称)____ 。
(4)操作A为_____ 、_____ 、______ 。产品处理时,温度对产品的纯度有很大影响。已知温度对产物纯度的影响如图所示,则温度最好控制在______ ℃。

(5)现准确称取4.000g样品,经酸溶、还原为Fe2+,在容量瓶中配成100mL溶液,用______ (填仪器名称)移取25.00 mL溶液于锥形瓶中,用0.l000mol/L的K2Cr2O7溶液进行滴定,消耗K2Cr2O7溶液20.60mL。产品中铁的含量为______ (假设杂质不与K2Cr2O7反应)。

已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
②3DDTC-NH4+Fe3+=(DDTC)3-Fe↓+3NH
 。
。请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式
(2)溶液中加入萃取剂X,转移至分液漏斗中,塞上玻璃塞振摇,振摇几次后需打开分液漏斗的
(3)可作反萃取的萃取剂Y的最佳试剂是(填试剂名称)
(4)操作A为

(5)现准确称取4.000g样品,经酸溶、还原为Fe2+,在容量瓶中配成100mL溶液,用
您最近一年使用:0次
2020-07-28更新
|
389次组卷
|
6卷引用:西藏拉萨中学2021届高三上学期第五次月考化学试题
真题
名校
7 . K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]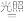 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________ 。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是________________________________________ 。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________ 、___________ 。
③为防止倒吸,停止实验时应进行的操作是_____________________________ 。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________ 。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________ 。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为________________________________ 。
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]
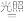 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
③为防止倒吸,停止实验时应进行的操作是
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为
您最近一年使用:0次
2018-06-09更新
|
13217次组卷
|
19卷引用:西藏自治区拉萨中学2022届高三第六次月考理综化学试题
西藏自治区拉萨中学2022届高三第六次月考理综化学试题西藏林芝市第二高级中学2022-2023学年高三上学期第二次月考化学试题2018年全国普通高等学校招生统一考试化学(新课标II卷)(已下线)2018年高考题及模拟题汇编 专题16 化学实验综合题四川省攀枝花市第十二中学2019届高三上学期10月月考化学试题广东省惠州市第一中学2019届高三上学期理科综合测试(二)化学试题云南省马关县二中2020届高三上学期开学考试化学试题云南省玉溪元江民中2020届高三开学考试化学试题云南省富宁县民族中学2020届高三上学期开学考试化学试题云南省大理白族自治州漾濞二中2019—2020学年9月份高三化学考试试题云南省富宁县第一中学2020届高三第一学期开学考试化学试题四川省自贡市田家炳中学2020届高三上学期期中考试化学试题(已下线)专题10.3 化学实验方案的设计与评价 (讲)-《2020年高考一轮复习讲练测》黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题山东省潍坊市诸城一中2021届高三11月份模拟化学试题(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点35 化学实验方案的设计与评价-备战2022年高考化学一轮复习考点帮(浙江专用)重庆市开州中学高 2021-2022学年高三上学期10月月考化学试题(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)
名校
8 . 某同学欲探究Na2O2与水的反应,可供使用的试剂有:Na2O2、蒸馏水、酸性KMnO4溶液、MnO2。该同学取一定量Na2O2样品与过量水反应,待完全反应后,得到溶液X和一定量O2,该同学推测反应中可能生成了H2O2,并进行实验探究。
(1)写出Na2O2与水反应的化学方程式_______________________________________ 。
(2)试设计实验证明溶液X中含过氧化氢____________________________________ 。
(3)通过上述实验证明溶液中确实存在H2O2。取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:______ H2O2+______ Fe2++_____ OH-===______ Fe(OH)3↓,该反应中H2O2表现了_______ (填“氧化”或“还原”)性。
(4)已知溶液X可使酸性KMnO4溶液褪色,已知高锰酸钾产物为Mn2+,此时H2O2表现了______ (填“氧化”或“还原”)性。该反应的离子方程式为____________________ 。
(1)写出Na2O2与水反应的化学方程式
(2)试设计实验证明溶液X中含过氧化氢
(3)通过上述实验证明溶液中确实存在H2O2。取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:
(4)已知溶液X可使酸性KMnO4溶液褪色,已知高锰酸钾产物为Mn2+,此时H2O2表现了
您最近一年使用:0次
9 . 为了测定某仅含碳、氢、氧三种元素组成的有机化合物的结构,进行了如下实验。首先取该有机化合物样品4.6 g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重5.4 g和8.8 g;然后用质谱仪测定其相对分子质量,经测定得到如图所示的质谱图;最后用核磁共振仪处理该有机物,得到如图所示的核磁共振氢谱图。
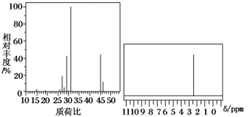
试回答下列问题:
(1)该有机化合物的相对分子质量为________ ;
(2)该有机物的实验式为________ ;
(3)能否根据该有机物的实验式确定其分子式________ (填“能”或“不能”),原因是________ ,该有机化合物的分子式为________ 。
(4)请写出该有机化合物的结构简式________ 。

试回答下列问题:
(1)该有机化合物的相对分子质量为
(2)该有机物的实验式为
(3)能否根据该有机物的实验式确定其分子式
(4)请写出该有机化合物的结构简式
您最近一年使用:0次
2017-04-22更新
|
410次组卷
|
2卷引用:2016-2017学年西藏自治区拉萨中学高二第五次月考化学试卷



