1 . (1)甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5KJ热量,则甲烷燃烧的热化学方程式为_________________________ 。
(2)能证明甲烷是正四面体结构的理由是________________
①中心原子C采取sp3杂化,②中心原子C上没有孤对电子,
③CH2Cl2不存在同分异构体,④键角是109028,,而不是900
(2)能证明甲烷是正四面体结构的理由是
①中心原子C采取sp3杂化,②中心原子C上没有孤对电子,
③CH2Cl2不存在同分异构体,④键角是109028,,而不是900
您最近半年使用:0次
2 . 宇宙中所有的一切都是能量的变化,研究化学反应中的能量变化意义重大。
(1)奥运会火炬常用的燃料为丙烷、丁烷等。已知:丙烷的燃烧热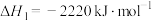 ,正丁烷的燃烧热
,正丁烷的燃烧热 ;异丁烷的燃烧热
;异丁烷的燃烧热 。下列有关说法正确的是
。下列有关说法正确的是_______ (填字母)。
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.燃烧等质量的正丁烷、异丁烷放热更多的是异丁烷
C.正丁烷比异丁烷稳定
(2)根据丙烷的燃烧热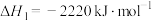 ,
,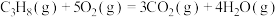

 ,则a
,则a___________ 2220(填“<”或“>”或“=”)。
(3)用 催化还原氮氧化物可以消除氮氧化物的污染。已知:
催化还原氮氧化物可以消除氮氧化物的污染。已知:
①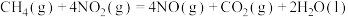
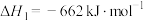
②
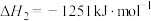
则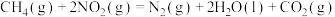

___________ 。
(4)已知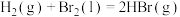
 ,其他相关数据如下表:
,其他相关数据如下表:
则表中a=___________ ;根据键能大小可判断,上述三种物质中最稳定的是___________ 。
(5)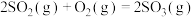 反应过程的能量变化如图所示。
反应过程的能量变化如图所示。

已知:1mol (g)氧化为1mol
(g)氧化为1mol  (g)的
(g)的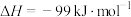 。请回答下列问题:
。请回答下列问题:
①图中
___________ 。
②根据上述计算的焓变值,阐述热化学方程式: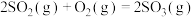
 代表的含义
代表的含义___________ 。
(1)奥运会火炬常用的燃料为丙烷、丁烷等。已知:丙烷的燃烧热
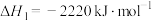 ,正丁烷的燃烧热
,正丁烷的燃烧热 ;异丁烷的燃烧热
;异丁烷的燃烧热 。下列有关说法正确的是
。下列有关说法正确的是A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.燃烧等质量的正丁烷、异丁烷放热更多的是异丁烷
C.正丁烷比异丁烷稳定
(2)根据丙烷的燃烧热
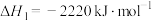 ,
,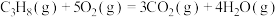

 ,则a
,则a(3)用
 催化还原氮氧化物可以消除氮氧化物的污染。已知:
催化还原氮氧化物可以消除氮氧化物的污染。已知:①
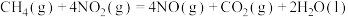
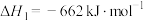
②

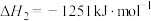
则
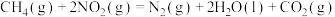

(4)已知
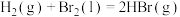
 ,其他相关数据如下表:
,其他相关数据如下表:| 物质 |  (g) (g) |  (l) (l) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 230 | a |
(5)
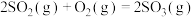 反应过程的能量变化如图所示。
反应过程的能量变化如图所示。
已知:1mol
 (g)氧化为1mol
(g)氧化为1mol  (g)的
(g)的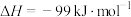 。请回答下列问题:
。请回答下列问题:①图中

②根据上述计算的焓变值,阐述热化学方程式:
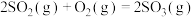
 代表的含义
代表的含义
您最近半年使用:0次
名校
3 . 利用CO2(g)与H2(g)反应生成CH3OCH3(g)和H2O(g)有利于实现碳中和,其反应过程中的能量变化如图所示。下列有关说法正确的是
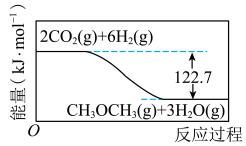

| A.若该反应在绝热密闭容器中进行,则反应过程中体系温度会降低 |
| B.1 molH2(g)在O2(g)中完全燃烧生成H2O(g)时放出的热量大于20.45kJ |
| C.若反应消耗0.4 molCO2(g)和1.2molH2(g),则该反应放出49.08kJ热量 |
| D.CH3OCH3(g)+3H2O(g)=2CO2(g) +6H2(g) ∆H=-122.7 kJ·mol-1 |
您最近半年使用:0次
2023-10-17更新
|
152次组卷
|
2卷引用:山东学情2023-2024学年高二上学期10月质量检测(鲁科版)化学试题
解题方法
4 .  ,有关物质的能量转化图如图,又已知
,有关物质的能量转化图如图,又已知 是
是 的稳定氧化物,试分析计算并回答下列说法不正确的是
的稳定氧化物,试分析计算并回答下列说法不正确的是

 ,有关物质的能量转化图如图,又已知
,有关物质的能量转化图如图,又已知 是
是 的稳定氧化物,试分析计算并回答下列说法不正确的是
的稳定氧化物,试分析计算并回答下列说法不正确的是
A. 时,单质 时,单质 的标准燃烧热: 的标准燃烧热: |
B.若 的摩尔质量为 的摩尔质量为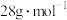 ,则 ,则 的热值为 的热值为 |
C.转化Ⅱ的热化学方程式为: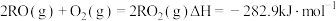 |
D.由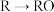 的热化学方程式为: 的热化学方程式为: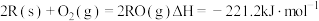 |
您最近半年使用:0次
5 .  是结构最简单的非金属单质,也是一种重要的清洁能源。对
是结构最简单的非金属单质,也是一种重要的清洁能源。对 分子结构有助于理解物质的微观结构。完成下列填空:
分子结构有助于理解物质的微观结构。完成下列填空:
(1)下列与氢原子有关的说法中,错误的是
(2)如图是 分子形成过程中的体系能量变化。以下关于氢气分子中成键状况的表达错误的是
分子形成过程中的体系能量变化。以下关于氢气分子中成键状况的表达错误的是
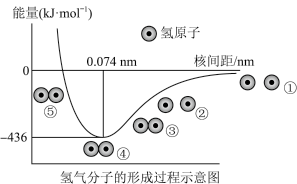
(3) 分子中,两个氢原子的核间距为
分子中,两个氢原子的核间距为_______ ,键能为_______  。
。
(4) 被誉为21世纪人类最理想的燃料。根据下表数据和本题信息,每千克
被誉为21世纪人类最理想的燃料。根据下表数据和本题信息,每千克 燃烧(生成水蒸气)放出的热量约为
燃烧(生成水蒸气)放出的热量约为_______  。
。
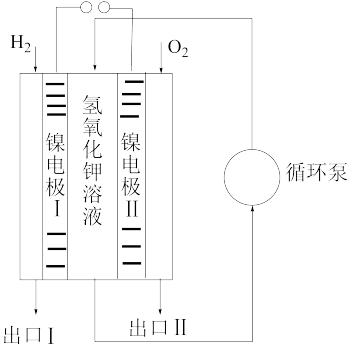
(5) 可用于燃料电池。某种碱性氢氧燃料电池原理如图所示,下列有关该电池的说法正确的是
可用于燃料电池。某种碱性氢氧燃料电池原理如图所示,下列有关该电池的说法正确的是
(6)储氢是氢能利用的关键。一种环保,安全的储氢原理为: 。有关该过程说法正确的是
。有关该过程说法正确的是
 是结构最简单的非金属单质,也是一种重要的清洁能源。对
是结构最简单的非金属单质,也是一种重要的清洁能源。对 分子结构有助于理解物质的微观结构。完成下列填空:
分子结构有助于理解物质的微观结构。完成下列填空:(1)下列与氢原子有关的说法中,错误的是
| A.氢原子电子云图中小黑点的疏密表示电子在该区域出现的概率密度 |
| B.霓虹灯能的发光机理与氢原子光谱形成机理基本相同 |
| C.利用玻尔原子结构模型可以较好地解释氢原子光谱为线状光谱 |
| D.氢原子核外只有一个电子,它产生的原子光谱中只有一根或明或暗的线 |
 分子形成过程中的体系能量变化。以下关于氢气分子中成键状况的表达错误的是
分子形成过程中的体系能量变化。以下关于氢气分子中成键状况的表达错误的是
A. | B.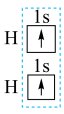 | C. | D. |
 分子中,两个氢原子的核间距为
分子中,两个氢原子的核间距为 。
。(4)
 被誉为21世纪人类最理想的燃料。根据下表数据和本题信息,每千克
被誉为21世纪人类最理想的燃料。根据下表数据和本题信息,每千克 燃烧(生成水蒸气)放出的热量约为
燃烧(生成水蒸气)放出的热量约为 。
。| 化学键 | 键能( ) ) |
 | 467 |
 | 498 |
 可用于燃料电池。某种碱性氢氧燃料电池原理如图所示,下列有关该电池的说法正确的是
可用于燃料电池。某种碱性氢氧燃料电池原理如图所示,下列有关该电池的说法正确的是
A.出口Ⅰ处有 生成 生成 |
| B.循环泵可使电解质溶液不断浓缩循环 |
C.电池放电时, 向镍电极I的方向迁移 向镍电极I的方向迁移 |
D.正极电极反应为: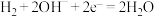 |
 。有关该过程说法正确的是
。有关该过程说法正确的是| A.储氢过程无能量变化 |
B.储氢过程中, 被氧化 被氧化 |
| C.储氢过程存在非极性键的断裂与极性键的形成 |
D.储氢过程中,每生成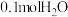 ,转移 ,转移 电子 电子 |
您最近半年使用:0次
名校
解题方法
6 . 下列说法或表示方法中,正确的是
A.由热化学方程式: C2H5OH(l)+ C2H5OH(l)+  O2(g)=CO2(g)+ O2(g)=CO2(g)+  H2O(l) ΔH=-683.4 kJ∙mol−1知乙醇的燃烧热为683.4 kJ∙mol−1 H2O(l) ΔH=-683.4 kJ∙mol−1知乙醇的燃烧热为683.4 kJ∙mol−1 |
| B.由C(金刚石)→ C(石墨) ΔH= −119 kJ∙mol−1可知,金刚石比石墨稳定 |
| C.H+(aq) + OH一(aq) = H2O(1) ΔH=−57.3 kJ∙mol−1。若将含0.5mol H2SO4的浓硫酸与含1molNaOH的稀溶液混合,放出的热量大于57.3 kJ |
| D.在101kPa 25℃时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,则氢气燃烧的热化学方程式表示为:2H2(g) + O2(g) = 2H2O(1) ΔH = −285.8 kJ∙mol−1 |
您最近半年使用:0次
名校
解题方法
7 . 已知CH4(g)、CO(g)和H2(g)的摩尔燃烧焓(△H)分别为—890.3kJ•mol-1、—283.0kJ•mol-1和—285.8kJ•mol-1,氢气与氧气反应生成气态水和液态水的热效应如图所示,下列有关说法正确的是
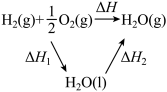

| A.反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的△H=—237.3kJ•mol-1 |
| B.1molCH4(g)充分燃烧生成CO2(g)和气态水,放出的热量为890.3kJ—2△H2 |
| C.当氢氧燃料电池负极消耗1mol氢气时,可释放的电能小于285.8kJ |
| D.图示过程中△H=△H1-△H2 |
您最近半年使用:0次
2023-04-29更新
|
252次组卷
|
2卷引用:山东省菏泽市2022-2023学年高一下学期期中考试化学(A)试题
8 . 用CH4催化还原NO2可以消除氮氧化物的污染。例如:
①
②
下列说法错误的是
①

②

下列说法错误的是
| A.反应①②中,相同物质的量的甲烷发生反应,转移的电子数相同 |
| B.若用标准状况下4.48LCH4还原NO2生成N2和H2O(g),放出的热量为173.4kJ |
C.由反应①可知: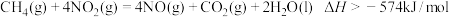 |
D.已知CH4的燃烧热为akJ/mol,由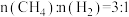 组成的混合物2mol,完全燃烧并恢复到常温时放出的热量为bkJ,则H2的燃烧热为 组成的混合物2mol,完全燃烧并恢复到常温时放出的热量为bkJ,则H2的燃烧热为 |
您最近半年使用:0次
2023-05-15更新
|
388次组卷
|
3卷引用: 重庆市第一中学校2022-2023学年高一下学期期中考试化学试题
名校
9 . 北京奥运会“祥云”奥运火炬所用环保型燃料为丙烷( ),悉尼奥运会所用火炬燃料为65%丁烷(
),悉尼奥运会所用火炬燃料为65%丁烷( )和
)和 丙烷。
丙烷。
已知: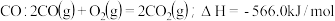 。
。
丙烷: 。
。
正丁烷: 。
。
异丁烷: 。
。
下列有关说法正确的是
 ),悉尼奥运会所用火炬燃料为65%丁烷(
),悉尼奥运会所用火炬燃料为65%丁烷( )和
)和 丙烷。
丙烷。已知:
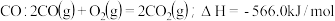 。
。丙烷:
 。
。正丁烷:
 。
。异丁烷:
 。
。下列有关说法正确的是
A.常温下,正丁烷的燃烧热为 |
| B.相同质量的丙烷和正丁烷分别完全燃烧,前者需要的氧气少产生的热量也多 |
C.常温下, 的燃烧热为 的燃烧热为 |
| D.人类利用的能源都是通过化学反应获得的 |
您最近半年使用:0次
10 . 已知25℃、101kPa下,1mol水蒸发为水蒸气需要吸热44.0kJ
①H+(aq)+OH-(aq)=H2O(l)△H1=-57.3kJ•mol-1
②2CH3OH(l)+3O2(g)=4H2O(g)+2CO2(g)△H2=-1277.0kJ•mol-1
下列有关说法错误的是
①H+(aq)+OH-(aq)=H2O(l)△H1=-57.3kJ•mol-1
②2CH3OH(l)+3O2(g)=4H2O(g)+2CO2(g)△H2=-1277.0kJ•mol-1
下列有关说法错误的是
| A.若反应②中CH3OH变为气态,则该反应的反应热△H>△H2 |
| B.CH3OH(l)的燃烧热△H=-726.5kJ•mol-1 |
| C.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l)△H>﹣57.3kJ•mol-1 |
| D.液态水变为水蒸气过程中需要克服分子间作用力 |
您最近半年使用:0次
2021-04-13更新
|
629次组卷
|
6卷引用:河北省秦皇岛市2021届普通高中学业水平选择性考试第二次模拟演练化学试题
河北省秦皇岛市2021届普通高中学业水平选择性考试第二次模拟演练化学试题(已下线)押山东卷第07题 化学反应与能量-备战2021年高考化学临考题号押题(山东卷)(已下线)第17讲 化学能与热能(精讲)-2022年一轮复习讲练测河南省商城县观庙高级中学2021-2022学年高二上学期12月月考化学试题(已下线)第03讲 盖斯定律(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)江西省九校2022-2023学年高二下学期开学联考化学试题



