名校
1 . 依据下图中氮元素及其化合物的转化关系,回答下列问题。

(1)过程II是氨的催化氧化,其化学方程式是_______ 。
(2)过程IV的化学方程式为_______ 。
(3)过程V可对NO2进行尾气处理,产物除NaNO2外,还有两种常见物质(其中一种是气体),反应的化学方程式为_______ 。
(4)一定条件下,在2L的密闭容器中,进行N2和H2合成NH3的反应。反应过程中测得各气体的物质的量如下图所示。回答下列问题:

①用H2表示0~2min内该反应的平均速率为_______ 。
②第2min末,N2的转化率为_______ 。
③能说明该反应已经达到平衡状态的是_______ 。
a.气体的密度不随时间而改变
b.体系总物质的量不随时间而改变
c.N2和H2的浓度比为1:3
d.H2的体积百分数保持恒定

(1)过程II是氨的催化氧化,其化学方程式是
(2)过程IV的化学方程式为
(3)过程V可对NO2进行尾气处理,产物除NaNO2外,还有两种常见物质(其中一种是气体),反应的化学方程式为
(4)一定条件下,在2L的密闭容器中,进行N2和H2合成NH3的反应。反应过程中测得各气体的物质的量如下图所示。回答下列问题:

①用H2表示0~2min内该反应的平均速率为
②第2min末,N2的转化率为
③能说明该反应已经达到平衡状态的是
a.气体的密度不随时间而改变
b.体系总物质的量不随时间而改变
c.N2和H2的浓度比为1:3
d.H2的体积百分数保持恒定
您最近一年使用:0次
2 . 研究碳、氮、硫等元素化合物的性质或转化对建设生态文明,美丽中国具有重要意义。
(1)基态氮原子的价层电子轨道表示式为:______ 。
(2)NO加速臭氧层被破坏,其反应过程如下图所示:
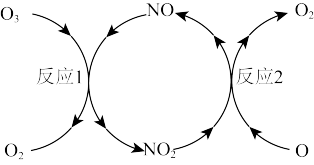
已知: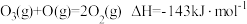
反应1: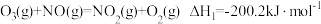 。
。
反应2的热化学方程式为___________ 。
(3)工业上以CO和 为原料合成甲醇的反应:
为原料合成甲醇的反应: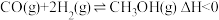 ,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
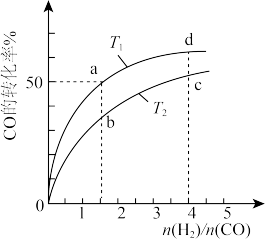
①判断T1___________ T2 (选填“<”、“>”或“=”);
②若a点达到平衡的时间是10分钟,从反应开始到平衡用H2表示的反应速率为
___________ ;
③该反应平衡常数的表达式为K=___________ ,d点的平衡常数的值为___________ ;
④a点状态下再通入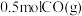 和
和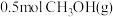 ,平衡
,平衡____ 移动(选填“正向”、“逆向”或“不”);
⑤a、b、c三点H2转化率由大到小的顺序是___________ 。
(1)基态氮原子的价层电子轨道表示式为:
(2)NO加速臭氧层被破坏,其反应过程如下图所示:

已知:
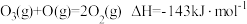
反应1:
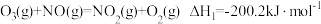 。
。反应2的热化学方程式为
(3)工业上以CO和
 为原料合成甲醇的反应:
为原料合成甲醇的反应: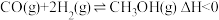 ,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
①判断T1
②若a点达到平衡的时间是10分钟,从反应开始到平衡用H2表示的反应速率为

③该反应平衡常数的表达式为K=
④a点状态下再通入
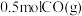 和
和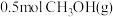 ,平衡
,平衡⑤a、b、c三点H2转化率由大到小的顺序是
您最近一年使用:0次
2022-02-16更新
|
302次组卷
|
2卷引用:重庆市七校2021-2022学年高二上学期期末考试化学试题



