1 . 完成下列问题。
(1)画出下面反应过渡态的前线轨道示意图___________ 。
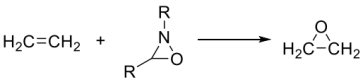
(2)试比较下列各组中两个化合物的第一电离势(IP1)大小,并简述理由。
(i) :
:___________ 。
(ii) :
:___________ 。
(iii) :
:___________ 。
(iv) :
:___________ 。
(3)为以下反应结果给出一个合适的解释(最好画出反应的过渡态)___________ 。
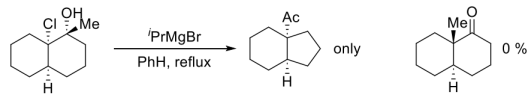
(4)下列烯烃与BH3发生硼氢化反应的速率从快到慢的排序为___________ 。
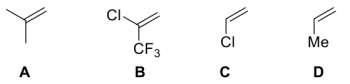
(5)下列二醇被高碘酸氧化的速率从快到慢的排序为___________ 。

(6)为什么负离子亲核试剂,例如碳负离子,在DMSO中的亲核性会显著增强___________ ?
(7)相比于四氢呋喃中,碘负离子的亲核性在甲醇中是更强还是更弱,为什么___________ ?
(1)画出下面反应过渡态的前线轨道示意图

(2)试比较下列各组中两个化合物的第一电离势(IP1)大小,并简述理由。
(i)
 :
:(ii)
 :
:(iii)
 :
:(iv)
 :
:(3)为以下反应结果给出一个合适的解释(最好画出反应的过渡态)

(4)下列烯烃与BH3发生硼氢化反应的速率从快到慢的排序为

(5)下列二醇被高碘酸氧化的速率从快到慢的排序为

(6)为什么负离子亲核试剂,例如碳负离子,在DMSO中的亲核性会显著增强
(7)相比于四氢呋喃中,碘负离子的亲核性在甲醇中是更强还是更弱,为什么
您最近一年使用:0次
2 . 当某反应物的初始浓度为0.04 mol·dm-3时,反应的半衰期为400s,初始浓度为0.024 mol·dm-3时,半衰期为240s,则此反应为
| A.零级反应 | B.1.5级反应 | C.二级反应 | D.一级反应 |
您最近一年使用:0次
2023-05-25更新
|
357次组卷
|
2卷引用:2023年广西高中学生竞赛(高一、高二同卷)化学试题
3 . 2022 年北京大学课题组发现[4+2)]反应并对反应机理进行研究,该[4+2]反应是通过在环丁酮2-位引入乙烯基取代作为导向基诱导铑对环丁酮的碳-碳键活化,同时酮碳基可以与路易斯酸配位,进一步活化环丁酮的碳-碳键。这一协同催化模式选择性切断羰基与季碳中心之间的碳-碳键,不仅成功地构建六元环系,还成功拓展到烷基及多种电子效应的芳基上,大部分底物都具有中等到良好的收率,对氰基,酮羰基,酯基及酰胺等官能团具有良好的兼容性,机理如下图,下列表述错误的是
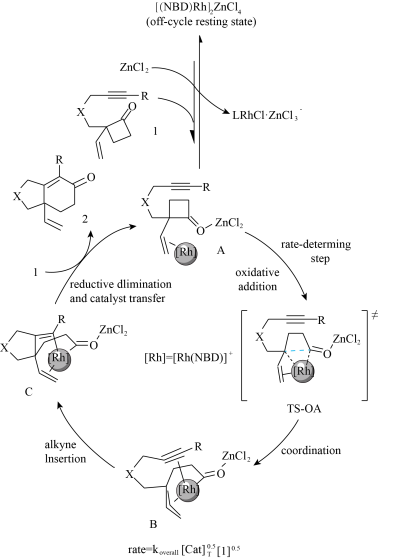

| A.生成TS-OA发生了氧化加成,这一步被认为是反应的决速步 |
| B.其中ZnCl2被认为具有促进C-C的活化和原位生成活性阳离子铑的作用 |
| C.由TS-OA生成B有配位键的形成 |
| D.该反应为合成4元环物质提供一种新的 C-C耦合方式 |
您最近一年使用:0次
2023-05-25更新
|
529次组卷
|
3卷引用:2023年广西高中学生竞赛(高一、高二同卷)化学试题
名校
4 . I.某温度时,在0.5L密闭容器中,某一可逆反应的A、B气体物质的量随时间变化的曲线如下图所示,由图中数据分析可得:
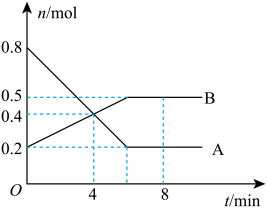
(1)该反应的化学方程式为___________ 。
(2)第4min时,正、逆反应速率的大小关系为v正___________ (填“>” “<”或“=”)v逆
(3)0~ 4min内,用B的浓度变化来表示该反应的平均反应速率为___________ mol ·L-1·min-1。
(4)平衡时混合气体中B的体积分数为___________ 。
II.某同学根据外界条件对化学反应速率影响的原理,设计了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如下表,请结合表中信息,回答有关问题:
(5)写出上述反应的离子方程式___________ 。
(6)若实验探究温度对该反应速率的影响,则a=___________ 采用比较实验的序号是___________ (填实验序号)

(1)该反应的化学方程式为
(2)第4min时,正、逆反应速率的大小关系为v正
(3)0~ 4min内,用B的浓度变化来表示该反应的平均反应速率为
(4)平衡时混合气体中B的体积分数为
II.某同学根据外界条件对化学反应速率影响的原理,设计了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如下表,请结合表中信息,回答有关问题:
| 实验序号 | 反应温度(°C) | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
| A | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| B | 20 | 5 | 0.1 | 10 | 0.1 | a |
| C | 25 | 10 | 0.1 | 5 | 0.1 | 5 |
| D | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
(6)若实验探究温度对该反应速率的影响,则a=
您最近一年使用:0次
2023-05-16更新
|
330次组卷
|
2卷引用:广东省揭阳市普宁市勤建学校2022-2023学年高一下学期学科竞赛化学试题
名校
解题方法
5 . 一定条件下,反应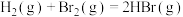 的速率方程为
的速率方程为 ,某温度下,该反应在不同浓度下的反应速率如下:
,某温度下,该反应在不同浓度下的反应速率如下:
根据表中的测定结果,下列结论错误的是
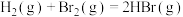 的速率方程为
的速率方程为 ,某温度下,该反应在不同浓度下的反应速率如下:
,某温度下,该反应在不同浓度下的反应速率如下: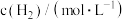 |  | 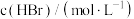 | 反应速率 |
| 0.1 | 0.1 | 2 |  |
| 0.1 | 0.4 | 2 | 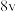 |
| 0.2 | 0.4 | 2 |  |
| 0.4 | 0.1 | 4 | 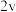 |
| 0.2 | 0.1 |  |  |
| A.α、β、γ的值分别为1、1.5、-1 |
| B.表中m的值为1 |
C.反应体系中的物质, 的浓度对反应速率影响最大 的浓度对反应速率影响最大 |
D.若其它条件不变,增大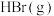 的浓度,则反应速率增大 的浓度,则反应速率增大 |
您最近一年使用:0次
2023-05-10更新
|
607次组卷
|
3卷引用:重庆市2022-2023学年高一下学期化学竞赛试题
名校
解题方法
6 . 中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。下列说法不正确的是
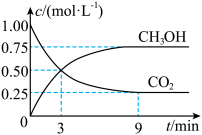

| A.从3min到9min,v(H2)为0.125mol·L-1·min-1 |
| B.若混合气体密度不变时,该反应达平衡状态 |
| C.平衡时向容器中充入Ne,反应速率不变 |
| D.9min时,反应处于平衡状态 |
您最近一年使用:0次
2023-04-27更新
|
264次组卷
|
3卷引用:广东省揭阳市普宁市勤建学校2022-2023学年高一下学期学科竞赛化学试题



