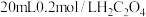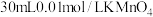1 . 甲、乙两个实验小组同学分别用酸性 和
和 (草酸)溶液反应来探究影响反应速率的因素:
(草酸)溶液反应来探究影响反应速率的因素:
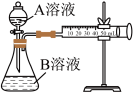
Ⅰ.甲组同学欲通过如图装置探究某种影响化学反应速率的因素,设计实验方案如下( 溶液已酸化):
溶液已酸化):
(1)写出酸性 溶液和
溶液和 (草酸)溶液反应的离子方程式
(草酸)溶液反应的离子方程式__________ 。
(2)相同时间内针筒中所得 的体积大小关系是①
的体积大小关系是①__________ ②(填“>”、“<”或“=”)。
(3)该小组同学发现反应速率总是如下图所示,其中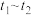 时间内速率变快的主要原因可能是:①产物
时间内速率变快的主要原因可能是:①产物 对该反应有催化作用:②
对该反应有催化作用:②__________ 。
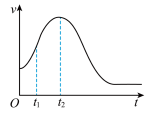
(4)对于反应 ,速率方程
,速率方程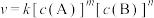 ,k为速率常数(只受温度影响),
,k为速率常数(只受温度影响),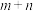 为反应级数。已知
为反应级数。已知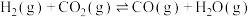
 ,CO的瞬时生成速率
,CO的瞬时生成速率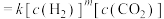 。一定温度下,控制
。一定温度下,控制 起始浓度为
起始浓度为 ,改变
,改变 的起始浓度,进行上述反应,得到CO的瞬时生成速率和
的起始浓度,进行上述反应,得到CO的瞬时生成速率和 起始浓度呈如图所示的直线关系。
起始浓度呈如图所示的直线关系。

①该反应的反应级数为__________ 。
②速率常数
__________ 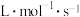 。
。
③当 的起始浓度为
的起始浓度为 ,反应进行到某一时刻时,测得
,反应进行到某一时刻时,测得 的浓度为
的浓度为 ,此时CO的瞬时生成速率
,此时CO的瞬时生成速率
__________  。
。
④该反应的反应速率(v)随时间(t)的变化关系如图所示,若 、
、 时刻只改变一个条件,下列说法错误的是
时刻只改变一个条件,下列说法错误的是__________ (填标号)。
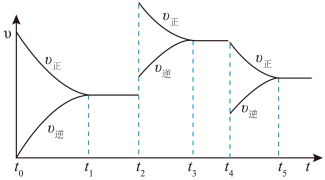
a.在 时,采取的措施可以是升高温度
时,采取的措施可以是升高温度
b.在 时,采取的措施可以是增大
时,采取的措施可以是增大 的浓度
的浓度
c.在 时,容器内
时,容器内 的转化率是整个过程中的最大值
的转化率是整个过程中的最大值
 和
和 (草酸)溶液反应来探究影响反应速率的因素:
(草酸)溶液反应来探究影响反应速率的因素:Ⅰ.甲组同学欲通过如图装置探究某种影响化学反应速率的因素,设计实验方案如下(
 溶液已酸化):
溶液已酸化):
实验序号 | A溶液 | B溶液 |
① |
|
|
② |
|
|
(1)写出酸性
 溶液和
溶液和 (草酸)溶液反应的离子方程式
(草酸)溶液反应的离子方程式(2)相同时间内针筒中所得
 的体积大小关系是①
的体积大小关系是①(3)该小组同学发现反应速率总是如下图所示,其中
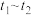 时间内速率变快的主要原因可能是:①产物
时间内速率变快的主要原因可能是:①产物 对该反应有催化作用:②
对该反应有催化作用:②
(4)对于反应
 ,速率方程
,速率方程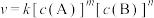 ,k为速率常数(只受温度影响),
,k为速率常数(只受温度影响),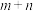 为反应级数。已知
为反应级数。已知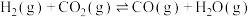
 ,CO的瞬时生成速率
,CO的瞬时生成速率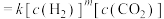 。一定温度下,控制
。一定温度下,控制 起始浓度为
起始浓度为 ,改变
,改变 的起始浓度,进行上述反应,得到CO的瞬时生成速率和
的起始浓度,进行上述反应,得到CO的瞬时生成速率和 起始浓度呈如图所示的直线关系。
起始浓度呈如图所示的直线关系。
①该反应的反应级数为
②速率常数

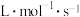 。
。③当
 的起始浓度为
的起始浓度为 ,反应进行到某一时刻时,测得
,反应进行到某一时刻时,测得 的浓度为
的浓度为 ,此时CO的瞬时生成速率
,此时CO的瞬时生成速率
 。
。④该反应的反应速率(v)随时间(t)的变化关系如图所示,若
 、
、 时刻只改变一个条件,下列说法错误的是
时刻只改变一个条件,下列说法错误的是
a.在
 时,采取的措施可以是升高温度
时,采取的措施可以是升高温度b.在
 时,采取的措施可以是增大
时,采取的措施可以是增大 的浓度
的浓度c.在
 时,容器内
时,容器内 的转化率是整个过程中的最大值
的转化率是整个过程中的最大值
您最近一年使用:0次
名校
2 . 下列实验方案或装置能达到目的的是
| 目的 | 实验方案或装置 | |
| A | 定量测量化学反应速率 |
|
| B | 测定酸碱中和热 |
|
| C | 探究浓度对化学平衡移动的影响 | 向两支盛有 溶液的试管中分别滴入3滴浓硫酸和3滴浓 溶液的试管中分别滴入3滴浓硫酸和3滴浓 ,观察溶液颜色的变化 ,观察溶液颜色的变化 |
| D | 探究浓度对反应速率的影响 | 分别向两支盛有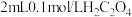 溶液的试管中分别加入 溶液的试管中分别加入 和 和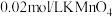 溶液,比较溶液褪色快慢 溶液,比较溶液褪色快慢 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 相同条件下,分别向20mL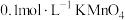 溶液和20mL 溶液和20mL 溶液中滴加相同浓度和体积的草酸溶液(过量)。 溶液中滴加相同浓度和体积的草酸溶液(过量)。 溶液紫色褪去的时间更短(生成的 溶液紫色褪去的时间更短(生成的 对该反应无影响) 对该反应无影响) | 浓度对反应速率的影响:浓度越大,反应速率越快 |
| B | 用乙酸浸泡水壶中的水垢,可将其清除 | 碳酸的酸性强于乙酸的酸性 |
| C | 室温下,测定浓度均为0.1molL-1的CH3COONa与HCOONa溶液的pH,CH3COONa溶液的pH大 | 结合H+的能力: |
| D | 取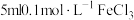 溶液,向其中滴加 溶液,向其中滴加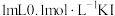 溶液,取上层清液滴加KSCN溶液,溶液变成红色。 溶液,取上层清液滴加KSCN溶液,溶液变成红色。 | 该反应是可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 化学是一门以实验为基础的自然科学,根据已有实验知识回答下列问题:

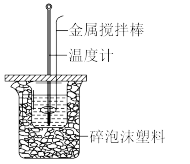
Ⅰ.右图是某实验小组改进的中和反应反应热测定实验装置。组装仪器后,先在塑料瓶中加入50mL 盐酸,然后通过注射器注入50mL
盐酸,然后通过注射器注入50mL NaOH溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
NaOH溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
(1)塑料瓶外泡沫板的作用是_____ ,缺少的仪器是_____ 。
(2)假设盐酸和氢氧化钠溶液的密度都是 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容 ,为了计算中和热,某学生记录实验数据如下:
,为了计算中和热,某学生记录实验数据如下:
依该学生的实验数据计算,该实验测得的中和热
_____ (结果保留一位小数)。
(数据处理时取盐酸和氢氧化钠溶液的平均值记为反应前体系起始温度)
Ⅱ.实验室经常用量气法测量化学反应的速率。

(3)图2与图1相比的优点是_____ 。
(4)也可以将图1中的注射器改为连通器如图3,为了准确地测量H2的体积,在读取反应后甲管中液面的读数时,应注意_____ (填写序号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管液面不再上升时读数
c.读数时应上、下移动乙管,使甲、乙两管液面相平
d.反应结束立即读数
(5)若想用图3测定二氧化碳的体积,结合平衡移动理论,为了减小误差,乙管中应盛放_____ (填试剂名称,已知: ,
, )。
)。

Ⅰ.右图是某实验小组改进的中和反应反应热测定实验装置。组装仪器后,先在塑料瓶中加入50mL
 盐酸,然后通过注射器注入50mL
盐酸,然后通过注射器注入50mL NaOH溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
NaOH溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:(1)塑料瓶外泡沫板的作用是
(2)假设盐酸和氢氧化钠溶液的密度都是
 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容 ,为了计算中和热,某学生记录实验数据如下:
,为了计算中和热,某学生记录实验数据如下:依该学生的实验数据计算,该实验测得的中和热

| 实验序号 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.2 | 23.4 |
| 2 | 20.2 | 20.4 | 23.8 |
| 3 | 20.3 | 20.5 | 25.6 |
Ⅱ.实验室经常用量气法测量化学反应的速率。

(3)图2与图1相比的优点是
(4)也可以将图1中的注射器改为连通器如图3,为了准确地测量H2的体积,在读取反应后甲管中液面的读数时,应注意
a.视线与凹液面最低处相平
b.等待片刻,待乙管液面不再上升时读数
c.读数时应上、下移动乙管,使甲、乙两管液面相平
d.反应结束立即读数
(5)若想用图3测定二氧化碳的体积,结合平衡移动理论,为了减小误差,乙管中应盛放
 ,
, )。
)。
您最近一年使用:0次
2023-08-20更新
|
384次组卷
|
4卷引用:黑龙江省大庆市大庆中学2023-2024学年高二上学期10月月考化学试题
名校
5 . 下列装置或操作不能达到目的的是


A.实验1 制取无水 固体 固体 |
| B.实验2 验证氯化银溶解度大于硫化银 |
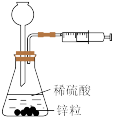
| C.实验3 测定锌与稀硫酸反应的速率 |
| D.实验4 验证温度对化学平衡的影响 |
您最近一年使用:0次
2022-12-29更新
|
627次组卷
|
5卷引用:黑龙江省哈尔滨市德强学校2022-2023学年高二上学期期末考试化学试题
名校
解题方法
6 . 为比较Fe3+和Cu2+对H2O2分解反应的催化效果,两位同学分别设计了如图甲、乙所示的实验。下列叙述不正确的是
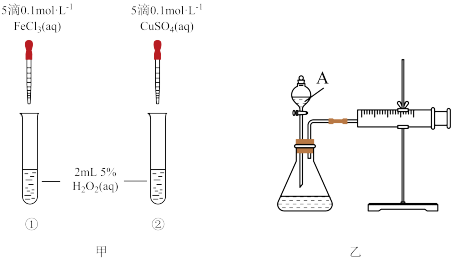

| A.图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小 |
| B.若图甲中所示实验反应速率为①>②,则说明Fe3+一定比Cu2+对H2O2分解的催化效果好 |
| C.用图乙所示装置测定反应速率,可测定产生的一定体积气体所需要的时间 |
| D.为检查图乙所示装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 |
您最近一年使用:0次
2022-11-02更新
|
128次组卷
|
85卷引用:2016届黑龙江省大庆实验中学高三上学期12月月考化学试卷
2016届黑龙江省大庆实验中学高三上学期12月月考化学试卷黑龙江省大庆中学2018-2019学年高一下学期期末考试化学试题黑龙江省齐齐哈尔市第八中学2020-2021学年高二上学期期中考试化学试题黑龙江省哈尔滨市第六中学2020-2021学年高二10月月考化学试题黑龙江省大庆中学2020-2021学年高二上学期期中考试化学试题黑龙江省佳木斯市第十二中学(佳木斯市建三江第一中学)2021-2022学年高一下学期期中考试化学试题(已下线)2010年江苏省启东中学高二上学期期中考试化学卷(已下线)2010-2011学年江苏省启东中学高二上学期期中考试化学试题(理)2015-2016学年辽宁鞍山一中高一下期中化学试卷2015-2016学年浙江宁波效实中学高二下期中化学试卷2015-2016学年河北武邑中学高一下5.15周考化学试卷2015-2016学年湖南省娄底市双峰县高一下期中化学试卷2016-2017学年山东省烟台第二中学高二下学期开学考试化学试卷四川省南充高级中学2016-2017学年高一下学期期末考试化学试题甘肃省兰州第一中学2017-2018学年高二上学期第一次月考(9月)化学试题安徽省淮北市第一中学2017-2018学年高二上学期第四次月考(12月)化学试题四川省三台中学实验学校2017-2018学年高一下学期期末仿真模拟(二)化学试题安徽省定远重点中学2018-2019学年高二上学期第三次月考化学试题(已下线)2019年3月31日 《每日一题》 必修2 每周一测四川省棠湖中学2018-2019学年高一下学期期末考试化学试题安徽省滁州市定远县育才学校2019-2020学年高二上学期入学考试化学试题贵州省贵阳市第二中学高一下学期期末考试化学试题辽宁省六校协作体2019-2020学年高二上学期10月月考化学试题广东省广州市第16中学2019-2020学年高二上学期期中考试化学试题2020届高三化学二轮冲刺新题专练——气体制取流程的规范操作(提升练)2020届高三化学实验复习——气密性的检查【选择突破】四川省棠湖中学2019-2020学年高一下学期第二次月考化学试题第二章 化学反应与能量 第三节 化学反应的速率和限度安徽省阜阳市2019-2020学年高一下学期开学考化学试题吉林省辽源市田家炳高级中学2019-2020学年高一下学期期中考试化学试题安徽省定远县育才学校2019-2020学年高一6月月考化学试题(已下线)第15讲 化学反应速率-2021年高考化学一轮复习名师精讲练(已下线)2.1.2 影响化学反应速率的因素(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)(已下线)2.1.2 影响化学反应速率的因素(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)安徽省定远县育才学校2020-2021学年高二上学期开学考试化学试题鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第3节 化学反应的速率 课时2 影响化学反应速率的因素鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第3节 化学反应的速率高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第一节 化学反应速率 课时2 影响化学反应速率的因素山东省潍坊市临朐县实验中学2020-2021学年高二9月月考化学试题(已下线)易错11 影响化学反应速率的因素-备战2021年高考化学一轮复习易错题湖北省随州市曾都一中2020-2021学年高二上学期9月月考化学试题必修第二册RJ高效学习手册-第六章山西省长治市第二中学校2020-2021学年高二上学期第一次月考化学试题四川省成都新津为明学校2020-2021学年高二上学期期中测试化学试题安徽省桐城中学2020-2021学年高一上学期12月月考化学试题山西省吕梁市2020-2021学年高二上学期期末考试化学试题河北省张家口市宣化一中2020-2021学年高一下学期期初考试化学试题浙江省丽水市高中发展共同体2020-2021学年高二下学期期中联合测试化学试题福建省三明市三地三校2020-2021学年高一下学期期中联考化学试题2018年广东和广西高中学生化学竞赛试题选择性必修1 专题2 第一单元 课时2 影响化学反应速率的因素河北省任丘一中2021-2022学年高二上学期阶段考试(一)化学试题(已下线)专题21 化学反应速率(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练甘肃省庆阳市第六中学2021-2022学年高二上学期第一次月考化学(理)试题山西省长治市第二中学校2021-2022学年高二上学期第一次月考化学试题陕西省西安市长安区第一中学2017-2018学年高二上学期第四次教学质量检测化学试题北京市石景山区第九中学2021-2022学年高二上学期期中考试化学试题(已下线)专题13 装置气密性的检查方法-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)湖北省武汉市部分普通高中联合体2021-2022学年高一下学期期中联考化学试题河南省南阳市第一中学校2021-2022学年高一下学期第三次月考化学试题四川省泸州市泸县第四中学2021-2022学年高一下学期期中考试化学试题湖南省长沙市实验中学2021-2022学年高一下学期期中考试化学试题甘肃省天水市秦安县第一中学2021-2022学年高一下学期期中考试化学试题 吉林省长春市东北师范大学附属中学2021-2022学年高一下学期期中考试化学试题宁夏石嘴山市平罗中学2021-2022学年高一下学期期中考试化学试题广东省珠海市三校2021-2022学年高一下学期期中联考化学试题河南省实验中学2021-2022学年高一下学期期期中考试化学试题辽宁省营口市第二高级中学2021-2022学年高一6月月考化学试题宁夏永宁县永宁中学2021-2022学年高二上学期期中考试化学试题新疆乌鲁木齐市林肯外国语培训学校、第十二中学2021-2022学年高一下学期期中考试化学试题(已下线)2.3.3 化学反应速率综合分析-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)湖北省襄阳市第五中学2022-2023学年高二上学期9月化学试题福建省福州市第三中学2022-2023学年高一上学期10月月考化学试题广东省化州市第一中学2020-2021学年高二上学期10月月考化学试题甘肃省礼县第一中学2020-2021学年高一上学期期中测试化学试题福建省南平市浦城第一中学2022-2023学年高一下学期期中考试化学试题福建省南平市浦城县2022-2023学年高一下学期期中考试化学试题浙江省温州市环大罗山联盟2022-2023学年高二上学期11月期中考试化学试题作业(十四) 外界条件对化学反应速率的影响四川省南充高级中学2021-2022学年高一下学期第二次月考化学试题浙江省温州十校联合体2023-2024学年高二上学期期中考试化学试题江苏省苏州市吴江市高级中学2023-2024学年高二上学期10月月考化学试题湖北省武汉市新洲区第一中学2024届高二上学期期末联考化学试题湖北省武汉市新洲区第一中学2024届高二上学期11月阶段测试化学试题新疆实验中学2023-2024学年高二上学期期中考试化学试题
名校
7 . I.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
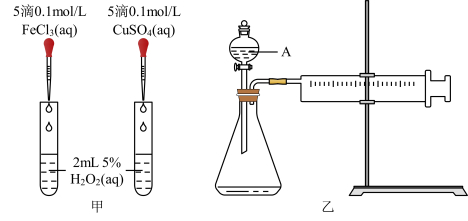
(1)定性分析:如图甲可通过观察_____ 的快慢,定性比较得出结论。有同学提出将FeCl3改为0.05mol•L-1Fe2(SO4)3更为合理,其理由是____ 。
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是____ 。
II.某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(3)该反应的化学方程式为_____ 。
(4)从开始至2min,A的平均反应速率为____ 。
(5)若平衡总压为P,则该温度下的KP=____ 。(保留两位有效数字)
KP类似于K,将平衡浓度换成气体分压,以分压表示,分压=总压×物质的量分数

(1)定性分析:如图甲可通过观察
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是
II.某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(3)该反应的化学方程式为
(4)从开始至2min,A的平均反应速率为
(5)若平衡总压为P,则该温度下的KP=
KP类似于K,将平衡浓度换成气体分压,以分压表示,分压=总压×物质的量分数
您最近一年使用:0次
名校
8 . 下列说法正确的是
A.可逆反应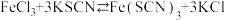 达到平衡后,加入 达到平衡后,加入 固体,逆反应速率加快 固体,逆反应速率加快 |
B.工业上合成 常选择500℃时进行而不是常温,是基于勒夏特列原理考虑的 常选择500℃时进行而不是常温,是基于勒夏特列原理考虑的 |
C.反应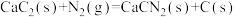 能自发进行,是因为 能自发进行,是因为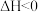 |
D.在装有2mL和1mL0.1mol/L 溶液的二支试管中,分别添加足量稀硫酸,观察浑浊产生的时间或产生气体的多少即可判断反应的快慢 溶液的二支试管中,分别添加足量稀硫酸,观察浑浊产生的时间或产生气体的多少即可判断反应的快慢 |
您最近一年使用:0次
名校
解题方法
9 . 下列实验装置能达到实验目的的是
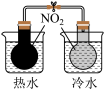 | 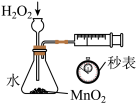 |  | 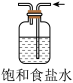 |
| A.验证温度对平衡移动的影响 | B.定量测定化学反应速率 | C.测定中和反应的反应热 | D.除去 中少量 中少量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验。下列叙述中不正确的是
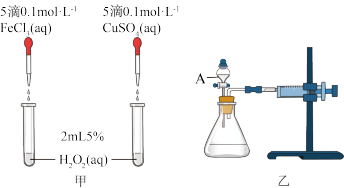

| A.图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小 |
| B.为排除阴离子对实验的干扰,可改为在甲中①试管中加入5滴0.1mol/L-1Fe2(SO4)3溶液 |
| C.用图乙所示装置测定反应速率,可测定相同时间内收集到的氧气的体积 |
| D.为检查图乙所示装置的气密性,可关闭A处活塞,将注射器活塞压缩一定距离,一段时间后松开活塞,观察活塞是否回到原位 |
您最近一年使用:0次
2022-10-07更新
|
475次组卷
|
8卷引用:黑龙江省哈尔滨市第九中学2022-2023学年高二上学期开学考试化学试题