名校
解题方法
1 . 如图表示某化学反应在使用催化剂(b曲线)和未使用催化剂(a曲线)时,反应进程和能量的对应关系。下列说法一定正确的是
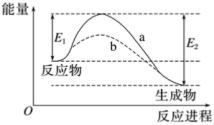

| A.a与b相比,b的活化能更高 |
| B.催化剂的使用,改变了反应的ΔH,因而能大大加快反应速率 |
| C.a与b相比,b中活化分子的百分数更高 |
| D.a与b相比,a的反应速率更快 |
您最近一年使用:0次
名校
2 . 如图表示某可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法正确的是
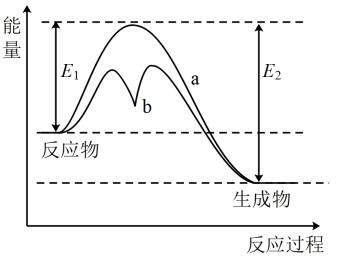

| A.反应为吸热反应 |
| B.a与b相比,a的反应速率更快 |
| C.a与b相比,反应的平衡常数一定不同 |
| D.反应物断键吸收的总能量小于生成物成键释放的总能量 |
您最近一年使用:0次
2022-02-18更新
|
211次组卷
|
2卷引用:广东省广州真光中学2021-2022学年高二上学期12月月考化学试题
3 . 如图表示某可逆反应在使用和未使用催化剂时,反应进程和能量的对应关系。下列说法一定正确的是


| A.a与b相比,b的活化能更高 |
| B.反应物断键吸收的总能量小于生成物成键释放的总能量 |
| C.a与b相比,a中的活化分子的百分比更高 |
| D.a与b相比,a对应的反应速率更快 |
您最近一年使用:0次
名校
解题方法
4 . 如图,这种具有不同能量的分子百分数和能量的对应关系图,叫做一定温度下分子能量分布曲线图。图中E表示分子平均能量,Ec是活化分子具有的最低能量。下列说法不正确的是
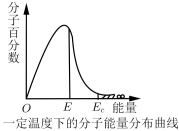

| A.图中Ec与E之差表示活化能 |
| B.升高温度,图中阴影部分面积会增大 |
| C.使用合适的催化剂,E不变,Ec变小 |
| D.能量大于Ec的分子间发生的碰撞一定是有效碰撞 |
您最近一年使用:0次
2020-03-05更新
|
258次组卷
|
3卷引用:江西省南昌三中2020届高三考前第二次适应性检测理综化学试题
名校
解题方法
5 . H2O2是一种常见试剂,在实验室、工业生产上有广泛用途。H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了如下图甲、乙两种实验装置。
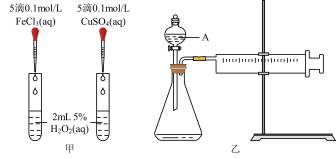
(1)若利用图甲装置,可通过观察___________ 现象,从而定性比较得出结论。
(2)有同学提出将0.1 FeCl3,改为
FeCl3,改为___________ 更为合理,其理由是___________ 。
(3)若利用乙实验可进行定量比较分析,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略,实验中还需要用到的实验仪器为___________ 。
(4)请简述如何用“微热法”检查装置乙的气密性良好:组装好实验装置,关闭分液漏斗活塞,___________ 。
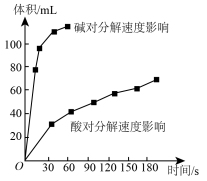
(5)如下图为某小组研究的酸、碱对H2O2分解的影响。该小组提出可以用BaO2固体与H2SO4溶液反应制H2O2,反应的化学方程式为___________ ,支持这一方案的理由是___________ 。
(6)使用催化剂Mn2+催化H2O2分解的反应中,Mn2+改变了___________ (填字母序号)
A.活化分子的浓度 B.反应限度 C.反应焓变
D.反应路径 E.反应活化能 F.活化分子百分数

(1)若利用图甲装置,可通过观察
(2)有同学提出将0.1
 FeCl3,改为
FeCl3,改为(3)若利用乙实验可进行定量比较分析,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略,实验中还需要用到的实验仪器为
(4)请简述如何用“微热法”检查装置乙的气密性良好:组装好实验装置,关闭分液漏斗活塞,
(5)如下图为某小组研究的酸、碱对H2O2分解的影响。该小组提出可以用BaO2固体与H2SO4溶液反应制H2O2,反应的化学方程式为

(6)使用催化剂Mn2+催化H2O2分解的反应中,Mn2+改变了
A.活化分子的浓度 B.反应限度 C.反应焓变
D.反应路径 E.反应活化能 F.活化分子百分数
您最近一年使用:0次
名校
解题方法
6 . 合成气(主要成分为CO、 及少量CO、
及少量CO、 )在工业上有广泛用途。
)在工业上有广泛用途。
(1)
 也称为水煤气变换反应(简称WGS),主要应用在制氢工业和合成氨工业。在金属催化剂Au(Ⅲ)表面上发生的所有基元反应步骤的活化能数值(单位:kJ/mol)如右表,其中*表示催化剂表面活性位,X*表示金属表面活性位吸附物种。其他条件一定时,决定WGS反应速率的基元反应为
也称为水煤气变换反应(简称WGS),主要应用在制氢工业和合成氨工业。在金属催化剂Au(Ⅲ)表面上发生的所有基元反应步骤的活化能数值(单位:kJ/mol)如右表,其中*表示催化剂表面活性位,X*表示金属表面活性位吸附物种。其他条件一定时,决定WGS反应速率的基元反应为_____ (填编号),基元反应 的焓变
的焓变
_____ kJ/mol。
由表中数据计算WGS反应的焓变
_____ kJ/mol。
(2)合成甲醇的主要反应为:
 。将CO与
。将CO与 混合气体充入密闭容器中,投料比
混合气体充入密闭容器中,投料比 ,测得平衡时混合气体中
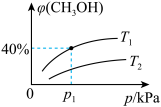
,测得平衡时混合气体中 的物质的量分数
的物质的量分数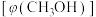 与温度(T)、压强(p)之间的关系如图所示。
与温度(T)、压强(p)之间的关系如图所示。
①图像中
_____  (填“>”、“<”或“=”,下同)。温度为
(填“>”、“<”或“=”,下同)。温度为 和
和 时对应的平衡常数分别为
时对应的平衡常数分别为 、
、 ,则
,则
_____  。
。
② 、
、 时,CO的转化率为
时,CO的转化率为_____ (保留3位有效数字)﹔压强平衡常数
_____ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,用含 的代数式表示)。
的代数式表示)。
③恒温恒容条件下,下列叙述不能说明反应达到化学平衡状态的是_____ 。
A.CO、 的物质的量浓度不再随时间的变化而变化
的物质的量浓度不再随时间的变化而变化
B.混合气体的平均摩尔质量不再随时间的变化而变化
C.混合气体的密度不再随时间的变化而变化
D.若将容器改为绝热恒容容器时,平衡常数K不随时间变化而变化
 及少量CO、
及少量CO、 )在工业上有广泛用途。
)在工业上有广泛用途。(1)

 也称为水煤气变换反应(简称WGS),主要应用在制氢工业和合成氨工业。在金属催化剂Au(Ⅲ)表面上发生的所有基元反应步骤的活化能数值(单位:kJ/mol)如右表,其中*表示催化剂表面活性位,X*表示金属表面活性位吸附物种。其他条件一定时,决定WGS反应速率的基元反应为
也称为水煤气变换反应(简称WGS),主要应用在制氢工业和合成氨工业。在金属催化剂Au(Ⅲ)表面上发生的所有基元反应步骤的活化能数值(单位:kJ/mol)如右表,其中*表示催化剂表面活性位,X*表示金属表面活性位吸附物种。其他条件一定时,决定WGS反应速率的基元反应为 的焓变
的焓变
由表中数据计算WGS反应的焓变

| 基元反应 | 正逆反应活化能 | ||
 | 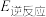 | ||
| ① |  | 0 | 67 |
| ② | 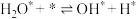 | 150 | 0 |
| ③ |  | 71 | 67 |
| ④ |  | 74 | 25 |
| ⑤ |  | 0 | 42 |
| ⑥ |  | 37 | 203 |
| ⑦ |  | 17 | 0 |
(2)合成甲醇的主要反应为:

 。将CO与
。将CO与 混合气体充入密闭容器中,投料比
混合气体充入密闭容器中,投料比 ,测得平衡时混合气体中
,测得平衡时混合气体中 的物质的量分数
的物质的量分数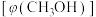 与温度(T)、压强(p)之间的关系如图所示。
与温度(T)、压强(p)之间的关系如图所示。
①图像中

 (填“>”、“<”或“=”,下同)。温度为
(填“>”、“<”或“=”,下同)。温度为 和
和 时对应的平衡常数分别为
时对应的平衡常数分别为 、
、 ,则
,则
 。
。②
 、
、 时,CO的转化率为
时,CO的转化率为
 的代数式表示)。
的代数式表示)。③恒温恒容条件下,下列叙述不能说明反应达到化学平衡状态的是
A.CO、
 的物质的量浓度不再随时间的变化而变化
的物质的量浓度不再随时间的变化而变化B.混合气体的平均摩尔质量不再随时间的变化而变化
C.混合气体的密度不再随时间的变化而变化
D.若将容器改为绝热恒容容器时,平衡常数K不随时间变化而变化
您最近一年使用:0次
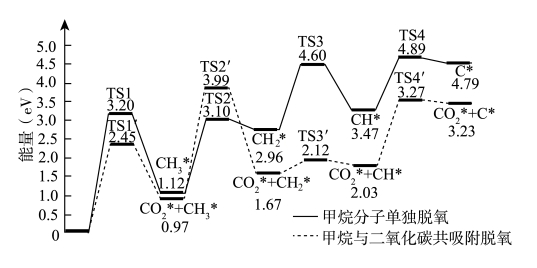
7 . 开发利用二氧化碳和甲烷资源,生产用途广泛、附加值高的烃类氧化物,对于环境保护,合成化学和资源利用均有重要意义。甲烷和二氧化碳可催化合成乙酸,其中一步为甲烷在催化剂表面脱氢,其方式有两种:甲烷分子单独脱氢,甲烷分子与二氧化碳共吸附脱氢,反应历程如下。下列说法正确的是

| A.电负性由大到小的顺序是O>C>H |
| B.单独脱氢的过程吸收能量,共吸附脱氢的过程释放能量 |
C.共吸附脱氢的决速步为由 转化为 转化为 的过程 的过程 |
| D.共吸附脱氢过程中,有极性键和非极性键的断裂 |
您最近一年使用:0次
名校
8 . 甲醛在木材加工、医药等方面有重要用途。甲醇利用脱氢法可制备甲醛,主要反应为: 。
。 是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:
是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:
历程ⅰ:
历程ⅱ:
历程ⅲ:
历程iv: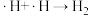
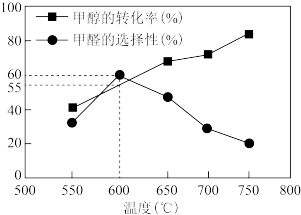
如图所示为在体积2L的恒容容器中,投入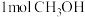 ,在碳酸钠催化剂作用下,经过5min反应,测得甲醇转化率与甲醛的选择性与温度的关系(甲醛的选择性:转化的
,在碳酸钠催化剂作用下,经过5min反应,测得甲醇转化率与甲醛的选择性与温度的关系(甲醛的选择性:转化的 中生成
中生成 的百分比),下列有关说法正确的是
的百分比),下列有关说法正确的是
 。
。 是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:
是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:历程ⅰ:

历程ⅱ:

历程ⅲ:

历程iv:
如图所示为在体积2L的恒容容器中,投入
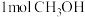 ,在碳酸钠催化剂作用下,经过5min反应,测得甲醇转化率与甲醛的选择性与温度的关系(甲醛的选择性:转化的
,在碳酸钠催化剂作用下,经过5min反应,测得甲醇转化率与甲醛的选择性与温度的关系(甲醛的选择性:转化的 中生成
中生成 的百分比),下列有关说法正确的是
的百分比),下列有关说法正确的是
A.600℃时,前5min内生成甲醛的平均速率 |
| B.700℃时,反应历程ⅱ的速率大于反应历程ⅲ的速率 |
| C.脱氢法制甲醛中,在高温高压条件下更有利于提高平衡产率 |
D.反应历程ⅰ的活化能小于 的活化能 的活化能 |
您最近一年使用:0次
2022-09-09更新
|
339次组卷
|
3卷引用:重庆市万州第二高级中学2022-2023学年高二上学期10月月考化学试题
重庆市万州第二高级中学2022-2023学年高二上学期10月月考化学试题江苏省包场高级中学2022-2023学年高三上学期暑期作业检测化学试题(已下线)2022年北京高考真题化学试题变式题(选择题11-14)
9 . 过二硫酸盐在工业上用途广泛,用作强氧化剂等。用过二硫酸盐(含Fe3+)去除溶液中I-的反应原理: (aq)+2I-(aq)=2
(aq)+2I-(aq)=2 (aq)+I2(aq)。该反应的分步机理如下,反应进程中的能量变化如图所示。
(aq)+I2(aq)。该反应的分步机理如下,反应进程中的能量变化如图所示。
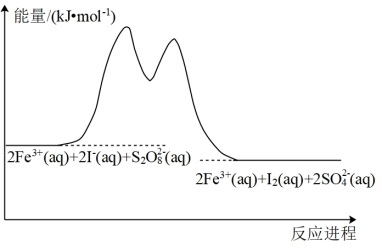
步骤①:2Fe3+(aq)+2I-(aq)=2Fe2+(aq)+I2(aq) Ea1
步骤②: (aq)+2Fe2+(aq)=2
(aq)+2Fe2+(aq)=2 (aq)+2Fe3+(aq) Ea2
(aq)+2Fe3+(aq) Ea2
下列关于该反应的说法错误的是
 (aq)+2I-(aq)=2
(aq)+2I-(aq)=2 (aq)+I2(aq)。该反应的分步机理如下,反应进程中的能量变化如图所示。
(aq)+I2(aq)。该反应的分步机理如下,反应进程中的能量变化如图所示。
步骤①:2Fe3+(aq)+2I-(aq)=2Fe2+(aq)+I2(aq) Ea1
步骤②:
 (aq)+2Fe2+(aq)=2
(aq)+2Fe2+(aq)=2 (aq)+2Fe3+(aq) Ea2
(aq)+2Fe3+(aq) Ea2下列关于该反应的说法错误的是
| A.相同条件下,活化能Ea1>Ea2,所以②比①反应速率慢,是决速步骤 |
| B.图中△H<0,其大小与Ea1、Ea2无关 |
| C.步骤①为吸热反应、步骤②为放热反应 |
| D.Fe3+是该反应的催化剂 |
您最近一年使用:0次
2022-03-17更新
|
179次组卷
|
2卷引用:湖南省长沙市第一中学2021-2022学年高三上学期第五次月考化学试题
名校
10 . 过二硫酸盐在工业上用途广泛,用作强氧化剂等。用过二硫酸盐(含 )去除溶液中
)去除溶液中 的反应原理:
的反应原理:
 。该反应的分步机理和能量变化如下:
。该反应的分步机理和能量变化如下:
步骤①: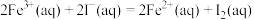
步骤②:
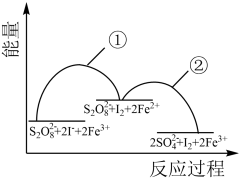
下列说法错误的是
 )去除溶液中
)去除溶液中 的反应原理:
的反应原理:
 。该反应的分步机理和能量变化如下:
。该反应的分步机理和能量变化如下:步骤①:
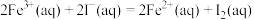
步骤②:


下列说法错误的是
| A.步骤①为吸热反应,步骤②为放热反应 |
| B.步骤①的反应速率大于步骤② |
C.总反应的 ,其大小与步骤①②的活化能无关 ,其大小与步骤①②的活化能无关 |
D. 是该反应的催化剂 是该反应的催化剂 |
您最近一年使用:0次
2022-05-05更新
|
153次组卷
|
2卷引用:海南省琼海市嘉积中学2021-2022学年高一下学期第二次月考化学试题



