名校
1 . 如图所示为氟利昂 破坏臭氧层的过程,下列说法
破坏臭氧层的过程,下列说法不正确 的是
 破坏臭氧层的过程,下列说法
破坏臭氧层的过程,下列说法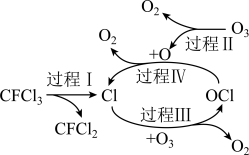
| A.过程Ⅳ中既有极性共价键的断裂又有非极性共价键的形成 |
B.整个过程可用方程式表示为 |
C. 的电子式为 的电子式为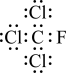 |
| D.上述过程说明氟利昂产生的氯原子是破坏臭氧层的催化剂 |
您最近一年使用:0次
2023-07-29更新
|
301次组卷
|
4卷引用:湖南省郴州市2023-2024学年高一上学期期末教学质量监测化学试卷
2 . 某温度时,在0.5 L密闭容器中,某一反应中A、B气体的物质的量随时间变化的曲线如图所示,回答下列问题:_______ 。
(2)第4 min时,正、逆反应速率的大小关系为:v(正)_______ v(逆),(填“>”“<”或“=”)。
(3)下列措施能加快反应速率的是_______。
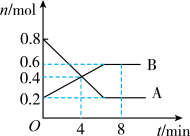
(2)第4 min时,正、逆反应速率的大小关系为:v(正)
(3)下列措施能加快反应速率的是_______。
| A.恒温恒容充入He气 | B.缩小体积,使压强增大 |
| C.恒温恒压充入He气 | D.使用催化剂 |
您最近一年使用:0次
3 . 硫及其化合物之间的转化在生产中有着重要作用。接触法制硫酸中, 制取
制取 的反应为
的反应为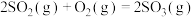
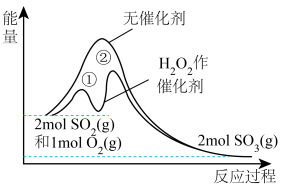
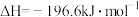 。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
 制取
制取 的反应为
的反应为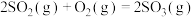
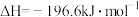 。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
| A.该反应中存在极性共价键和非极性共价键的断裂 |
B.使用 作催化剂只降低了正反应的活化能 作催化剂只降低了正反应的活化能 |
C.达到化学平衡时, 、 、 、 、 的物质的量之比为 的物质的量之比为 |
D.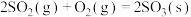 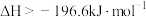 |
您最近一年使用:0次
名校
4 . 已知H2O2(aq)分解为H2O(l)和O2(g)的能量变化如图曲线A所示,若在H2O2溶液中加入少量KI,则H2O2的分解过程可表示为:①H2O2+I-=H2O+IO-,②H2O2+IO-=H2O+O2+I-,其能量变化如图曲线B所示。下列有关说法不正确 的是
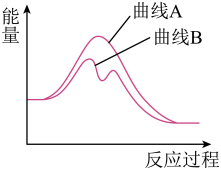

| A.上述反应①为吸热反应,反应②为放热反应 |
| B.2molH2O2(aq)具有的能量大于2molH2O(l)和1molO2(g)具有的总能量 |
| C.I-在H2O2分解过程中起到催化剂作用 |
| D.催化剂不参与化学反应,反应前后性质、质量不变 |
您最近一年使用:0次
2023-05-05更新
|
362次组卷
|
4卷引用:湖南省长沙市长沙县、望城区、浏阳市2022-2023学年高一下学期期末考试化学试题
5 . TiO2可以催化分解CO2实现碳元素的循环利用,其催化反应机理如图。下列说法错误的是
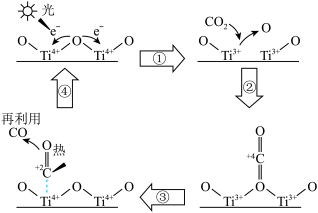

| A.过程①中TiO2发生了还原反应 |
| B.使用TiO2催化剂可以大大降低CO2分解的反应热 |
| C.该反应消耗了光能和热能 |
| D.该反应过程产生的O原子可能结合成O2 |
您最近一年使用:0次
名校
6 . 下列图示与对应的叙述正确的是
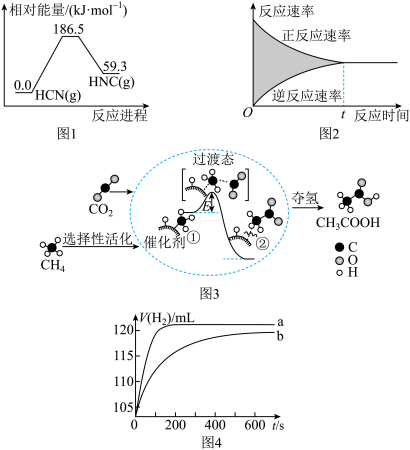

| A.图1所示曲线表示HCN(g)转化为HNC(g)需要吸收59.3kJ的能量 |
| B.图2所示的阴影部分面积可表示正反应速率的改变值 |
| C.图3所示曲线中状态①的物质比状态②的物质稳定 |
| D.图4是其他条件相同时,镁条与不同浓度盐酸反应曲线,其中曲线a表示的盐酸浓度比曲线b大 |
您最近一年使用:0次
2023-04-13更新
|
315次组卷
|
4卷引用:湖南省郴州市2022-2023学年高一下学期期末考试(选择考)化学试题
名校
7 . 如图所示为工业合成氨的流程图。下列有关说法不正确的是
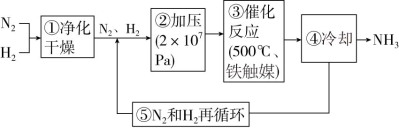

| A.步骤①中“净化”的目的是防止催化剂中毒 |
| B.步骤②中“加压”既可提高原料的转化率,又可加快反应速率 |
| C.步骤③中“500℃、铁触媒”有利于提高原料的平衡转化率 |
| D.步骤④中“冷却”的目的是将氨液化分离出来,提高原料的转化率 |
您最近一年使用:0次
2023-02-19更新
|
178次组卷
|
3卷引用:湖南省永州市2022-2023学年高二上学期期末考试化学试题
湖南省永州市2022-2023学年高二上学期期末考试化学试题(已下线)第08讲 化学反应的调控-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)河南省宜阳县第一高级中学2023-2024学年高二上学期9月开学考试化学试题
8 . 理论研究表明,在101 和298K下,
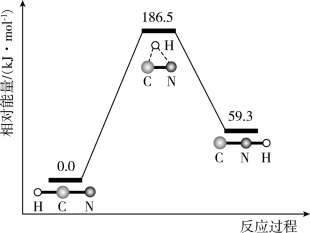
和298K下, 异构化反应过程的能量变化如图所示。下列说法错误的是
异构化反应过程的能量变化如图所示。下列说法错误的是
 和298K下,
和298K下, 异构化反应过程的能量变化如图所示。下列说法错误的是
异构化反应过程的能量变化如图所示。下列说法错误的是
A. 比 比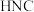 稳定 稳定 | B.使用催化剂,可以改变反应的反应热 |
| C.正反应的活化能大于逆反应的活化能 | D.该异构化反应的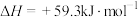 |
您最近一年使用:0次
2023-02-15更新
|
110次组卷
|
2卷引用:湖南省邵阳市新邵县第八中学2022-2023学年高二上学期期末质量检测化学试题
9 . 工业合成氨反应包含多个基元反应,其反应机理如图所示。下列说法错误的是
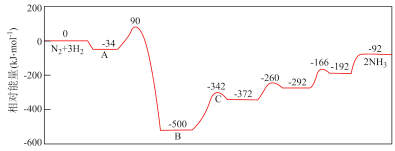

| A.从充入反应物到A处,表示N2、H2在催化剂表面吸附放热 |
| B.该历程中最大活化能E正=590kJ•mol-1 |
| C.工业合成氨温度为700K左右,主要考虑催化剂在此温度下活性较高 |
| D.催化剂可以降低活化能,从而显著提高反应速率 |
您最近一年使用:0次
2023-02-14更新
|
149次组卷
|
2卷引用:湖南省娄底市涟源市2023-2024学年高二上学期1月期末考试化学试题
解题方法
10 . 某化学兴趣小组为了探究催化剂对H2O2分解速率的影响,进行了一系列实验,请回答相关问题。
(1)将0.10molMnO2粉末加入到40mLH2O2溶液中,在标准状况下放出气体的体积和时间的关系如右图所示。
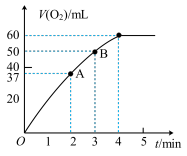
①该实验放出气体的总体积是_______ mL。
②A、B两点反应速率较慢的为_______ 点,理由是_______ 。
③H2O2的初始物质的量浓度是_______ (保留两位有效数字)。
(2)已知:Fe3+和Cu2+也能作为H2O2分解的催化剂,为了比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如下图甲、乙所示的实验。
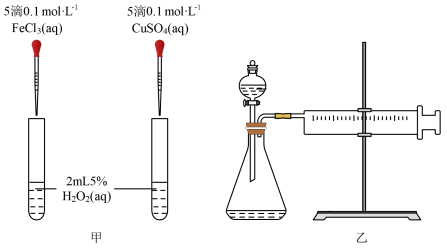
①定性分析:如图甲可通过观察_______ ,定性比较得出结论。小红认为此方案还需要进一步控制变量,提出可将试剂CuSO4更换为_______ (填化学式)。
②定量分析:如图乙所示,实验时均以生成40mL气体为标准,其它可能影响实验的因素均忽略。实验中需要测量的数据是_______ 。
(1)将0.10molMnO2粉末加入到40mLH2O2溶液中,在标准状况下放出气体的体积和时间的关系如右图所示。

①该实验放出气体的总体积是
②A、B两点反应速率较慢的为
③H2O2的初始物质的量浓度是
(2)已知:Fe3+和Cu2+也能作为H2O2分解的催化剂,为了比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如下图甲、乙所示的实验。

①定性分析:如图甲可通过观察
②定量分析:如图乙所示,实验时均以生成40mL气体为标准,其它可能影响实验的因素均忽略。实验中需要测量的数据是
您最近一年使用:0次



