1 . 下列说法错误的是( )
| A.升高温度可加快H2O2的分解速率 |
| B.减小H2O2溶液浓度可降低其分解速率 |
| C.加FeCl3不能加快H2O2分解速率 |
| D.用带火星的木条可检验H2O2分解产生的气体 |
您最近一年使用:0次
名校
解题方法
2 . 一种双功能结构催化剂能同时活化水和甲醇,用以解决氢气的高效存储和安全运输。下图是甲醇脱氢转化的反应历程( 表示过渡态)
表示过渡态)

下列说法正确的是
 表示过渡态)
表示过渡态)
下列说法正确的是
A. 的脱氢反应是分步进行的 的脱氢反应是分步进行的 |
B.甲醇脱氢反应历程的最大能垒(活化能)是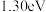 |
| C.甲醇脱氢反应中断裂了极性键和非极性键 |
| D.该催化剂的研发为醇类重整产氢的工业应用提供了新思路 |
您最近一年使用:0次
2020-08-07更新
|
246次组卷
|
3卷引用:湖南师范大学附属中学2019-2020学年高二下学期期末考试化学试题
3 . CO2是一种重要的化学资源,基于Sabatier反应,中科院设计完成了在催化剂作用下CO2氧化 制取具有工业使用价值的
制取具有工业使用价值的 气体。回答下列问题:
气体。回答下列问题:
(1)已知:
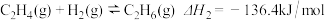
则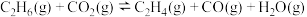

_____  。
。
(2)CO2氧化 制
制 的过程中,还存在反应:
的过程中,还存在反应: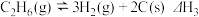 。
。
①随着反应进行,催化剂的活性明显降低,原因是_________________ ;
②若适当通入过量的CO2,则会明显减缓催化剂活性降低现象,原因是________________ 。
(3)CO2氧化 制
制 过程中,不同催化剂对反应物的转化率有不同影响,研究发现使用钴盐、铬盐作催化剂,未达到平衡时,其催化效果有如下结论:
过程中,不同催化剂对反应物的转化率有不同影响,研究发现使用钴盐、铬盐作催化剂,未达到平衡时,其催化效果有如下结论:
说明: 选择性是指转化的乙烷中生成乙烯的百分比;
选择性是指转化的乙烷中生成乙烯的百分比; 选择性是指转化的
选择性是指转化的 中生成
中生成 的百分比。该反应宜选取的催化剂为
的百分比。该反应宜选取的催化剂为______ ,理由是________________ 。
(4) 、
、 的某刚性容器中充入
的某刚性容器中充入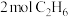 、
、 混合气体,压强为p,若仅发生如下反应:
混合气体,压强为p,若仅发生如下反应: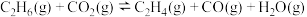 ,达到平衡时,
,达到平衡时, 的体积分数为0.2。
的体积分数为0.2。
①测得正反应速率为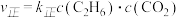 ,逆反应速率为
,逆反应速率为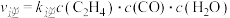 ,其中
,其中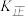 、
、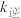 为速率常数,则
为速率常数,则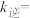
______ (以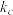 和
和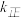 表示),
表示),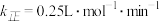 ,则平衡时
,则平衡时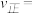
________ 。
②已知:气体分压=气体总压×体积分数,上述反应若应用平衡分压代替平衡浓度,所得的化学平衡常数
______ 。
 制取具有工业使用价值的
制取具有工业使用价值的 气体。回答下列问题:
气体。回答下列问题:(1)已知:

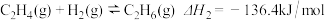
则
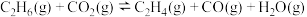

 。
。(2)CO2氧化
 制
制 的过程中,还存在反应:
的过程中,还存在反应: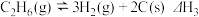 。
。①随着反应进行,催化剂的活性明显降低,原因是
②若适当通入过量的CO2,则会明显减缓催化剂活性降低现象,原因是
(3)CO2氧化
 制
制 过程中,不同催化剂对反应物的转化率有不同影响,研究发现使用钴盐、铬盐作催化剂,未达到平衡时,其催化效果有如下结论:
过程中,不同催化剂对反应物的转化率有不同影响,研究发现使用钴盐、铬盐作催化剂,未达到平衡时,其催化效果有如下结论:| 实验编号 |  | 催化剂 | 转化率/% | 选择性/% | ||
 | CO2 |  |  | |||
| Ⅰ | 650 | 钴盐 | 19.0 | 37.6 | 17.6 | 78.1 |
| Ⅱ | 650 | 铬盐 | 32.1 | 23.0 | 77.3 | 10.4 |
说明:
 选择性是指转化的乙烷中生成乙烯的百分比;
选择性是指转化的乙烷中生成乙烯的百分比; 选择性是指转化的
选择性是指转化的 中生成
中生成 的百分比。该反应宜选取的催化剂为
的百分比。该反应宜选取的催化剂为(4)
 、
、 的某刚性容器中充入
的某刚性容器中充入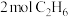 、
、 混合气体,压强为p,若仅发生如下反应:
混合气体,压强为p,若仅发生如下反应: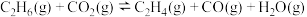 ,达到平衡时,
,达到平衡时, 的体积分数为0.2。
的体积分数为0.2。①测得正反应速率为
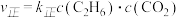 ,逆反应速率为
,逆反应速率为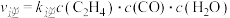 ,其中
,其中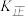 、
、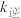 为速率常数,则
为速率常数,则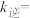
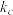 和
和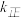 表示),
表示),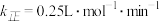 ,则平衡时
,则平衡时
②已知:气体分压=气体总压×体积分数,上述反应若应用平衡分压代替平衡浓度,所得的化学平衡常数

您最近一年使用:0次
4 . 氮气是一种重要的化工原料,工业上常用氮气合成氨、制硝酸。合成氨、制取硝酸的转化过程如图所示。下列说法正确的是
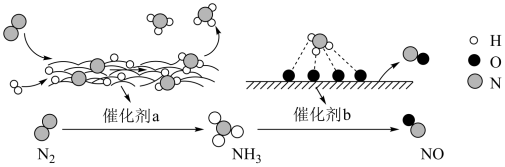

| A.图示中N元素在转化过程中均被氧化 |
| B.催化剂a可加快合成氨的反应速率并提高平衡转化率 |
| C.不使用催化剂,上述转化不能发生 |
| D.催化剂a与催化剂b表面均有极性键形成 |
您最近一年使用:0次
名校
5 . 氮及其化合物的转化过程如图所示。下列分析合理的是( )
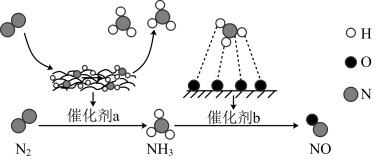

| A.N2 与 H2 反应生成NH3的原子利用率为 100% |
| B.催化剂a 表面发生了极性共价键的断裂和形成 |
| C.在催化剂 b 表面形成氮氧键时,不涉及电子转移 |
| D.催化剂 a、b 不仅能改变反应速率,还能提高反应的平衡转化率 |
您最近一年使用:0次
解题方法
6 . 某些化学问题可用相似的示意图来表示。下列说法不正确的是
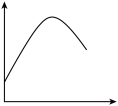


| 选项 | 横坐标 | 纵坐标 | 研究对象 |
| A | 反应时间 | 溶液温度 | 足量镁条放在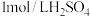 溶液中 溶液中 |
| B | 反应温度 | 反应速率 | 酶催化反应 |
| C | 盐酸体积 | 沉淀质量 | 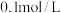 盐酸滴加到同浓度 盐酸滴加到同浓度 溶液中 溶液中 |
| D | 反应过程 | 能量 |  和 和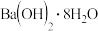 反应 反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
13-14高三上·北京海淀·期中
名校
7 . 下列图中的实验方案,能达到实验目的的是
| A | B | C | D | |
| 实验方案 | 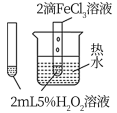 | 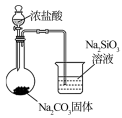 | 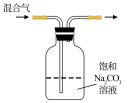 | 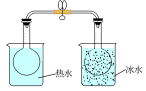 将NO2球浸泡在冰水和热水中 |
| 实验 目的 | 验证FeCl3对H2O2分解反应有催化作用 | 比较HCl、H2CO3和H2SiO3的酸性强弱 | 除去CO2气体中混有的SO2 | 探究温度对平衡 2NO2  N2O4的影响 N2O4的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-01-30更新
|
1048次组卷
|
17卷引用:2015-2016学年湖南省洞口县高二下学期期末化学试卷
2015-2016学年湖南省洞口县高二下学期期末化学试卷2015届湖南省岳阳市高三教学质量检测化学试卷2017届海南省农垦中学高三上学期期末化学试卷(已下线)2014届北京市海淀区高三上学期期中考试化学试卷(已下线)2014届山西省四校高三第二次联考化学试卷2015届云南省红河州高三统一检测理综化学试卷2015届甘肃省部分普高高三2月联考化学试卷2016届河南省洛阳市高三上学期12月统考化学试卷2016届福建省厦门一中高三下周考(三)理综化学试卷河北省邯郸市(大名县、永年区、磁县、邯山区)四县2016-2017学年高二下学期期中联考化学试题福建省三明市第一中学2016-2017学年高二下学期第二次月考化学试题山西省运城市2018届高三上学期期中考试化学试题内蒙古巴彦淖尔市第一中学2018届高三12月月考理科综合化学试题2019年高考化学一轮复习《化学实验方案的设计与评价》专题同步练习卷北京市第十二中学2019届高三第一学期期中考试化学试题河北省保定市唐县第一中学2021-2022学年高二10月月考化学试题福建省连城县第一中学2022-2023学年高二上学期第一次月考化学试题
名校
8 . 研究表明N2O与CO在Fe+作用下发生反应的能量变化及反应历程如图所示,下列说法错误的是
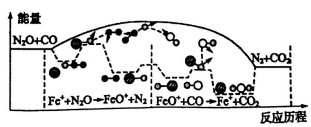

| A.反应总过程△H<0 |
| B.Fe+使反应的活化能减小 |
| C.总反应若在2L的密闭容器中进行,温度越高反应速率一定越快 |
| D.Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步反应均为放热及应 |
您最近一年使用:0次
2018-01-18更新
|
748次组卷
|
9卷引用:湖南省临澧县第一中学2020-2021学年高二上学期期末考试化学试题
湖南省临澧县第一中学2020-2021学年高二上学期期末考试化学试题辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校2018届高三上学期期末考试化学试题湖南省雅礼中学2020-2021学年高二上学期期中考试化学试题辽宁省实验中学东戴河分校2020届高三10月月考化学试题辽宁省大连海湾高级中学2019-2020学年高三上学期期中考试化学试题2020届高三化学二轮冲刺新题专练——能量变化的图像分析四川省新津中学2020-2021学年高二10月月考化学试题山东省济南市平阴一中2021届高三1月模拟化学试题江苏省灌南二中、南师大灌云附中2022-2023学年高二上学期第二次阶段性检测化学试题
9-10高一下·湖南·期末
名校
解题方法
9 . 某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生的化学反应方程式有_____________ 。
(2)硫酸铜溶液可以加快氢气生成速率的原因是__________ 。
(3)实验室中现有Na2SO4溶液、MgSO4溶液、Ag2SO4溶液、K2SO4溶液共4种溶液,其中可与上述实验中CuSO4溶液起相似作用的是_____ 。
(4) 要加快上述实验中气体产生的速率,还可采取的措施有
要加快上述实验中气体产生的速率,还可采取的措施有__________ (答两种)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
①请完成此实验设计,其中V1=________ ,V6=________ ,V9=________ 。
②该同学最后得出的结论为:当加入少量CuSO4溶液时,氢气的生成速率会大大提高,但当加入的CuSO4溶液超过一定量时,氢气的生成速率反而会下降。请分析氢气生成速率下降的主要原因______
(1)上述实验中发生的化学反应方程式有
(2)硫酸铜溶液可以加快氢气生成速率的原因是
(3)实验室中现有Na2SO4溶液、MgSO4溶液、Ag2SO4溶液、K2SO4溶液共4种溶液,其中可与上述实验中CuSO4溶液起相似作用的是
(4)
 要加快上述实验中气体产生的速率,还可采取的措施有
要加快上述实验中气体产生的速率,还可采取的措施有(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
| 项目 | A | B | C | D | E | F |
| 4 mol·L-1H2SO4溶液/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②该同学最后得出的结论为:当加入少量CuSO4溶液时,氢气的生成速率会大大提高,但当加入的CuSO4溶液超过一定量时,氢气的生成速率反而会下降。请分析氢气生成速率下降的主要原因
您最近一年使用:0次
2016-12-09更新
|
604次组卷
|
9卷引用:09—10湖南师大附中高一下学期期末(结业)考试化学卷
(已下线)09—10湖南师大附中高一下学期期末(结业)考试化学卷黑龙江省双鸭山市第一中学2016-2017学年高一下学期期末考试化学试题(已下线)2011-2012学年江西省九江一中高一下学期期中考试理科化学试卷(已下线)2012年人教版高中化学必修二2.3 化学反应的速率和限度练习卷2014—2015江西省九江市彭泽县第二高中高一下学期期中考试化学试卷山西省汾阳中学2016-2017学年高一下学期期中考试(理)化学试题贵州省思南中学2017-2018学年高二上学期第一次月考化学试题高二人教版选修4 第二章 第二节 影响化学反应速率的因素黑龙江省齐齐哈尔市第八中学2018-2019学年高一下学期期中考试化学试题



