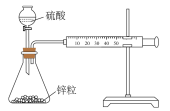
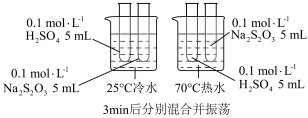
下列说法错误的是( )
| A.升高温度可加快H2O2的分解速率 |
| B.减小H2O2溶液浓度可降低其分解速率 |
| C.加FeCl3不能加快H2O2分解速率 |
| D.用带火星的木条可检验H2O2分解产生的气体 |
更新时间:2020-09-03 13:34:31
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关实验的现象和解释或结论都正确的是
| 实验操作 | 现象 | 解释或结论 | |
| A | 两支试管各盛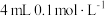 酸性高锰酸钾溶液,分别加入 酸性高锰酸钾溶液,分别加入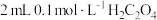 溶液和 溶液和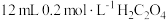 溶液 溶液 | 加入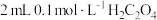 溶液的试管中,酸性高锰酸钾溶液褪色更快 溶液的试管中,酸性高锰酸钾溶液褪色更快 | 反应物浓度越大,反应速率越快 |
| B | 将稀硫酸酸化的 溶液滴入 溶液滴入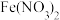 溶液中 溶液中 | 溶液变黄色 | 氧化性: 比 比 强 强 |
| C | 向盛有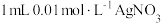 溶液的试管中滴加5滴 溶液的试管中滴加5滴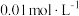 的 的 溶液,再滴加5滴 溶液,再滴加5滴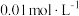 的 的 溶液 溶液 | 先有白色沉淀生成,后沉淀又转化为黄色沉淀 | 此温度下: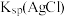 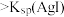 |
| D | 取 蔗糖溶液,加入3滴稀 蔗糖溶液,加入3滴稀 ,水浴加热 ,水浴加热 ,冷却后加入 ,冷却后加入 溶液调至碱性,再加入少量新制 溶液调至碱性,再加入少量新制 悬浊液,加热 悬浊液,加热 | 有砖红色沉淀产生 | 蔗糖发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关化学反应速率的实验探究方案设计合理的是
| 选项 | 实验方案 | 实验目的 |
| A | 向等体积等浓度的H2O2溶液中分别加入5滴 等浓度的CuSO4和FeCl3溶液,观察气体产生 的速度 | 比较Cu2+和Fe3+的催化效果 |
| B | 两支试管,都加入2mL1mol/L的酸性KMnO4溶 液,再同时向两支试管分别加入2mL0.1mol/L的 H2C2O4溶液和2mL0.05mol/L的H2C2O4溶液, 观察高锰酸钾溶液褪色所需时间 | 探究草酸浓度对反应速率影响 |
| C | 在锥形瓶内各盛有2g锌粒(颗粒大小基本相同), 然后通过分液漏斗分别加入40mL1mol/L和40mL 18mol/L的硫酸。比较两者收集10mL氢气所用的 时间
| 探究硫酸浓度对反应速率影响 |
| D |
| 探究温度对反应速率的影响 |
A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】某实验小组欲探究酸性KMnO4溶液和H2C2O4 (草酸)溶液反应过程中影响反应速率的因素,设计的实验方案和测得的实验数据如表所示(实验均在室温下进行):
已知实验①中酸性KMnO4 溶液褪色的速率开始十分缓慢,一段时间后突然加快。下列说法不正确的是
| 实验 序号 | ① | ② | ③ |
加入 试剂 | 4mL0.01 mol·L-1的酸性KMnO4溶液、2 mL 0.1mol·L-1 的H2C2O4溶液 | 4mL0.01 mol·L-1 的酸性KMnO4溶液、2 mL 0.1mol·L-1 的H2C2O4溶液、一粒黄豆粒大的MnSO4固体 | 4mL0.01 mol·L-1 的酸性KMnO4溶液、2 mL0.1 mol·L-1 的H2C2O4溶液、一粒黄豆粒大的K2SO4固体 |
| 褪色 时间/s | 116 | 6 |
A.草酸溶液与酸性高锰酸钾溶液反应的离子方程式为 2MnO +5 H2C2O4+6H+=2Mn2+ + 10CO2↑+8H2O +5 H2C2O4+6H+=2Mn2+ + 10CO2↑+8H2O |
| B.对比实验①、②可得出的结论是MnSO4为该反应的催化剂 |
| C.实验②中可用MnCl2固体替代MnSO4固体 |
| D.设计实验③可使结论更加严密,预测褪色时间约为116s |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O。某化学小组欲探究该反应过程中浓度、温度对化学反应速率的影响,进行如表实验(忽略溶液体积变化)。
下列说法错误的是
| 编号 | 0.01mol•L-1酸性KMnO4溶液体积/mL | 0.1mol•L-1H2C2O4溶液体积/mL | 水的体积/mL | 反应温度/℃ | 反应时间/min |
| I | 2 | 2 | 0 | 20 | 2.1 |
| II | 2 | V1 | 1 | 20 | 5.5 |
| III | 2 | V2 | 0 | 50 | 0.5 |
| A.V1=1,V2=2 |
| B.由实验I、II可知,增大H2C2O4浓度,反应速率减慢 |
| C.实验I、III的目的是探究温度对化学反应速率的影响 |
| D.若改用1mol•L-1酸性KMnO4溶液,将不能达到实验目的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】2SO2(g)+O2(g)  2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是
2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是

 2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是
2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是
| A.E1—E2=△H | B.该反应为吸热反应 |
| C.升高温度,不影响活化分子的百分数 | D.使用催化剂使该反应的反应热发生改变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】一定条件能发生反应:2N2Og) 2N2(g)+O2(g)。为探究不同条件对该反应的影响,在四个恒容密闭容器中按下表相应量充入气体,测得容器①、②、③、④中氧气的物质的量随时间的变化如图所示:
2N2(g)+O2(g)。为探究不同条件对该反应的影响,在四个恒容密闭容器中按下表相应量充入气体,测得容器①、②、③、④中氧气的物质的量随时间的变化如图所示:

下列说法正确的是
 2N2(g)+O2(g)。为探究不同条件对该反应的影响,在四个恒容密闭容器中按下表相应量充入气体,测得容器①、②、③、④中氧气的物质的量随时间的变化如图所示:
2N2(g)+O2(g)。为探究不同条件对该反应的影响,在四个恒容密闭容器中按下表相应量充入气体,测得容器①、②、③、④中氧气的物质的量随时间的变化如图所示:| 容器 | 温度/℃ | 容积/L | 起始物质的量/mol | ||
| N2O | N2 | O2 | |||
| ① | 450 | V① | 0.1 | 0 | 0 |
| ② | 450 | 1.0 | 0.1 | 0 | 0 |
| ③ | 400 | 0.8 | 0.1 | 0 | 0 |
| ④ | T④ | 1.0 | 0.2 | 0 | 0 |

下列说法正确的是
| A.相同温度下反应,t1时间内,该反应的平均反应速率v①=v③ |
| B.第②个容器中一定加入催化剂 |
| C.若T④>450℃,说明温度越高,反应速率越快 |
| D.若①②③④四个容器都未加催化剂,比较①③两个容器的数据,说明温度越高,反应速率越快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列关于N2+3 H2  2 NH3的反应说法
2 NH3的反应说法错误 的是
 2 NH3的反应说法
2 NH3的反应说法| A.升高温度能加快反应速率 |
| B.增大压强能加快反应速率 |
| C.使用恰当的催化剂能加快反应速率 |
| D.提高H2的浓度能将N2全部转化为NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】氮气是一种重要的化工原料,工业上常用氮气合成氨、制硝酸。合成氨、制取硝酸的转化过程如图所示。下列说法正确的是
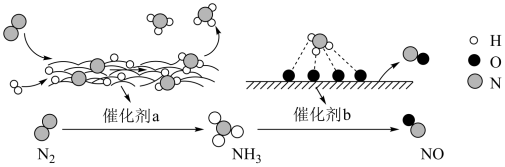

| A.图示中N元素在转化过程中均被氧化 |
| B.催化剂a可加快合成氨的反应速率并提高平衡转化率 |
| C.不使用催化剂,上述转化不能发生 |
| D.催化剂a与催化剂b表面均有极性键形成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究常温下, 和 和 的 的 大小关系 大小关系 | 将 相同的 相同的 溶液和 溶液和 溶液均稀释10倍 溶液均稀释10倍 | 若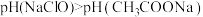 , ,则说明 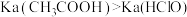 |
| B | 探究催化剂对 分解速率的影响 分解速率的影响 | 在相同条件下向一支试管中加入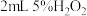 和 和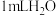 ,向另一支试管中加入 ,向另一支试管中加入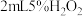 和 和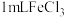 溶液 溶液 | 可观察到后者产生气泡速度更快,说明 可加快 可加快 分解速率 分解速率 |
| C | 测定常温下某 溶液的 溶液的 | 用胶头滴管将待测液滴在湿润的 试纸上,与标准比色卡对照 试纸上,与标准比色卡对照 | 测得 为13 为13 |
| D | 检验电解法制备的氯气 | 电解饱和食盐水,用湿润的碘化钾淀粉试纸检验阴极产生的气体 | 若试纸变蓝色,则说明有氯气产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次