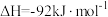理论研究表明,在101 和298K下,
和298K下, 异构化反应过程的能量变化如图所示。下列说法错误的是
异构化反应过程的能量变化如图所示。下列说法错误的是
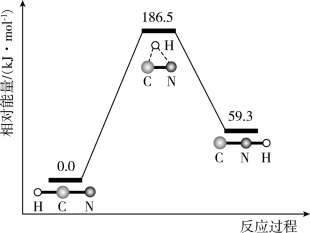
 和298K下,
和298K下, 异构化反应过程的能量变化如图所示。下列说法错误的是
异构化反应过程的能量变化如图所示。下列说法错误的是
A. 比 比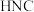 稳定 稳定 | B.使用催化剂,可以改变反应的反应热 |
| C.正反应的活化能大于逆反应的活化能 | D.该异构化反应的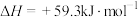 |
更新时间:2023-02-15 06:46:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】有关能量的判断或表示方法正确的是
| A.由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量等于57.3 kJ |
| B.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
| C.2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g) =2 H2O(l) △H=-285.8kJ/mol |
| D.从C(石墨)=C(金刚石)△H=+1.9kJ/mol,可知石墨比金刚石更稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是金属镁和卤素单质X2反应的能量变化示意图。下列说法正确的是
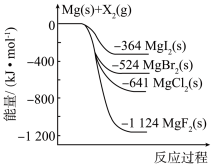
| A.由MgCl2制取Mg是放热过程 |
| B.热稳定性:MgI2>MgBr2>MgCl2>MgF2 |
| C.金属镁和卤素单质X2的反应都是放热反应 |
| D.由图可知,此温度下MgI2(s)所含化学键的键能最大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】反应2C(s)+O2(g)=2CO(g)的能量变化如下图所示。下列说法正确的是


| A.C(s)与一定量O2(g)反应生成14g CO(g)放出的热量为110.5kJ |
| B.该反应的热化学方程式:2C(s)+O2(g)=2CO(g) ΔH=-221kJ |
| C.该反应的反应热等于CO分子中化学键形成时所释放的总能量与O2分子中化学键断裂时所吸收的总能量的差 |
| D.2mol C(s)与足量O2(g)充分反应,生成CO2(g),放出的热量大于221kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】2SO2(g)+O2(g) 2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
 2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
2SO3(g) △H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是| A.基元反应发生的先决条件是反应物分子发生有效碰撞 |
| B.增大SO2的浓度可以显著提高总反应的速率 |
| C.V2O5的存在提高了该反应活化分子百分数,使有效碰撞次数增加,反应速率加快 |
| D.逆反应的活化能比正反应的活化能大198kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ•mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) △H=-192.9kJ•mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9kJ•mol-1
下列说法正确的是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ•mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) △H=-192.9kJ•mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9kJ•mol-1下列说法正确的是

A.根据②推知反应:CH3OH(l)+ O2(g)=CO2(g)+2H2(g) △H>-192.9kJ•mol-1 O2(g)=CO2(g)+2H2(g) △H>-192.9kJ•mol-1 |
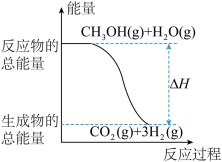
| B.反应①中的能量变化如图所示 |
| C.CH3OH的燃烧热为192.9kJ•mol-1 |
| D.CH3OH转变成H2的过程一定要吸收能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 标记的乙酸甲酯在足量
标记的乙酸甲酯在足量 溶液中发生水解,部分反应历程可表示为:
溶液中发生水解,部分反应历程可表示为: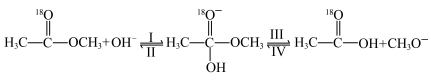 能量变化如图所示。已知
能量变化如图所示。已知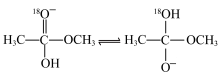 为快速平衡,下列说法正确的是
为快速平衡,下列说法正确的是
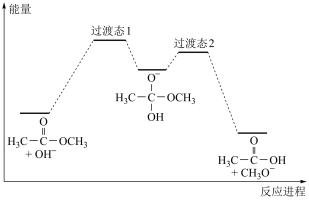
 标记的乙酸甲酯在足量
标记的乙酸甲酯在足量 溶液中发生水解,部分反应历程可表示为:
溶液中发生水解,部分反应历程可表示为: 能量变化如图所示。已知
能量变化如图所示。已知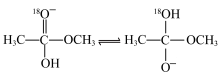 为快速平衡,下列说法正确的是
为快速平衡,下列说法正确的是
| A.反应Ⅱ、Ⅲ为决速步 |
| B.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓 |
C.反应结束后,溶液中存在 |
D.反应结束后,溶液中存在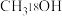 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对某一可逆反应来说,使用催化剂的作用是( )
| A.提高反应物的平衡转化率 | B.以同样程度改变正、逆反应速率 |
| C.增大反应的活化能 | D.改变平衡混合物的组成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
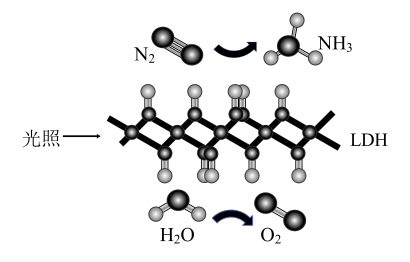
【推荐1】哈伯法合成氢的反应原理为 ,新研制的催化剂可使该反应在常温、常压下进行,以氮气和氢气为反应物的燃料电池是利用氮气的一种新方法。我国科学家研制的高效固体催化剂
,新研制的催化剂可使该反应在常温、常压下进行,以氮气和氢气为反应物的燃料电池是利用氮气的一种新方法。我国科学家研制的高效固体催化剂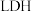 ,实现了在常温常压、可见光条件下“人工固氮”,其原理如图所示。下列有关说法不正确的是
,实现了在常温常压、可见光条件下“人工固氮”,其原理如图所示。下列有关说法不正确的是
 ,新研制的催化剂可使该反应在常温、常压下进行,以氮气和氢气为反应物的燃料电池是利用氮气的一种新方法。我国科学家研制的高效固体催化剂
,新研制的催化剂可使该反应在常温、常压下进行,以氮气和氢气为反应物的燃料电池是利用氮气的一种新方法。我国科学家研制的高效固体催化剂 ,实现了在常温常压、可见光条件下“人工固氮”,其原理如图所示。下列有关说法不正确的是
,实现了在常温常压、可见光条件下“人工固氮”,其原理如图所示。下列有关说法不正确的是
| A.反应过程中存在共价键的断裂与形成 |
| B.反应过程中存在太阳能转化为化学能 |
C.使用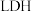 ,可降低反应的活化能 ,可降低反应的活化能 |
D.反应生成 时,电子转移了 时,电子转移了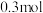 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】恒容高压氢气氛围中CO在铑基催化剂表面主要发生反应为2CO(g)+4H2(g) C2H5OH(g)+ H2O(g),该反应的速率方程为
C2H5OH(g)+ H2O(g),该反应的速率方程为 = k c2(CO),其中k为速率常数,下列说法中错误的是
= k c2(CO),其中k为速率常数,下列说法中错误的是
 C2H5OH(g)+ H2O(g),该反应的速率方程为
C2H5OH(g)+ H2O(g),该反应的速率方程为 = k c2(CO),其中k为速率常数,下列说法中错误的是
= k c2(CO),其中k为速率常数,下列说法中错误的是| A.充入CO的量越多,平衡体系中C2H5OH的浓度越大 |
| B.在该体系中继续充入H2可提高反应速率 |
| C.在该体系中加入适量生石灰可提高反应物的平衡转化率 |
| D.对铑基催化剂进行改良可能会进一步提高催化效率 |
您最近一年使用:0次



 的
的