1 . 利用“萨巴蒂尔反应”,空间站的水气整合系统将 转化为
转化为 和水蒸气,配合
和水蒸气,配合 生成系统可实现
生成系统可实现 的再生。回答下列问题:
的再生。回答下列问题:
Ⅰ.萨巴蒂尔反应为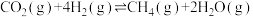

(1)已知25℃和101kPa时,
① 的燃烧热
的燃烧热 ;
;
② 的燃烧热
的燃烧热 ;
;
③
 。
。
则萨巴蒂尔反应的
_______  。
。
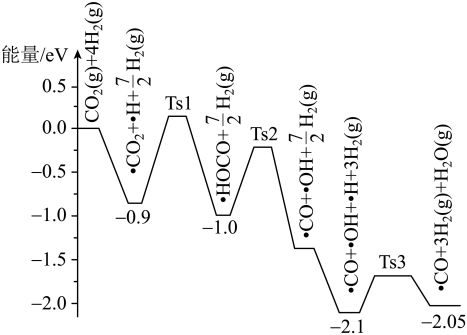
(2)萨巴蒂尔反应的前三步反应历程如图所示,其中吸附在催化剂 表面的物质用“·”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
表面的物质用“·”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会_______ (填“放出”或“吸收”)热量,反应历程中最小能垒(活化能)步骤的化学方程式为_______ 。
Ⅱ. 在一定条件下能与
在一定条件下能与 发生氧再生反应:
发生氧再生反应:

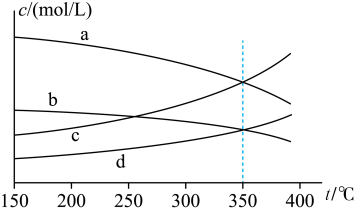
(3)恒压p0条件下,按 投料,进行氧再生反应,测得不同温度下平衡时体系中各物质浓度的关系如图所示。350℃时,该反应的平衡常数
投料,进行氧再生反应,测得不同温度下平衡时体系中各物质浓度的关系如图所示。350℃时,该反应的平衡常数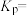
_______ (以分压表示,分压=总压×物质的量分数)。为了提高 的转化率,除升高温度外,还可采取的措施为
的转化率,除升高温度外,还可采取的措施为_______ (写出一条)。
(4)氧再生反应还可以通过酸性条件下半导体光催化转化实现,反应机理如图甲所示:
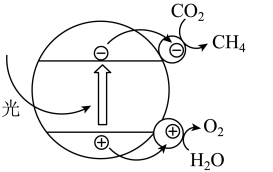
图甲
①光催化 转化为
转化为 时,阴极的电极反应式为
时,阴极的电极反应式为_______ 。
②催化剂的催化效率和 的生成速率随温度的变化关系如图乙所示。300~400℃之间,
的生成速率随温度的变化关系如图乙所示。300~400℃之间, 生成速率加快的原因是
生成速率加快的原因是_______ 。
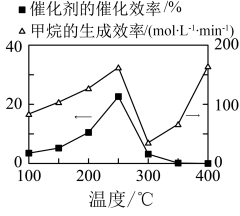
图乙
(5)氧再生反应所需的能量可由合成氨反应提供。合成氨反应的焓变和熵变:

 ,常温(298K)下,合成氨反应的自由能
,常温(298K)下,合成氨反应的自由能
_______  。
。
 转化为
转化为 和水蒸气,配合
和水蒸气,配合 生成系统可实现
生成系统可实现 的再生。回答下列问题:
的再生。回答下列问题:Ⅰ.萨巴蒂尔反应为
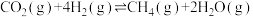

(1)已知25℃和101kPa时,
①
 的燃烧热
的燃烧热 ;
;②
 的燃烧热
的燃烧热 ;
;③

 。
。则萨巴蒂尔反应的

 。
。(2)萨巴蒂尔反应的前三步反应历程如图所示,其中吸附在催化剂
 表面的物质用“·”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
表面的物质用“·”标注,Ts表示过渡态。从物质吸附在催化剂表面到形成过渡态的过程会
Ⅱ.
 在一定条件下能与
在一定条件下能与 发生氧再生反应:
发生氧再生反应:

(3)恒压p0条件下,按
 投料,进行氧再生反应,测得不同温度下平衡时体系中各物质浓度的关系如图所示。350℃时,该反应的平衡常数
投料,进行氧再生反应,测得不同温度下平衡时体系中各物质浓度的关系如图所示。350℃时,该反应的平衡常数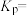
 的转化率,除升高温度外,还可采取的措施为
的转化率,除升高温度外,还可采取的措施为
(4)氧再生反应还可以通过酸性条件下半导体光催化转化实现,反应机理如图甲所示:

图甲
①光催化
 转化为
转化为 时,阴极的电极反应式为
时,阴极的电极反应式为②催化剂的催化效率和
 的生成速率随温度的变化关系如图乙所示。300~400℃之间,
的生成速率随温度的变化关系如图乙所示。300~400℃之间, 生成速率加快的原因是
生成速率加快的原因是
图乙
(5)氧再生反应所需的能量可由合成氨反应提供。合成氨反应的焓变和熵变:


 ,常温(298K)下,合成氨反应的自由能
,常温(298K)下,合成氨反应的自由能
 。
。
您最近一年使用:0次
名校
2 . “一锅法”用[Ru]催化硝基苯(PhNO2,Ph-表示苯基)与醇(RCH2OH)反应为仲胺(RCH2NHPh),反应过程如下图所示。下列叙述错误的是
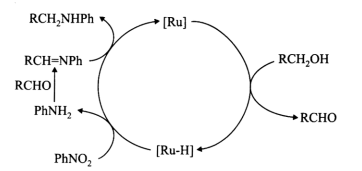

| A.反应原料中的RCH2OH 不能用RCH(CH3)OH代替 |
| B.历程中存在反应PhNH2+RCHO→RCH=NPh+H2O |
| C.有机物还原反应的氢都来自于RCH2OH |
| D.该反应过程结束后RCHO没有剩余 |
您最近一年使用:0次
2021-03-05更新
|
1640次组卷
|
9卷引用:河北省河北衡水中学2021届高三下学期第二次调研考试化学试题
河北省河北衡水中学2021届高三下学期第二次调研考试化学试题湖北省武汉市2021届高三下学期3月质量检测化学试题湖南省新高考联盟2021届高三下学期3月提升检测化学(A)试题(已下线)2021年高考化学押题预测卷(辽宁卷)(03)(已下线)押山东卷第13题 陌生反应机理选择题-备战2021年高考化学临考题号押题(山东卷)广东省汕头市金山中学2020-2021学年高二下学期期中考试化学试题湖南省岳阳县一中2022届高三年级入学考试化学试题(已下线)2022年新高考化学时事热点情境化考题---物质循环图山东省济宁邹城市2021-2022学年高二下学期期中考试化学试题
名校
3 . 一定温度下,向10 mL H2O2溶液中加入适量FeCl3溶液,反应分两步进行:
①2Fe3++ H2O2=2Fe2++ O2↑+ 2H+,② H2O2 + 2Fe2+ + 2H+ =2Fe3++2H2O,
反应过程中能量变化如下图所示。下列说法正确的是( )
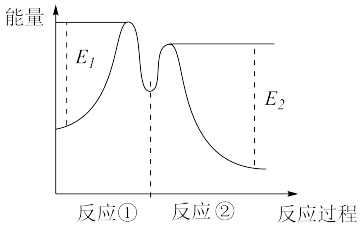
①2Fe3++ H2O2=2Fe2++ O2↑+ 2H+,② H2O2 + 2Fe2+ + 2H+ =2Fe3++2H2O,
反应过程中能量变化如下图所示。下列说法正确的是( )

| A.反应②的ΔH=(E2 -E1)kJ·mol-1 |
| B.Fe3+的作用是增大过氧化氢的分解速率 |
| C.反应2H2O2(aq)=2H2O(l)+O2(g)的△H<0 |
| D.反应①是放热反应、反应②是吸热反应 |
您最近一年使用:0次
2018-05-16更新
|
1085次组卷
|
3卷引用:河北深州市长江中学2021-2022学年高二上学期10月月考化学(理)试题
名校
4 . Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15 ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出大试管中发生反应的化学方程式:_________________ ,该反应是______ 反应(填放热[或吸热)。
(2)实验结果表明,催化剂的催化效果与___________________________ 有关。
Ⅱ.某可逆反应在某体积为5L的密闭容器中进行,在从0—3分钟各物质的量的变化情况如图所示(A,B,C均为气体)。

(3)该反应的的化学方程式为_____________________________________________ ;
(4)反应开始至2分钟时,B的平均反应速率为_____________________________ 。
(5)能说明该反应已达到平衡状态的是________________________ 。
a.v(A)= 2v(B)
b.容器内压强保持不变
c.2v逆(A)= v正(B)
d.容器内混合气体的密度保持不变
(6)在密闭容器里,通入a mol A (g)、b mol B (g)、c molC(g),发生上述反应,当改变下列条件时,反应速率会减小的是____ 。
A.降低温度 B.加入催化剂(正) C.增大容器体积
Ⅲ.为了减缓过量Zn与盐酸产生氢气的反应速率而又不减少产生氢气的量,在盐酸中分别加入下列物质:
A.H2O
B.NaCl溶液
C.Na2CO3溶液
D.Na2NO3溶液
E.CuSO4粉末
你认为可行的是(填编号)________________ 。
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5 min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30 min |
(2)实验结果表明,催化剂的催化效果与
Ⅱ.某可逆反应在某体积为5L的密闭容器中进行,在从0—3分钟各物质的量的变化情况如图所示(A,B,C均为气体)。

(3)该反应的的化学方程式为
(4)反应开始至2分钟时,B的平均反应速率为
(5)能说明该反应已达到平衡状态的是
a.v(A)= 2v(B)
b.容器内压强保持不变
c.2v逆(A)= v正(B)
d.容器内混合气体的密度保持不变
(6)在密闭容器里,通入a mol A (g)、b mol B (g)、c molC(g),发生上述反应,当改变下列条件时,反应速率会减小的是
A.降低温度 B.加入催化剂(正) C.增大容器体积
Ⅲ.为了减缓过量Zn与盐酸产生氢气的反应速率而又不减少产生氢气的量,在盐酸中分别加入下列物质:
A.H2O
B.NaCl溶液
C.Na2CO3溶液
D.Na2NO3溶液
E.CuSO4粉末
你认为可行的是(填编号)
您最近一年使用:0次
2017-09-16更新
|
334次组卷
|
2卷引用:河北省故城县高级中学2017-2018学年高二9月月考化学试题
名校
5 . 臭氧的脱硝反应为:2NO2(g) + O3(g) N2O5(g) + O2(g),一定条件下,向2.0L恒容密闭容器中充入2.0molNO2和1.0 molO3,一段时间后达到平衡。下图曲线a表示该反应在温度T下O3的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时O3的浓度随时间的变化。下列叙述正确的是( )
N2O5(g) + O2(g),一定条件下,向2.0L恒容密闭容器中充入2.0molNO2和1.0 molO3,一段时间后达到平衡。下图曲线a表示该反应在温度T下O3的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时O3的浓度随时间的变化。下列叙述正确的是( )
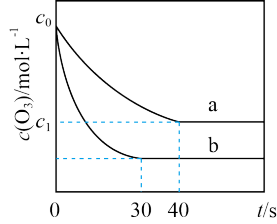
 N2O5(g) + O2(g),一定条件下,向2.0L恒容密闭容器中充入2.0molNO2和1.0 molO3,一段时间后达到平衡。下图曲线a表示该反应在温度T下O3的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时O3的浓度随时间的变化。下列叙述正确的是( )
N2O5(g) + O2(g),一定条件下,向2.0L恒容密闭容器中充入2.0molNO2和1.0 molO3,一段时间后达到平衡。下图曲线a表示该反应在温度T下O3的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时O3的浓度随时间的变化。下列叙述正确的是( )
A.反应2NO2(g) + O3(g) N2O5(g) + O2(g) △S<0 N2O5(g) + O2(g) △S<0 |
| B.曲线b对应的条件改变可能是加入了催化剂,平衡常数Ka=Kb |
| C.曲线b对应的条件改变可能是密闭容器的体积变为4.0L |
| D.若c1=0.3mol·L-1,从反应开始到平衡时该反应的速率v(NO2)=0.005 mol·L-1·s-1 |
您最近一年使用:0次
2016-12-09更新
|
290次组卷
|
4卷引用:【全国百强校】河北省武邑中学2018-2019学年高二下学期第一次月考化学试题
【全国百强校】河北省武邑中学2018-2019学年高二下学期第一次月考化学试题2016届江苏省苏北四市高三上学期期中质量抽测化学试卷江西省抚州市临川第二中学2022-2023学年高二上学期第一次月考化学试题(已下线)期中考试模拟试题(二)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)



