名校
解题方法
1 . 工业上利用黄铁矿(FeS2)制取硫酸,其反应流程如下:

| A.反应①矿石粉碎的目的是提高反应速率 |
| B.反应②中即使通入过量的氧气,也不能将SO2全部转化成SO3 |
| C.接触室选择500℃左右的温度是因为比常温更有利于合成SO3 |
| D.过量的氨水吸收SO2的化学方程式:2NH3·H2O+SO2=(NH4)2SO3+H2O |
您最近一年使用:0次
2024-03-20更新
|
82次组卷
|
2卷引用:宁夏石嘴山市第三中学2023-2024学年高一下学期4月期中考试化学试题
名校
2 .  和
和 可用于烟气中的大量氮氧化物
可用于烟气中的大量氮氧化物 转化为无害物质.将NO与
转化为无害物质.将NO与 的混合气体通入
的混合气体通入 和
和 的混合溶液中,发生以下转化过程.下列说法
的混合溶液中,发生以下转化过程.下列说法错误 的是
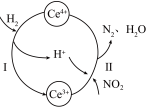
 和
和 可用于烟气中的大量氮氧化物
可用于烟气中的大量氮氧化物 转化为无害物质.将NO与
转化为无害物质.将NO与 的混合气体通入
的混合气体通入 和
和 的混合溶液中,发生以下转化过程.下列说法
的混合溶液中,发生以下转化过程.下列说法
A.反应前后溶液中 和 和 的总物质的量不变 的总物质的量不变 |
| B.参加反应Ⅰ的氧化剂与还原剂的个数之比为2∶1 |
C.反应Ⅱ的离子方程式为 |
D.反应过程中消耗 与生成 与生成 的体积(标况下)相等 的体积(标况下)相等 |
您最近一年使用:0次
名校
解题方法
3 . 我国是世界上最早冶炼锌的国家之一,有独立的炼锌发展史。现代炼锌主要采取湿法工艺,以闪锌矿(主要成分为 ,还含铁等元素)、软锰矿(主要成分为
,还含铁等元素)、软锰矿(主要成分为 )为原料联合生产锌和高纯度二氧化锰的一种流程如下:
)为原料联合生产锌和高纯度二氧化锰的一种流程如下:
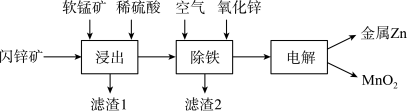
(1)浸出:加入 能促进
能促进 的溶解,提高锌的浸出率,同时生成硫单质。
的溶解,提高锌的浸出率,同时生成硫单质。 的作用类似催化剂,“催化”过程可表示为:
的作用类似催化剂,“催化”过程可表示为:
ⅰ:
ⅱ:……
①写出ⅱ的离子方程式:_______ 。
②下列实验方案可证实上述“催化”过程。将实验方案补充完整。
a.向酸化的 溶液中加入
溶液中加入 溶液,溶液几乎无色,再加入少量
溶液,溶液几乎无色,再加入少量 ,溶液变红。
,溶液变红。
b._______ 。
(2)除铁:已知①进入除铁工艺的溶液的pH约为3;②控制溶液pH为2.5~3.5,使铁主要以 沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量
沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量 的理由是
的理由是_______ 。
(3)电解:总反应(未配平): 。若不考虑副反应,为了使溶液中的
。若不考虑副反应,为了使溶液中的 、
、 均恰好完全反应,理论上需要再添加哪种离子?
均恰好完全反应,理论上需要再添加哪种离子?_______ (填“ ”、“
”、“ ”或“都不需要”)。
”或“都不需要”)。
 ,还含铁等元素)、软锰矿(主要成分为
,还含铁等元素)、软锰矿(主要成分为 )为原料联合生产锌和高纯度二氧化锰的一种流程如下:
)为原料联合生产锌和高纯度二氧化锰的一种流程如下:
(1)浸出:加入
 能促进
能促进 的溶解,提高锌的浸出率,同时生成硫单质。
的溶解,提高锌的浸出率,同时生成硫单质。 的作用类似催化剂,“催化”过程可表示为:
的作用类似催化剂,“催化”过程可表示为:ⅰ:

ⅱ:……
①写出ⅱ的离子方程式:
②下列实验方案可证实上述“催化”过程。将实验方案补充完整。
a.向酸化的
 溶液中加入
溶液中加入 溶液,溶液几乎无色,再加入少量
溶液,溶液几乎无色,再加入少量 ,溶液变红。
,溶液变红。b.
(2)除铁:已知①进入除铁工艺的溶液的pH约为3;②控制溶液pH为2.5~3.5,使铁主要以
 沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量
沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量 的理由是
的理由是(3)电解:总反应(未配平):
 。若不考虑副反应,为了使溶液中的
。若不考虑副反应,为了使溶液中的 、
、 均恰好完全反应,理论上需要再添加哪种离子?
均恰好完全反应,理论上需要再添加哪种离子? ”、“
”、“ ”或“都不需要”)。
”或“都不需要”)。
您最近一年使用:0次
名校
解题方法
4 . 空气质量评价的主要污染物为  等,一般来自于燃煤、工业废气、汽车尾气,会导致雾霾、酸雨的形成,危害环境。烟气中的
等,一般来自于燃煤、工业废气、汽车尾气,会导致雾霾、酸雨的形成,危害环境。烟气中的  可以用以下工艺除去。下列说法
可以用以下工艺除去。下列说法不正确 的是
 等,一般来自于燃煤、工业废气、汽车尾气,会导致雾霾、酸雨的形成,危害环境。烟气中的
等,一般来自于燃煤、工业废气、汽车尾气,会导致雾霾、酸雨的形成,危害环境。烟气中的  可以用以下工艺除去。下列说法
可以用以下工艺除去。下列说法
A.过程Ⅰ中, 和 和  均为反应物 均为反应物 |
B.过程Ⅱ中,发生反应:  |
C. 最终转化为 最终转化为  |
D. 在反应中作催化剂 在反应中作催化剂 |
您最近一年使用:0次
2024-02-19更新
|
346次组卷
|
2卷引用:北京市房山区2023-2024学年高一上学期期末检测化学试题
5 . N2O和CO是环境污染性气体,可在Pt2O+表面转化为无害气体,其反应原理如图所示。下列说法正确的是
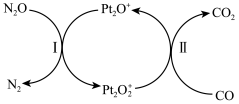

| A.Pt2O+的质量和化学性质不发生改变 | B.反应Ⅱ中,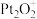 作还原剂 作还原剂 |
C.为了实现转化需不断补充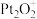 和Pt2O+ 和Pt2O+ | D.发生的化学反应为N2O+CO=CO2+N2 |
您最近一年使用:0次
名校
6 . H2O2是一种绿色试剂,在化学工业中用作生产过氧乙酸、亚氯酸钠等的原料,医药工业用作杀菌剂、消毒剂。某化学小组欲探究双氧水的性质做了如下实验:MnO2是中学实验中的常用试剂。常用来作为H2O2分解实验的催化剂。
甲同学设计如下实验探究影响双氧水分解反应速率的外界因素。
(1)写出相关反应方程式___________ 。
(2)若 且实验②反应后MnO2的质量和化学性质不变,则实验结论是
且实验②反应后MnO2的质量和化学性质不变,则实验结论是_________________ 。
(3)设计实验①和③的目的是___________________ 。
甲同学设计如下实验探究影响双氧水分解反应速率的外界因素。
| 实验 | 30%的双氧水/ | 温度/℃ | MnO2/g | 收集等体积的O2所用时间/s |
| ① | 20ml | 25 | 0 | a |
| ② | 20ml | 25 | 1 | b |
| ③ | 20ml | 50 | 0 | c |
(2)若
 且实验②反应后MnO2的质量和化学性质不变,则实验结论是
且实验②反应后MnO2的质量和化学性质不变,则实验结论是(3)设计实验①和③的目的是
您最近一年使用:0次
7 . 历史上曾利用HCl、CuCl2和O2制取氯气,反应原理如图所示。下列推断不正确 的是
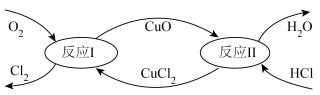

A.反应Ⅰ的化学方程式为 |
| B.反应Ⅱ属于复分解反应 |
| C.上述反应原理图中有2种元素化合价发生变化 |
| D.CuO是整个过程的催化剂 |
您最近一年使用:0次
8 . CO2捕获和转化可减少CO2排放并实现资源利用,原理如图1所示。反应①完成后,以N2为载气,将恒定组成的N2、CH4混合气,以恒定流速通入反应器,单位时间内流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到CO2,在催化剂上检测到有积炭( )。
)。

下列说法不正确 的是
 )。
)。
下列说法
| A.反应①为化合反应,CaO、CaCO3可循环利用 |
B. ,发生反应②: ,发生反应②: |
C. ,初始CH4物质的量 ,初始CH4物质的量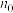 与反应后部分含碳物质物质的量n之间一定存在: 与反应后部分含碳物质物质的量n之间一定存在: |
D. 后,催化剂可能完全失去活性 后,催化剂可能完全失去活性 |
您最近一年使用:0次
名校
9 . 钯的配合物离子[PdC14]2-可催化合成H2O2,反应历程如图,下 列说法错误的是


| A.历程中发生了Pd+O2+2Cl-=[PdCl2O2]2- |
B.该过程的总反应为H2+O2 H2O2 H2O2 |
| C.[PdC14]2-在此过程中作为催化剂 |
| D.该过程中HCl的浓度减小(整个过程中溶液的体积不变) |
您最近一年使用:0次
10 . 为了深入探究某个化学问题,往往需要我们会依据一定的原理作出假设,并设计一定的化学实验方案。某化学兴趣小组的同学,对实验室制备氧气的若干问题进行如下探究:
[探究一]为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
(1)写出本实验中反应的化学方程式为___________ ;测量 体积的装置是
体积的装置是___________ (选填下图1中的装置编号)。
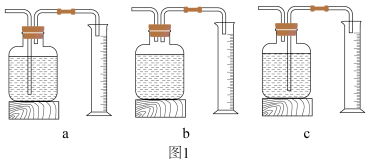
(2)由实验I、Ⅱ、Ⅲ可知:影响双氧水分解速率的因素是:___________
[探究二]B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂。于是他们用天平称量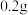 氧化铜,取5%过氧化氢溶液
氧化铜,取5%过氧化氢溶液 于试管中,进行如图2实验:
于试管中,进行如图2实验:
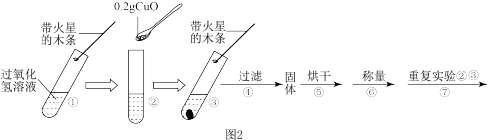
(3)填表:
(4)步骤①的目的是___________ 。
(5)步骤④需用到的玻璃仪器有铁架台(带铁圈)、烧杯、___________ 、___________ 。
(6)步骤⑦中应选用___________ 的过氧化氢溶液。
(7)过氧化氢能将二氧化硫氧化,请写出离子方程式为___________ 。
[探究一]为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
| 双氧水的质量 | 双氧水的浓度 |  的质量 的质量 | 相同时间内产生 的体积 的体积 | |
| I | 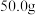 | 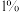 |  |  |
| Ⅱ | 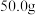 |  |  | 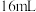 |
| Ⅲ | 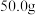 | 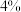 |  | 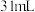 |
(1)写出本实验中反应的化学方程式为
 体积的装置是
体积的装置是
(2)由实验I、Ⅱ、Ⅲ可知:影响双氧水分解速率的因素是:
[探究二]B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂。于是他们用天平称量
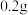 氧化铜,取5%过氧化氢溶液
氧化铜,取5%过氧化氢溶液 于试管中,进行如图2实验:
于试管中,进行如图2实验:
(3)填表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 称得氧化铜的质量为 | 将固体加入盛有过氧化氢溶液的试管中,并把带火星的木条伸入试管,观察现象。 | 在过氧化氢溶液的分解实验中,氧化铜也能作催化剂。 |
(4)步骤①的目的是
(5)步骤④需用到的玻璃仪器有铁架台(带铁圈)、烧杯、
(6)步骤⑦中应选用
(7)过氧化氢能将二氧化硫氧化,请写出离子方程式为
您最近一年使用:0次



