1 . CO2可转化成有机物实现碳循环。一定条件下,向体积为1L的密闭容器中充入1molCO2和3molH2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。

(1)9min时,容器中H2O的物质的量浓度为______ mol∙L−1。
(2)从3min到9min,υ(H2)=______ mol∙L−1min−1。
(3)平衡时CO2的转化率为______ 。
(4)第3min时,υ正______ υ逆(填“>”、“<”或“=”)。
(5)下列措施不能增大化学反应速率的是______ (填序号)。
a.向容器中再加入2molCO2和3molH2 b.升高温度
c.将密闭容器由1L改为2L d.加入金属Pt(催化剂)
 CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
(1)9min时,容器中H2O的物质的量浓度为
(2)从3min到9min,υ(H2)=
(3)平衡时CO2的转化率为
(4)第3min时,υ正
(5)下列措施不能增大化学反应速率的是
a.向容器中再加入2molCO2和3molH2 b.升高温度
c.将密闭容器由1L改为2L d.加入金属Pt(催化剂)
您最近一年使用:0次
名校
2 . 某研究小组同学用活性炭还原处理氮氧化物,向 恒容密闭容器中加入足量C与
恒容密闭容器中加入足量C与 发生反应,
发生反应, 。在不同实验条件下,平衡时
。在不同实验条件下,平衡时 与温度T的关系如图所示:
与温度T的关系如图所示:
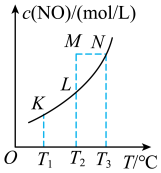
(1)结合图中数据,判断该反应的
___________ 0(填“>”或“<”),理由是___________ 。
(2)K、L、M、N四点对应的平衡常数分别为 、
、 、
、 、
、 ,判断其大小关系
,判断其大小关系_____ 。
使用氢能源可以减少汽车尾气中氮氧化合物的排放。利用甲醇与水蒸气反应可以制备氢气: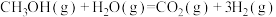 ,该反应过程中的能量变化如图:
,该反应过程中的能量变化如图:

(3)
___________ 0(填“>”“=”或“<”),途径(I)的活化能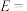
___________ 。
(4)途径(I)变为途径(II):改变的条件是___________ ,反应热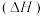
___________ (填“增大”“减小”或“不变”)。
(5)下列有关活化分子的说法正确的是___________。
 恒容密闭容器中加入足量C与
恒容密闭容器中加入足量C与 发生反应,
发生反应, 。在不同实验条件下,平衡时
。在不同实验条件下,平衡时 与温度T的关系如图所示:
与温度T的关系如图所示:
(1)结合图中数据,判断该反应的

(2)K、L、M、N四点对应的平衡常数分别为
 、
、 、
、 、
、 ,判断其大小关系
,判断其大小关系使用氢能源可以减少汽车尾气中氮氧化合物的排放。利用甲醇与水蒸气反应可以制备氢气:
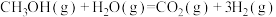 ,该反应过程中的能量变化如图:
,该反应过程中的能量变化如图:
(3)

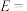
(4)途径(I)变为途径(II):改变的条件是
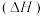
(5)下列有关活化分子的说法正确的是___________。
| A.增大反应物浓度可以提高活化分子百分数 |
| B.增大体系的压强一定能提高活化分子百分数 |
| C.使用合适的催化剂可以增大活化分子的能量 |
| D.升高温度能提高活化分子百分数 |
您最近一年使用:0次
2023-04-15更新
|
406次组卷
|
5卷引用:天津市第一中学2023-2024学年高二上学期10月月考化学试题
天津市第一中学2023-2024学年高二上学期10月月考化学试题上海市卢湾高级中学2022-2023学年高二下学期期中考试(等级考)化学试题上海市徐汇中学2022-2023学年高二下学期 5月月考化学(等级)试题(已下线)专题05 影响化学平衡的因素【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)山西省大同市第一中学校2023-2024学年高二上学期9月月考化学试题



