上海市徐汇中学2022-2023学年高二下学期 5月月考化学(等级)试题
上海
高二
阶段练习
2023-07-01
80次
整体难度:
适中
考查范围:
化学反应原理、认识化学科学、有机化学基础
上海市徐汇中学2022-2023学年高二下学期 5月月考化学(等级)试题
上海
高二
阶段练习
2023-07-01
80次
整体难度:
适中
考查范围:
化学反应原理、认识化学科学、有机化学基础
一、填空题 添加题型下试题
填空题
|
较难(0.4)
名校
1. 利用化学原理研究对废气进行脱硝处理,可实现绿色环保、废物利用,对构建生态文明有重要意义。合理应用和处理氮氧化合物,在生产生活中有着重要的意义。
I.
(1)闪电时空气中的 和
和 会发生反应:
会发生反应:
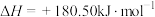 ,
,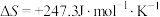 ,若不考虑温度对该反应焓变的影响,则下列说法中正确的是___________。
,若不考虑温度对该反应焓变的影响,则下列说法中正确的是___________。
II.已知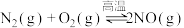 ,该反应在2404℃时的平衡常数
,该反应在2404℃时的平衡常数 。
。
(2)该温度下,向 密闭容器中充入
密闭容器中充入 与
与 各
各 ,平衡时
,平衡时 的转化率是
的转化率是___________ %(保留整数)。
(3)该温度下,某时刻测得容器内 、
、 、
、 的浓度分别为
的浓度分别为 、
、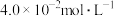 、
、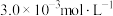 ,此时反应
,此时反应___________ (填“处于化学平衡状态”“正向进行”或“逆向进行”)。请说明理由___________ 。
(4)将 、
、 的混合气体充入恒温恒容密闭容器中,下图所示变化趋势正确的是
的混合气体充入恒温恒容密闭容器中,下图所示变化趋势正确的是___________ 。
A.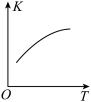 B.
B.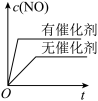 C.
C.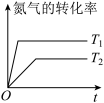
(5)向恒温恒容的密闭容器中充入等物质的量的 与
与 ,达到平衡状态后再向其中充入一定量
,达到平衡状态后再向其中充入一定量 ,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中
,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中 的体积分数
的体积分数___________ (填“变大”“变小”或“不变”)。
I.
(1)闪电时空气中的
 和
和 会发生反应:
会发生反应:
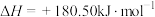 ,
,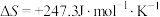 ,若不考虑温度对该反应焓变的影响,则下列说法中正确的是___________。
,若不考虑温度对该反应焓变的影响,则下列说法中正确的是___________。| A.在1000℃时,此反应能自发进行 |
| B.在1000℃时,此反应不能自发进行 |
| C.该反应能自发进行的最低温度约为730℃ |
D.该反应能自发进行的最高温度约为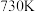 |
II.已知
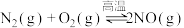 ,该反应在2404℃时的平衡常数
,该反应在2404℃时的平衡常数 。
。(2)该温度下,向
 密闭容器中充入
密闭容器中充入 与
与 各
各 ,平衡时
,平衡时 的转化率是
的转化率是(3)该温度下,某时刻测得容器内
 、
、 、
、 的浓度分别为
的浓度分别为 、
、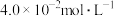 、
、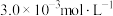 ,此时反应
,此时反应(4)将
 、
、 的混合气体充入恒温恒容密闭容器中,下图所示变化趋势正确的是
的混合气体充入恒温恒容密闭容器中,下图所示变化趋势正确的是A.
 B.
B. C.
C.
(5)向恒温恒容的密闭容器中充入等物质的量的
 与
与 ,达到平衡状态后再向其中充入一定量
,达到平衡状态后再向其中充入一定量 ,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中
,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中 的体积分数
的体积分数
您最近一年使用:0次
2023-04-15更新
|
400次组卷
|
3卷引用:上海市卢湾高级中学2022-2023学年高二下学期期中考试(等级考)化学试题
填空题
|
适中(0.65)
名校
2. 我国在汽车尾气和燃煤尾气的净化方面取得了一定成效。汽车尾气净化的主要原理为 。在密闭容器中发生该反应时,
。在密闭容器中发生该反应时, 随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
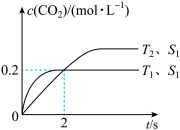
(1) 温度下,
温度下, 内的平均反应速率
内的平均反应速率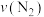
___________ 。
(2)当固体催化剂的质量一定时,将催化剂磨成粉末,则反应速率___________ (填“增大”“减小”或“不变”,下同), 转化率
转化率___________ 。
(3)若在绝热、恒容的密闭体系中充入一定量的 和
和 气体进行该反应,下列示意图正确且能说明反应在进行到
气体进行该反应,下列示意图正确且能说明反应在进行到 时刻达到平衡状态的是
时刻达到平衡状态的是___________ (填序号)。
a.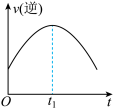 b.
b.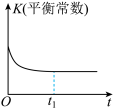 c.
c.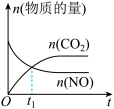 d.
d.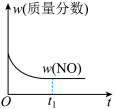
 。在密闭容器中发生该反应时,
。在密闭容器中发生该反应时, 随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
(1)
 温度下,
温度下, 内的平均反应速率
内的平均反应速率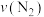
(2)当固体催化剂的质量一定时,将催化剂磨成粉末,则反应速率
 转化率
转化率(3)若在绝热、恒容的密闭体系中充入一定量的
 和
和 气体进行该反应,下列示意图正确且能说明反应在进行到
气体进行该反应,下列示意图正确且能说明反应在进行到 时刻达到平衡状态的是
时刻达到平衡状态的是a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
2023-04-15更新
|
235次组卷
|
2卷引用:上海市卢湾高级中学2022-2023学年高二下学期期中考试(等级考)化学试题
填空题
|
适中(0.65)
名校
3. 某研究小组同学用活性炭还原处理氮氧化物,向 恒容密闭容器中加入足量C与
恒容密闭容器中加入足量C与 发生反应,
发生反应, 。在不同实验条件下,平衡时
。在不同实验条件下,平衡时 与温度T的关系如图所示:
与温度T的关系如图所示:
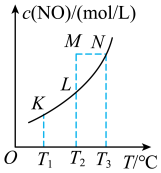
(1)结合图中数据,判断该反应的
___________ 0(填“>”或“<”),理由是___________ 。
(2)K、L、M、N四点对应的平衡常数分别为 、
、 、
、 、
、 ,判断其大小关系
,判断其大小关系_____ 。
使用氢能源可以减少汽车尾气中氮氧化合物的排放。利用甲醇与水蒸气反应可以制备氢气: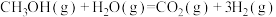 ,该反应过程中的能量变化如图:
,该反应过程中的能量变化如图:

(3)
___________ 0(填“>”“=”或“<”),途径(I)的活化能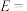
___________ 。
(4)途径(I)变为途径(II):改变的条件是___________ ,反应热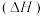
___________ (填“增大”“减小”或“不变”)。
(5)下列有关活化分子的说法正确的是___________。
 恒容密闭容器中加入足量C与
恒容密闭容器中加入足量C与 发生反应,
发生反应, 。在不同实验条件下,平衡时
。在不同实验条件下,平衡时 与温度T的关系如图所示:
与温度T的关系如图所示:
(1)结合图中数据,判断该反应的

(2)K、L、M、N四点对应的平衡常数分别为
 、
、 、
、 、
、 ,判断其大小关系
,判断其大小关系使用氢能源可以减少汽车尾气中氮氧化合物的排放。利用甲醇与水蒸气反应可以制备氢气:
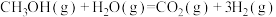 ,该反应过程中的能量变化如图:
,该反应过程中的能量变化如图:
(3)

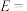
(4)途径(I)变为途径(II):改变的条件是
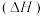
(5)下列有关活化分子的说法正确的是___________。
| A.增大反应物浓度可以提高活化分子百分数 |
| B.增大体系的压强一定能提高活化分子百分数 |
| C.使用合适的催化剂可以增大活化分子的能量 |
| D.升高温度能提高活化分子百分数 |
您最近一年使用:0次
2023-04-15更新
|
407次组卷
|
5卷引用:上海市卢湾高级中学2022-2023学年高二下学期期中考试(等级考)化学试题
上海市卢湾高级中学2022-2023学年高二下学期期中考试(等级考)化学试题上海市徐汇中学2022-2023学年高二下学期 5月月考化学(等级)试题(已下线)专题05 影响化学平衡的因素【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)天津市第一中学2023-2024学年高二上学期10月月考化学试题山西省大同市第一中学校2023-2024学年高二上学期9月月考化学试题
二、解答题 添加题型下试题
解答题-原理综合题
|
适中(0.65)
名校
解题方法
4. 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究重点。
【资料1】
已知:CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ•mol-1 ①
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=+247.4kJ•mol-1 ②
(1)以甲烷为原料制取氢气是工业上常用的制氢方法,CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_____ 。反之,工业上也可以调控条件利用CO2与H2反应可制备。有利于该反应自发的条件是_____ (填“高温”或“低温”)。
【资料II】
已知:2H2(g)+O2(g)=2H2O(g) △H1=-483.6kJ•mol-1
CH3OH(g)+ O2(g)=CO2(g)+2H2O(l) △H2=-764.7kJ•mol-1
O2(g)=CO2(g)+2H2O(l) △H2=-764.7kJ•mol-1

(2)①根据上述信息计算:断开1molH-O所需能量为_____ kJ。
②请你分析H2(g)作为能源比甲醇蒸汽作为能源的优点:_____ (写出两点)。
(3)高温下H2O可分解生成分子或原子。若在相同温度下,1molH2O按下列两种途径转化为氢原子与氧原子。则△H1、△H2、△H3三者之间的关系是_____ 。

(4)高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A表示的物质(或微粒)是_____ 。等物质的量的A、H2相比,化学能较低的物质是_____ 。

【资料1】
已知:CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ•mol-1 ①
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=+247.4kJ•mol-1 ②
(1)以甲烷为原料制取氢气是工业上常用的制氢方法,CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为
【资料II】
已知:2H2(g)+O2(g)=2H2O(g) △H1=-483.6kJ•mol-1
CH3OH(g)+
 O2(g)=CO2(g)+2H2O(l) △H2=-764.7kJ•mol-1
O2(g)=CO2(g)+2H2O(l) △H2=-764.7kJ•mol-1
(2)①根据上述信息计算:断开1molH-O所需能量为
②请你分析H2(g)作为能源比甲醇蒸汽作为能源的优点:
(3)高温下H2O可分解生成分子或原子。若在相同温度下,1molH2O按下列两种途径转化为氢原子与氧原子。则△H1、△H2、△H3三者之间的关系是

(4)高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A表示的物质(或微粒)是

您最近一年使用:0次
三、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
解题方法
5. 在菠菜等植物中含有丰富的草酸,草酸对生命活动有重要影响。草酸的学名叫乙二酸,是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料。常温下0.01mL的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示:
(1)草酸(H2C2O4)是一种二元弱酸。写出它在水中的电离方程式:_____ 。
(2)将0.1mol/L草酸溶液中[H2C2O4]、[HC2O ]、[C2O
]、[C2O ]按照由大到小的顺序排列:
]按照由大到小的顺序排列:_____ 。
(3)在H2C2O4溶液稀释过程中,下列物理量始终增大的是_____ 。
(4)KHC2O4溶液中c(H2C2O4)_____ c(C2O )(填>、<、=,下同),若0.1mol/LH2C2O4溶液中第二步电离产生的c(H+)=amol/L,则同浓度的KHC2O4溶液中HC2O
)(填>、<、=,下同),若0.1mol/LH2C2O4溶液中第二步电离产生的c(H+)=amol/L,则同浓度的KHC2O4溶液中HC2O 电离出来的c(H+)
电离出来的c(H+)_____ amol/L
(5)写出草酸钾(K2C2O4)溶液中的电荷守恒关系式_____ ,及物料守恒关系式_____ 。
| 物质 | H2C2O4 | KHC2O4 | K2C2O4 |
| pH | 2.1 | 3.1 | 8.1 |
(2)将0.1mol/L草酸溶液中[H2C2O4]、[HC2O
 ]、[C2O
]、[C2O ]按照由大到小的顺序排列:
]按照由大到小的顺序排列:(3)在H2C2O4溶液稀释过程中,下列物理量始终增大的是
A. | B.c(H+)•c(C2O ) ) |
C.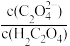 | D.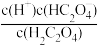 |
 )(填>、<、=,下同),若0.1mol/LH2C2O4溶液中第二步电离产生的c(H+)=amol/L,则同浓度的KHC2O4溶液中HC2O
)(填>、<、=,下同),若0.1mol/LH2C2O4溶液中第二步电离产生的c(H+)=amol/L,则同浓度的KHC2O4溶液中HC2O 电离出来的c(H+)
电离出来的c(H+)(5)写出草酸钾(K2C2O4)溶液中的电荷守恒关系式
您最近一年使用:0次



