名校
解题方法
1 . 已知难溶性化合物 的化学式为
的化学式为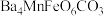 ,对
,对 进行如下实验,部分产物已经略去。
进行如下实验,部分产物已经略去。 中的金属元素在该实验条件下不能与
中的金属元素在该实验条件下不能与 产生配合物。
产生配合物。
(1) 高温下在
高温下在 气流中的反应
气流中的反应________ 氧化还原反应(填“属于”或“不属于”), 中钡元素的化合价为
中钡元素的化合价为________ 。
(2)步骤Ⅳ可以进行的原因除了生成 降低体系的能量之外,从化学平衡的角度解释能够发生的原因
降低体系的能量之外,从化学平衡的角度解释能够发生的原因________ 。
(3)下列说法正确的是________。
(4)固体 在一定条件下也可以与
在一定条件下也可以与 溶液反应,写出反应的离子方程式
溶液反应,写出反应的离子方程式________ 。
(5)设计实验检验混合气体A(除 外)的成份
外)的成份________ 。
 的化学式为
的化学式为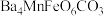 ,对
,对 进行如下实验,部分产物已经略去。
进行如下实验,部分产物已经略去。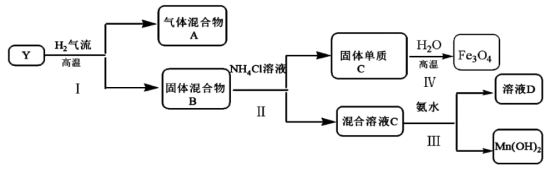
 中的金属元素在该实验条件下不能与
中的金属元素在该实验条件下不能与 产生配合物。
产生配合物。(1)
 高温下在
高温下在 气流中的反应
气流中的反应 中钡元素的化合价为
中钡元素的化合价为(2)步骤Ⅳ可以进行的原因除了生成
 降低体系的能量之外,从化学平衡的角度解释能够发生的原因
降低体系的能量之外,从化学平衡的角度解释能够发生的原因(3)下列说法正确的是________。
A.溶液D中阳离子只有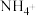 |
| B.若磁铁能吸引反应Ⅳ的剩余固体,则证明铁有剩余 |
| C.步骤Ⅱ中的氯化铵溶液也可以用盐酸代替 |
D.依据步骤Ⅲ可知碱性强弱 |
 在一定条件下也可以与
在一定条件下也可以与 溶液反应,写出反应的离子方程式
溶液反应,写出反应的离子方程式(5)设计实验检验混合气体A(除
 外)的成份
外)的成份
您最近半年使用:0次
名校
解题方法
2 . 某小组模拟工业上回收分银渣中的银,过程如下:

(1)Ⅰ中主要反应:
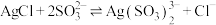 。研究发现:其他条件不变时,该反应在敞口容器中进行,浸出时间过长会使银的浸出率(浸出液中银的质量占起始分银渣中银的质量的百分比)降低,可能原因是
。研究发现:其他条件不变时,该反应在敞口容器中进行,浸出时间过长会使银的浸出率(浸出液中银的质量占起始分银渣中银的质量的百分比)降低,可能原因是(2)研究发现:浸出液中含银化合物总浓度与含硫化合物总浓度及浸出液pH的关系如下图。
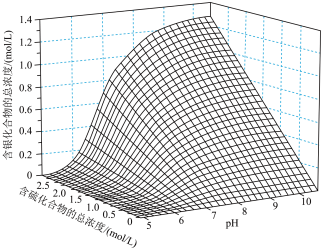
① 时,含银化合物总浓度随含硫化合物总浓度的变化趋势是
时,含银化合物总浓度随含硫化合物总浓度的变化趋势是
②解释①中变化趋势的原因:
③ 时,含银化合物总浓度随含硫化合物总浓度的变化与
时,含银化合物总浓度随含硫化合物总浓度的变化与 时不同,原因是
时不同,原因是
(3)将Ⅱ中反应的离子方程式补充完整
□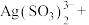 □
□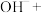 □___________
□___________ □___________
□___________ □___________
□___________ □___________
□___________
(4)Ⅲ中回收液可直接循环使用,但循环多次后,银的浸出率会降低。从回收液离子浓度变化和反应平衡的角度分析原因:
您最近半年使用:0次
解题方法
3 . 化合物X由四种元素组成,按如下流程进行实验。混合气体A由气体E和元素种类相同的另两种气体组成,且气体C的平均相对分子质量为8.5。混合物B中有两种固体。
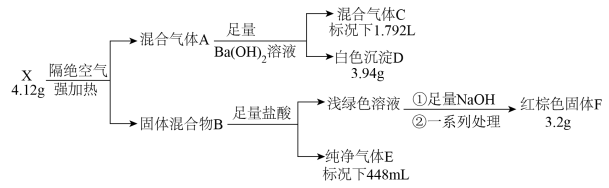
请回答:
(1)组成X的四种元素为_______ ;X的化学式为_______ 。
(2)写出由X到A的化学方程式_______ 。
(3)用盐酸溶解固体F,滴加一定量KSCN溶液,得到血红色溶液Y。往溶液Y中加入一定量KCl固体,溶液Y颜色变淡,请结合离子方程式说明原因_______ 。
(4)设计实验检验混合气体A中相对分子量较小的两种气体_______ 。

请回答:
(1)组成X的四种元素为
(2)写出由X到A的化学方程式
(3)用盐酸溶解固体F,滴加一定量KSCN溶液,得到血红色溶液Y。往溶液Y中加入一定量KCl固体,溶液Y颜色变淡,请结合离子方程式说明原因
(4)设计实验检验混合气体A中相对分子量较小的两种气体
您最近半年使用:0次
4 . 某物质A由三种常见的元素组成,某兴趣小组进行了如下实验:
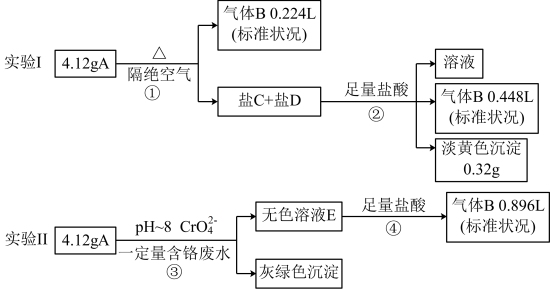
已知:A的摩尔质量在200~300g/mol之间,焰色为紫色;盐C和盐D的组成元素和A相同,①②④处气体体积均在充分加热挥发后经干燥测定。
(1)组成A的元素有_______ ;A的化学式_______ ;
(2)无色溶液E中所有阴离子结合H+的能力由强到弱的顺序_______ ;
(3)一种生产A的方法:在35~45℃下气体B与锌粉—水悬浮液反应生成中间产物;然后加入相应的碱溶液,充分反应,压滤分离得A溶液。写出该过程的总反应方程式_______ ;
(4)A可除去废水(pH~8)中的Cr(VI),且处理后pH变化不大,则反应③的离子方程式_______ ;
(5)设计实验确定溶液E中所含溶质的阴离子_______ ;

已知:A的摩尔质量在200~300g/mol之间,焰色为紫色;盐C和盐D的组成元素和A相同,①②④处气体体积均在充分加热挥发后经干燥测定。
(1)组成A的元素有
(2)无色溶液E中所有阴离子结合H+的能力由强到弱的顺序
(3)一种生产A的方法:在35~45℃下气体B与锌粉—水悬浮液反应生成中间产物;然后加入相应的碱溶液,充分反应,压滤分离得A溶液。写出该过程的总反应方程式
(4)A可除去废水(pH~8)中的Cr(VI),且处理后pH变化不大,则反应③的离子方程式
(5)设计实验确定溶液E中所含溶质的阴离子
您最近半年使用:0次
名校
5 . 铬是不锈钢中一种重要的元素,铬的毒性与其存在的价态有关,低价铬对人体基本无害,六价铬比三价铬毒性高100倍,并易被人体吸收且在体内蓄积,有关含铬化合物的相互转化关系如图甲。
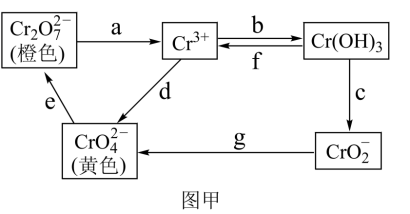
回答下列问题:
(1)从图甲中信息判断,Cr(OH)3是___________ 氢氧化物(填“酸性”、“碱性”或“两性”),相关反应的离子方程式为___________ 。
(2)图甲中所示转化过程中需要加入氧化剂的是___________ (填写表示转化过程的小写字母)。
(3)在水溶液中橙色的 与黄色的
与黄色的 有下列平衡关系:
有下列平衡关系: +H2O
+H2O 2
2 +2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是
+2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是___________ 。
(4)CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率( )随温度的变化如图乙所示。
)随温度的变化如图乙所示。
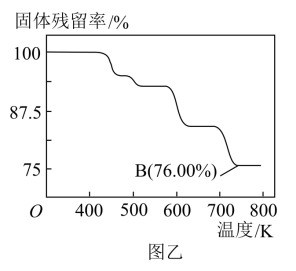
①三氧化铬在稀硫酸环境中氧化乙醇,CrO3变为绿色的Cr2(SO4)3,乙醇被完全氧化为CO2,则其化学方程式是___________ 。
②图乙中B点所示固体的化学式是___________ 。

回答下列问题:
(1)从图甲中信息判断,Cr(OH)3是
(2)图甲中所示转化过程中需要加入氧化剂的是
(3)在水溶液中橙色的
 与黄色的
与黄色的 有下列平衡关系:
有下列平衡关系: +H2O
+H2O 2
2 +2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是
+2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是(4)CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率(
 )随温度的变化如图乙所示。
)随温度的变化如图乙所示。
①三氧化铬在稀硫酸环境中氧化乙醇,CrO3变为绿色的Cr2(SO4)3,乙醇被完全氧化为CO2,则其化学方程式是
②图乙中B点所示固体的化学式是
您最近半年使用:0次
解题方法
6 . 甲、乙、丙三种化合物均由氢、氮、氧、铜四种元素中两种元素组成。常温下,甲是一种含氮质量分数为87.5%的液态化合物,相对分子质量与空气中某种主要成分的相对分子质量相同;乙和丙是铜的两种常见氧化物,乙是新制的氢氧化铜与乙醛反应的还原产物。试回答下列问题:
(1)甲的结构式___ 。
(2)甲和丙反应的产物中含有乙和一种气态单质,写出其化学方程式___ 。
(3)向乙固体中加入过量硫酸酸化的硫酸铁溶液,乙固体完全溶解,得到透明溶液。
①写出其离子方程式___ 。
②若所得溶液阳离子浓度均约为0.1mol⋅L-1,再向所得混合液中加丙,最先得到___ 沉淀(不同浓度的金属离子开始和完全以氢氧化物沉淀的pH如图)。
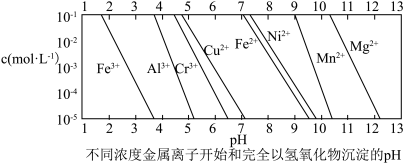
③向上述混合液加入有机萃取剂(RH)发生反应:2RH(有机相)+Cu2+(水相)⇌R2Cu(有机相)+2H+(水相),已知其它阳离子与该有机物不能发生反应,也不相溶。试设计实验验证有机相中含有铜元素___ 。
(1)甲的结构式
(2)甲和丙反应的产物中含有乙和一种气态单质,写出其化学方程式
(3)向乙固体中加入过量硫酸酸化的硫酸铁溶液,乙固体完全溶解,得到透明溶液。
①写出其离子方程式
②若所得溶液阳离子浓度均约为0.1mol⋅L-1,再向所得混合液中加丙,最先得到

③向上述混合液加入有机萃取剂(RH)发生反应:2RH(有机相)+Cu2+(水相)⇌R2Cu(有机相)+2H+(水相),已知其它阳离子与该有机物不能发生反应,也不相溶。试设计实验验证有机相中含有铜元素
您最近半年使用:0次
2011·山西太原·三模
解题方法
7 . 已知A~N分别代表一种物质,它们之间的转化关系如图所示(部分反应的反应条件和生成物已略去)。A、B、C分别是由短周期元素组成的单质,A是金属,D是无色液体。F是一种离子化含物,其阴阳离子的个数比为1:3,且能与水反应得到两种碱。反应①是实验室检验某离子的方法,反应②是工业、生产N的重要反应。请回答下列问题:
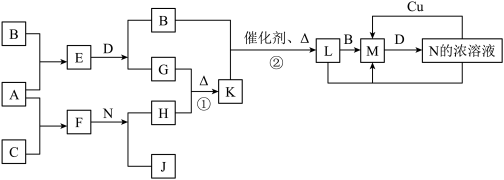
(1)B元素在元素周期表中的位置是__________ ,F的电子式是_____________ 。
(2)写出反应①的离子方程式:___________ ;
(3)Cu与足量的N的浓溶液反应得到的产物主要是M不是L,其原因是__________ (请用上图所示关系中反应的化学方程式回答)。
(4)选择性催化还原(SCR)是在有催化剂的条件下将M转变为无毒的物质,这是目前国外进行尾气治理遍采用的一种方法。亚铬酸铜(Adkin偿化剂)是极好的M催化还原的催化剂,是铜和铬的复合氧化物,成分不固定,如:aCuO·bCr2O3等,统称为亚铬酸铜。其中:CuNH4(OH)CrO4在295℃分解生成复合的氧化物(催化剂)、氮气及水,写出该反应的化学方程式:______________________ 。
(5)已知一定温度(>100℃)下,反应②的平衡常数为1。将0.8molK和1.1molB放入容积为1L的封闭容器中,发生反应②,一段时间后L的浓度为0.4mol/L,此时反应v正_____ v逆(填“>”、“<”或“=”)。当反应到达平衡后,保持温度不变,再加入一定物质的量的B,重新达到平衡,则L的平衡浓度__________ (填“增大”、“不变”或“减小”),B的转化率_________ 。(填“升高”、“不变”或“降低”),L的体积分数___________ (填“增大”、“不变”、“减小”或“无法确定”)。

(1)B元素在元素周期表中的位置是
(2)写出反应①的离子方程式:
(3)Cu与足量的N的浓溶液反应得到的产物主要是M不是L,其原因是
(4)选择性催化还原(SCR)是在有催化剂的条件下将M转变为无毒的物质,这是目前国外进行尾气治理遍采用的一种方法。亚铬酸铜(Adkin偿化剂)是极好的M催化还原的催化剂,是铜和铬的复合氧化物,成分不固定,如:aCuO·bCr2O3等,统称为亚铬酸铜。其中:CuNH4(OH)CrO4在295℃分解生成复合的氧化物(催化剂)、氮气及水,写出该反应的化学方程式:
(5)已知一定温度(>100℃)下,反应②的平衡常数为1。将0.8molK和1.1molB放入容积为1L的封闭容器中,发生反应②,一段时间后L的浓度为0.4mol/L,此时反应v正
您最近半年使用:0次



